Com la psilocibina pot remodelar el cervell adult
- Què és la neuroplasticitat i com funciona en el cervell adult
- Fonaments biològics i farmacologia de la psilocibina
- Com la psilocibina transforma el cervell adult
- Psilocibina com a psicoplastogen: els mecanismes del canvi neuronal
- Per què la psilocibina actua diferent de la serotonina
- El BDNF i el seu paper en la plasticitat induïda per psilocibina
- Per què els efectes neuroplàstics de la psilocibina són duradors?
- Psilocibina i canvis estructurals en preclínica
- Psilocibina i modulació de la Xarxa Neuronal per Defecte
- Evidència de la psilocibina en assajos clínics amb humans
- Depressió resistent al tractament
- Depressió moderada-greu: l'assaig comparatiu amb escitalopram
- Ansietat i depressió associades a malaltia terminal
- Trastorns per ús de substàncies
- Riscos d'una neuroplasticitat no adaptativa
- La integració com a eix de la plasticitat post-psicodèlica
- Fonts i referències
- Mecanisme molecular i neuroplasticitat
- Períodes crítics
- Xarxa Neuronal per Defecte i entropia cerebral
- Evidència clínica — Depressió
- Evidència clínica — Ansietat i malaltia terminal
- Evidència clínica — Addiccions
Imagina el cervell com una muntanya coberta de neu. Cada pensament recurrent, cada reacció automàtica i cada hàbit mental és un trineu que davalla una i altra vegada pel mateix recorregut. Amb el temps, aquests camins es converteixen en solcs profunds: eficients i ràpids… però cada vegada més difícils d'abandonar.
Aquesta imatge resumeix bé el que passa en molts estats de rigidesa psicològica. L'estrès crònic, l'ansietat, la depressió o fins i tot la rutina quotidiana reforcen patrons de pensament repetitius. No perquè siguin els millors, sinó perquè són els més transitats. El cervell, com qualsevol sistema biològic, tendeix a optimitzar allò que ja coneix.
Durant dècades es va assumir que aquesta rigidesa era, en gran mesura, irreversible en l'edat adulta. Avui sabem que no té per què ser-ho. El cervell conserva una capacitat notable per canviar, adaptar-se i reorganitzar-se. A aquesta propietat l'anomenem neuroplasticitat.
En els últims anys, els bolets psicodèlics (en particular les espècies del gènere Psilocybe) han reaparegut en la recerca científica com a possibles catalitzadors d'aquesta plasticitat. No només pels estats alterats de consciència que produeixen, sinó per alguna cosa més profunda i duradora: la seva capacitat per induir canvis estructurals i funcionals en el cervell que persisteixen molt més enllà de l'experiència aguda.
Aquest article explora què significa realment la neuroplasticitat, com actua la psilocibina sobre el cervell, què diu l'evidència científica actual i quines són les seves implicacions, límits i riscos.
Què és la neuroplasticitat i com funciona en el cervell adult
La neuroplasticitat és la capacitat del sistema nerviós per reorganitzar-se a diferents nivells: molecular, cel·lular, estructural i funcional. Implica tant la creació de noves connexions com l'eliminació d'aquelles que deixen de ser adaptatives —un procés de ‘neteja’ natural anomenat poda sinàptica que permet que el cervell no només creixi, sinó que es refini.
Durant molt de temps es va pensar que aquesta capacitat es reduïa dràsticament després de la infància, una idea heretada dels primers models del desenvolupament cerebral. Avui sabem que el cervell adult continua sent plàstic, tot i que aquesta plasticitat sol estar més “regulada” i menys disponible de forma espontània.
Per comprendre com els psicodèlics interactuen amb aquests processos, cal distingir diversos tipus de plasticitat rellevants:
- Plasticitat estructural: inclou el creixement de dendrites, la formació de noves sinapsis i els canvis en la densitat d'espines dendrítiques. És el substrat físic de l'aprenentatge: cada vegada que el cervell consolida alguna cosa nova, ho fa en part modificant l'arquitectura de les seves neurones, afegint o reforçant els punts de contacte entre elles.
- Plasticitat funcional: la reorganització de les xarxes cerebrals i dels patrons de comunicació entre diferents regions. No implica necessàriament canvis estructurals visibles, sinó canvis en quins circuits s'activen junts, amb quina intensitat i amb quina sincronia. És la plasticitat que permet, per exemple, que una regió danyada sigui parcialment compensada per una altra, o que un hàbit mental crònic es vagi debilitant quan deixem d'alimentar-lo.
- Meta-plasticitat: un concepte clau que opera a un nivell superior als anteriors: no només canvien les connexions, sinó el llindar perquè es produeixin canvis futurs. És a dir, el propi cervell modula quant de fàcil o difícil li resulta tornar a modelar-se en resposta a l'experiència. Un cervell que ha passat per períodes d'alt estrès sostingut, per exemple, pot tornar-se menys receptiu als canvis adaptatius; un en un estat de plasticitat elevada, al contrari, respon amb més facilitat a nous aprenentatges i experiències.
- Reobertura de períodes crítics: Aquest és un dels conceptes més avantguardistes —i també dels més preliminars— de la neurociència actual. Es refereix a finestres temporals d'extrema sensibilitat a l'entorn que, biològicament, solen tancar-se després de la infància o adolescència. L'evidència recent suggereix que els psicodèlics poden tornar a obrir aquestes “portes”, retornant el cervell a un estat de mal·leabilitat social i emocional on és possible reescriure aprenentatges profunds —com traumes o patrons d'aferrament— que fins ara es consideraven immutables. És important subratllar, no obstant això, que aquesta línia de recerca encara no compta amb replicacions robustes en humans i s'ha d'interpretar amb cautela.
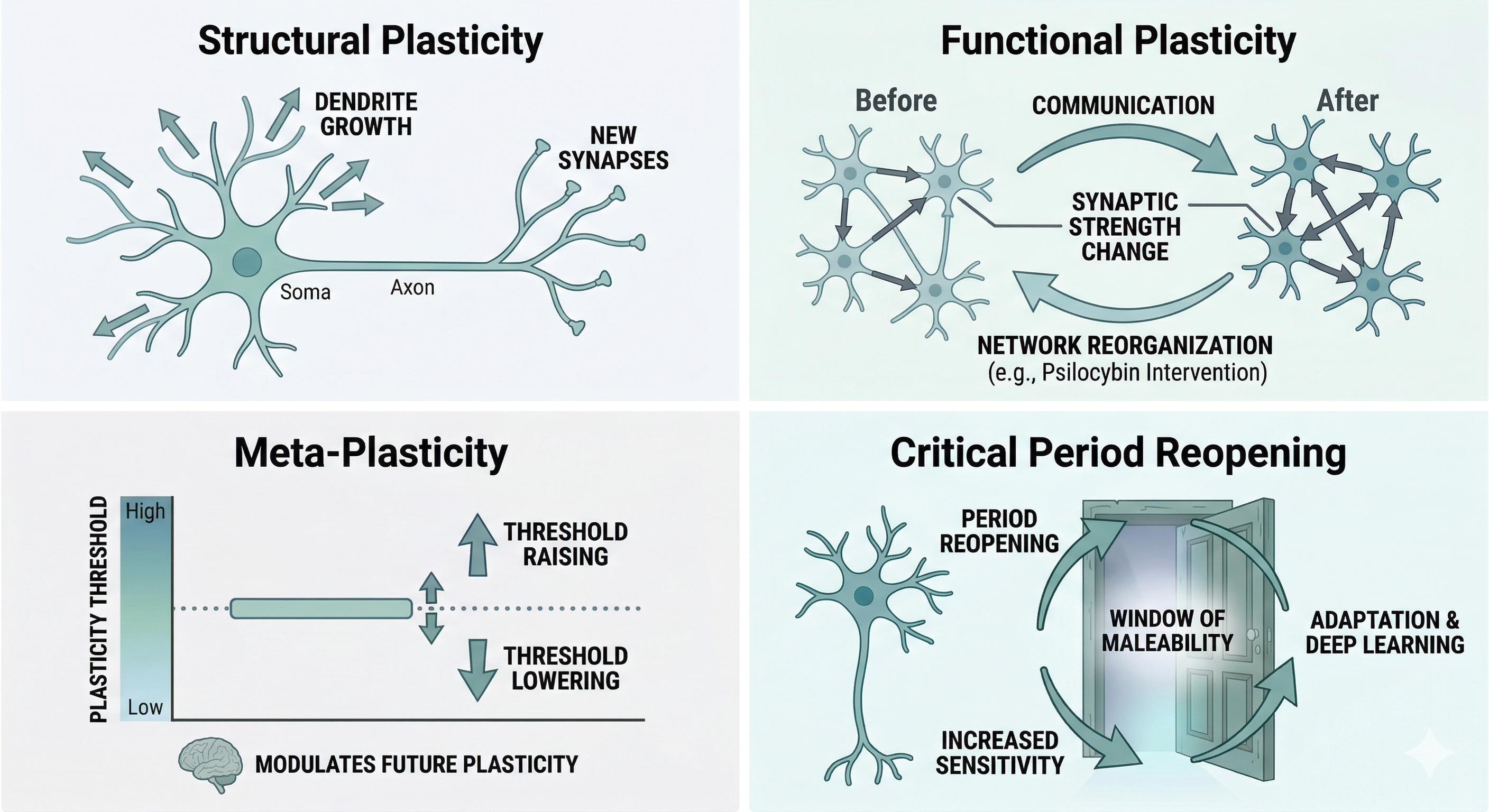
Aquests diferents tipus de plasticitat proporcionen el marc conceptual per entendre com substàncies com la psilocibina poden induir canvis cerebrals significatius fins i tot en l'adult.
Fonaments biològics i farmacologia de la psilocibina
Els bolets psicodèlics, especialment les espècies del gènere Psilocybe, produeixen de forma natural psilocibina. És important destacar que la psilocibina és, en rigor, un profàrmac: una substància que per si mateixa no és significativament activa, però que el cos metabolitza (principalment al fetge) per convertir-la en psilocina, que és la molècula que realment travessa la barrera hematoencefàlica i genera els efectes en el cervell.
A diferència de molts altres metabòlits secundaris produïts per bolets i plantes, la psilocibina mostra una afinitat notable pel sistema serotoninèrgic humà, en particular per certs receptors implicats en processos com la percepció, la cognició i la regulació emocional.
Tot i que estan relacionats, la recerca actual suggereix que els segons no poden explicar-se únicament pels primers. Aquesta distinció és crucial, ja que suggereix que la veritable potència terapèutica de la psilocibina podria residir no només en la intensitat de l'experiència subjectiva, sinó en la «finestra d'oportunitat» biològica que s'obre a nivell cel·lular. Entendre la substància com un modulador estructural ens permet separar el fenomen de l'al·lucinació del procés de reparació i recablatge neuronal que analitzarem a continuació.
Un tercer element, tan determinant com la dosi o el mecanisme molecular, és el que la recerca anomena set and setting: el set fa referència a l'estat intern del participant —la seva disposició emocional, les seves expectatives i la seva història personal—; el setting a l'entorn físic, social i relacional en què es produeix l'experiència. En els assajos clínics, tots dos es controlen acuradament mitjançant preparació prèvia, acompanyament professional i sessions d'integració posteriors. Aquesta variable no és accessòria: els estudis mostren que el mateix compost, administrat en contextos diferents, pot produir experiències radicalment diferents, i que la qualitat del set and setting prediu en part la magnitud i la direcció del canvi terapèutic.
Com la psilocibina transforma el cervell adult
Psilocibina com a psicoplastogen: els mecanismes del canvi neuronal
En els últims anys ha sorgit un terme clau per descriure substàncies com la psilocibina: els psicoplastogens. El concepte, proposat en el context de la recerca moderna per equips com el de David E. Olson, es refereix a compostos capaços de promoure de forma ràpida i potent la neuroplasticitat, més enllà dels seus efectes subjectius.
Abans d'entrar en els mecanismes moleculars, cal assenyalar una distinció que sovint s'omet en la divulgació sobre aquest tema: no existeix un únic “mode d'ús” de la psilocibina, i els contextos d'administració produeixen perfils biològics i terapèutics molt diferents. En l'àmbit clínic i investigador es distingeixen principalment dues aproximacions:
- La dosi terapèutica —la emprada en els assajos clínics moderns— implica dosis mitjanes o altes (generalment entre 20 i 30 mg de psilocibina sintètica, o el seu equivalent en bolet sec) administrades en sessions úniques o molt escasses, sempre amb acompanyament professional i preparació prèvia. Produeix estats alterats de consciència d'entre quatre i sis hores de durada i és el model sobre el qual s'acumula la major part de l'evidència neurobiològica i terapèutica.
- La microdosificació, per la seva banda, consisteix en la ingesta periòdica de dosis subperceptuals —habitualment entre 0,1 i 0,3 grams de bolet sec— al llarg de dies o setmanes, sense que es produeixin alteracions perceptives notables. Tot i que la pràctica ha guanyat popularitat i existeix una àmplia base d'usuaris que reporten beneficis en focus, estat d'ànim o creativitat, l'evidència científica sobre els seus efectes neuroplàstics específics és avui considerablement més limitada i menys sistemàtica. La gran majoria de les troballes que es descriuen en aquest article corresponen al model de dosi terapèutica.
Per què la psilocibina actua diferent de la serotonina
Tradicionalment es pensava que n'hi havia prou amb activar els receptors 5-HT2A situats a la superfície de la neurona per desencadenar els efectes psicodèlics. No obstant això, recerques recents han revelat un matís neurobiològic crucial: la localització.
A diferència de la serotonina endògena, que té dificultats per travessar la membrana cel·lular a causa de la seva polaritat, la psilocina (i altres psicodèlics) pot creuar aquesta barrera lipídica i accedir a l'interior de la cèl·lula. Un cop dins, s'uneix a una reserva de receptors 5-HT2A ubicats en orgànuls intracel·lulars, com l'aparell de Golgi.
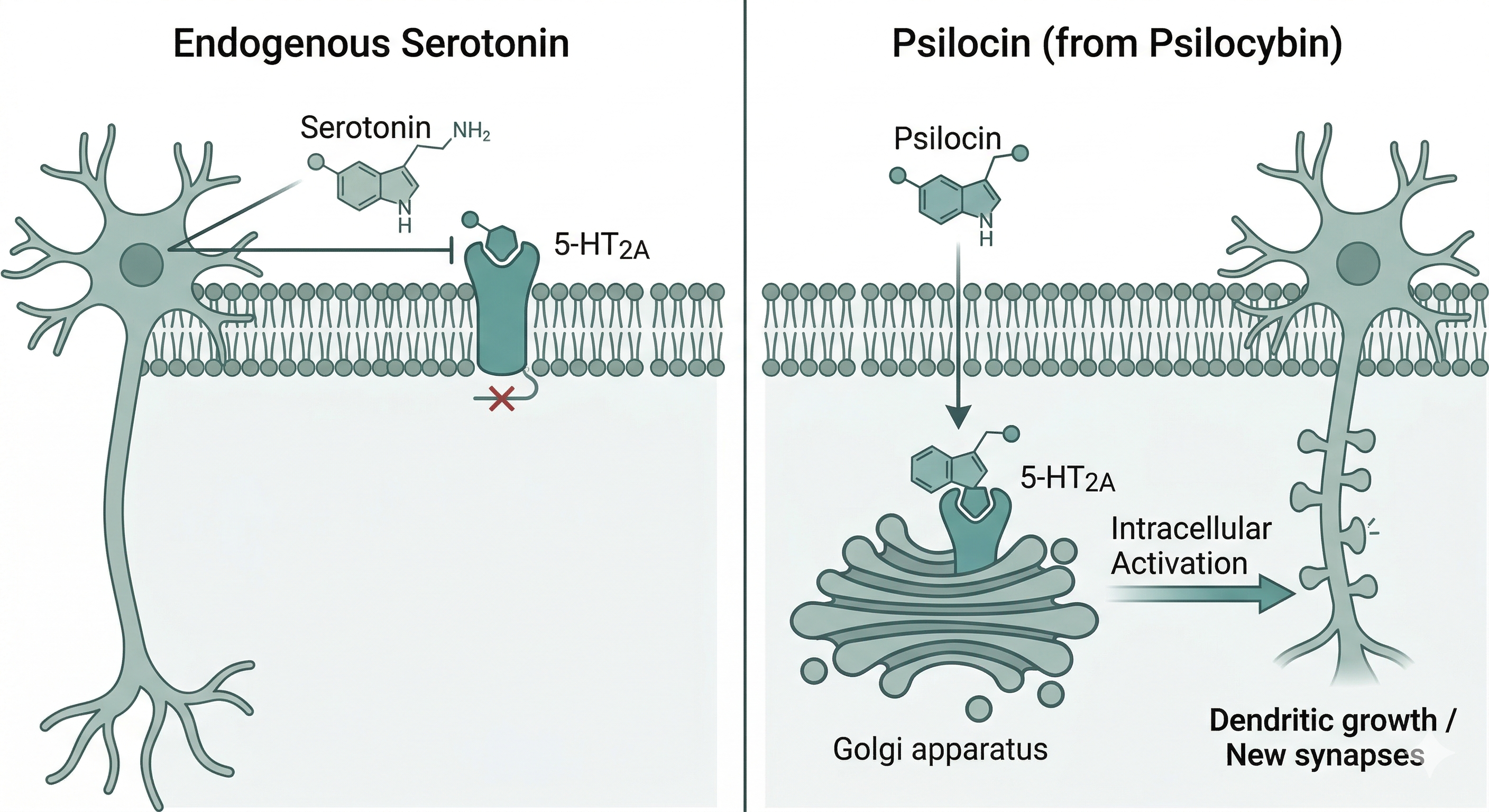
L'evidència actual suggereix que és precisament aquesta activació intracel·lular la que desencadena de forma consistent el creixement de les dendrites i la formació de noves espines. Això explicaria per què, tot i que tenim serotonina al cervell constantment, aquesta no provoca els canvis estructurals profunds ni els estats de plasticitat ràpida que observem amb els psicodèlics.
El BDNF i el seu paper en la plasticitat induïda per psilocibina
Un dels actors clau en aquest procés és el BDNF (Factor Neurotròfic Derivat del Cervell), una proteïna fonamental per al creixement, la supervivència i la diferenciació neuronal. La psilocibina s'associa amb un augment en l'expressió i alliberament de BDNF, la qual cosa facilita l'activació del seu receptor TrkB i contribueix a la consolidació de noves connexions sinàptiques.
Alguns estudis suggereixen que certs efectes plàstics poden produir-se de forma parcialment independent del receptor 5-HT2A, la qual cosa apunta a mecanismes més complexos del que s'assumia inicialment.
Aquests canvis moleculars es tradueixen potencialment en un cervell més flexible i capaç de reorganitzar les seves xarxes, la qual cosa fonamenta millores en aprenentatge, adaptació i regulació emocional.
Aquest efecte es veu a més potenciat per un mecanisme que tractarem més endavant: la reducció simultània de l'activitat ruminant de la DMN, la hiperactivitat crònica de la qual actua com a supressor actiu de l'expressió de BDNF a través de l'eix de l'estrès.
Per què els efectes neuroplàstics de la psilocibina són duradors?
Tot i que la psilocibina s'elimina de l'organisme en qüestió d'hores, els canvis que indueix poden persistir durant setmanes o fins i tot mesos. Aquesta aparent paradoxa s'explica perquè la substància no actua únicament com un estímul transitori, sinó com un desencadenant de processos biològics que continuen desenvolupant-se un cop finalitzada la fase aguda.
Un dels mecanismes implicats és l'activació de programes d'expressió gènica associats a la plasticitat sinàptica. La psilocibina indueix l'expressió de gens de resposta immediata i d'altres gens implicats en el creixement neuronal, l'estabilització de sinapsis i la reorganització de circuits. Aquests canvis moleculars poden consolidar-se amb el temps mitjançant la síntesi de noves proteïnes i la modificació estructural de les connexions existents.
A més, la formació de noves espines dendrítiques i el reforçament de determinades sinapsis no són processos efímers. Un cop establertes, aquestes modificacions poden integrar-se de forma relativament estable en les xarxes neuronals, especialment si van acompanyades de canvis en l'experiència, el comportament o l'entorn de l'individu.
A nivell funcional, la psilocibina també s'associa amb una reorganització transitòria de les dinàmiques de connectivitat cerebral. Durant aquest període, el cervell pot explorar configuracions menys rígides i més flexibles. En alguns casos, certes d'aquestes configuracions persisteixen després de l'experiència, donant lloc a patrons de processament més adaptatius.
Aquestes dades suggereixen que la durada dels efectes no depèn de la presència contínua de la substància, sinó de la capacitat de la psilocibina per iniciar una cascada de canvis moleculars, estructurals i funcionals que, sota determinades condicions, poden consolidar-se a mitjà i llarg termini.
Psilocibina i canvis estructurals en preclínica
Els estudis preclínics han estat fonamentals per caracteritzar com la psilocibina indueix canvis plàstics a nivell cel·lular i estructural. En cultius cel·lulars, exposicions breus a psilocibina o a compostos anàlegs produeixen augments significatius en la complexitat dendrítica i en la densitat sinàptica en un termini de 24 a 72 hores. Resulta especialment rellevant que estímuls de curta durada puguin generar efectes comparables als observats després de tractaments prolongats.
En models animals, una única administració s'associa amb un augment de la densitat d'espines dendrítiques en regions clau com el còrtex prefrontal medial i l'hipocamp. Aquests canvis poden persistir durant diverses setmanes, i fins i tot més d'un mes. A més, en models d'estrès crònic, la psilocibina reverteix l'atròfia dendrítica induïda per l'estrès i s'associa amb millores en indicadors de comportament adaptatiu.
Aquestes troballes proporcionen un suport mecanístic sòlid que justifica l'exploració de la psilocibina en estudis clínics en humans.
Psilocibina i modulació de la Xarxa Neuronal per Defecte
Per comprendre els efectes psicològics i terapèutics de la psilocibina, és imprescindible parlar de la Xarxa Neuronal per Defecte (DMN), un conjunt de regions cerebrals altament interconnectades que actuen com un eix organitzador de l'experiència interna.
La DMN és especialment activa quan no realitzem una tasca concreta orientada a l'exterior. S'associa amb la narrativa del jo, la memòria autobiogràfica, la planificació mental i l'avaluació constant d'un mateix. Quan la seva activitat és excessiva o rígida, es relaciona amb patrons de ruminació, autocrítica i pensament repetitiu.
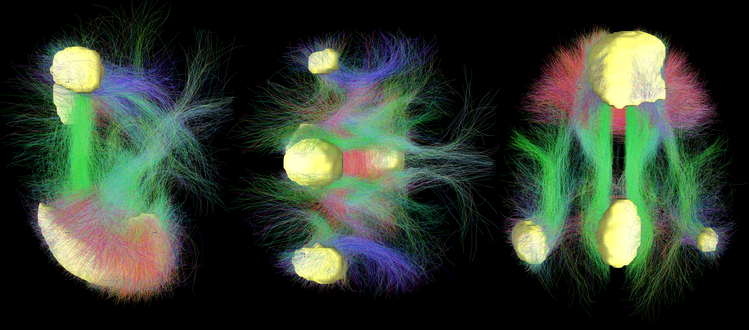
La psilocibina redueix de forma significativa la coherència i la dominància funcional d'aquesta xarxa. És com si el “gerent” del cervell —el sistema que centralitza, prioritza i dóna continuïtat a l'experiència— es retirés temporalment. Aquest descens en el control jeràrquic es correlaciona amb la disminució de l'activitat sincronitzada dins de la DMN i és el que moltes persones descriuen subjectivament com una dissolució de l'ego.
Quan aquest control es relaxa, augmenta la connectivitat global entre xarxes cerebrals. Regions que normalment operen de forma més segregada comencen a intercanviar informació de manera més directa. Aquest patró de connectivitat menys restrictiu s'ha associat a fenòmens com la sinestèsia, els reencadraments cognitius profunds i l'emergència de perspectives no habituals.
Aquest augment de connectivitat global es tradueix en el que la neurociència descriu com un increment de l'entropia cerebral: el cervell opera en un espai d'estats més ampli, amb patrons d'activació menys predictibles i més variables. Lluny de ser un signe de desorganització patològica, aquesta entropia elevada reflecteix un cervell temporalment alliberat de les seves rutines perceptives i cognitives més rígides —més semblant, en termes de dinàmica de xarxa, al cervell d'un nen explorant el món que al d'un adult resolent allò conegut.
Des del punt de vista de la neuroplasticitat, un cervell menys jeràrquic i menys constrenyit per models interns dominants és un cervell més mal·leable. Aquesta finestra de flexibilitat és clau per entendre per què certes experiències induïdes per la psilocibina poden facilitar canvis psicològics duradors.
Evidència de la psilocibina en assajos clínics amb humans
Abans d'entrar en els estudis concrets, cal emmarcar l'estat actual del camp. La recerca clínica amb psilocibina ha avançat notablement en l'última dècada, però continua operant amb mostres relativament petites, protocols heterogenis i una limitació estructural difícil de resoldre: el doble cec verdader és pràcticament impossible quan els participants poden percebre amb claredat si van rebre la substància activa. Això no invalida les troballes —la consistència dels efectes a través de diferents grups, institucions i metodologies és en si mateixa un senyal sòlid— però sí que exigeix llegir els resultats amb la precisió que mereix qualsevol ciència en construcció.
Depressió resistent al tractament
Els assajos més influents provenen del grup de Robin Carhart-Harris, iniciats al Imperial College de Londres i posteriorment continuats a la Universitat de Califòrnia San Francisco. Els seus estudis amb pacients que no havien respost a múltiples línies de tractament farmacològic convencional van documentar reduccions significatives en la simptomatologia depressiva després d'una o dues sessions de psilocibina integrades en un protocol de suport psicoterapèutic.
En neuroimatge funcional, aquests treballs van revelar una reducció persistent de l'activitat de la DMN setmanes després de la intervenció, correlacionada amb la millora clínica.
Depressió moderada-greu: l'assaig comparatiu amb escitalopram
El mateix grup va liderar posteriorment un assaig amb una població diferent: pacients amb depressió moderada-greu sense criteri de resistència al tractament. L'assaig publicat al The New England Journal of Medicine el 2021 va comparar psilocibina amb l'antidepressiu escitalopram i va mostrar resultats comparables en l'escala de símptomes primària —tot i que l'endpoint primari no va assolir significació estadística, en part pel tamany mostral— i resultats superiors per al grup de psilocibina en diverses mesures secundàries de benestar emocional. L'escitalopram va presentar resposta més ràpida en les primeres setmanes, la qual cosa suggereix que les dues intervencions tenen perfils temporals diferents i potencialment complementaris.
Ansietat i depressió associades a malaltia terminal
El grup de Roland Griffiths a la Johns Hopkins University ha produït alguns dels assajos més acuradament dissenyats del camp. En un estudi controlat amb aleatorització amb pacients oncològics amb diagnòstic potencialment mortal, una única dosi alta de psilocibina va produir reduccions clínicament significatives tant en ansietat com en depressió, que es van mantenir estables en seguiments realitzats als sis mesos. En aproximadament el 80 % dels participants els efectes beneficiosos continuaven sent perceptibles en avaluacions a llarg termini, una dada de persistència inusual en psicofarmacologia. Els autors van observar a més que la intensitat de l'experiència mística durant la sessió correlacionava amb la magnitud del benefici terapèutic posterior, la qual cosa ha alimentat el debat sobre la rellevància del component experiencial en el mecanisme d'acció.
Trastorns per ús de substàncies
La recerca ha donat resultats preliminars notables. El grup de Johns Hopkins va publicar un estudi pilot sobre dependència al tabac en el qual dues o tres sessions de psilocibina combinades amb teràpia cognitivo-conductual van produir taxes d'abstinència als sis mesos superiors al 60 %, molt per sobre dels referents històrics dels tractaments de primera línia. Per al trastorn per ús d'alcohol, un assaig controlat de la Universitat de Nova York va reportar reduccions sostingudes i significatives en el consum enfront de placebo actiu. Ambdues línies de recerca són encara incipients en termes de tamany mostral i requereixen replicació, però la magnitud dels efectes observats justifica l'interès creixent.
Tècniques de neuroimatge funcional i estructural mostren canvis en la connectivitat entre regions prefrontals i subcorticals setmanes després d'una única administració. Aquestes modificacions afecten circuits implicats en la regulació emocional, la presa de decisions i la resposta a l'estrès. Així mateix, s'han descrit variacions en el gruix cortical en àrees relacionades amb el control cognitiu i la integració emocional.
A nivell psicològic, s'han documentat millores sostingudes en flexibilitat cognitiva, empatia emocional i benestar subjectiu. Aquests canvis no van acompanyats d'un deteriorament de les funcions cognitives bàsiques, com la memòria de treball o l'atenció, la qual cosa reforça el perfil de seguretat observat en els estudis controlats.
En contextos terapèutics controlats, especialment en depressió resistent o ansietat, els efectes beneficiosos poden mantenir-se durant mesos i fins i tot fins a un any després d'una o dues sessions, sempre integrades en un marc d'acompanyament psicològic.
| Condició | Institució | Resultat Clau |
|---|---|---|
| Depressió Resistent | Imperial College / UCSF | Millora ràpida; superior a fàrmacs comuns en benestar a llarg termini. |
| Ansietat Terminal | Johns Hopkins University | 80% d'èxit amb millora clínica sostinguda després de 6 mesos. |
| Addicció al Tabac | Johns Hopkins University | 60% d'abstinència als 6 mesos (dobla l'eficàcia convencional). |
| Ús d'Alcohol | NYU | Descens significatiu en dies de consum excessiu enfront de placebo. |
Riscos d'una neuroplasticitat no adaptativa
La psilocibina indueix canvis cerebrals reals. Això significa que els riscos també són reals. L'exemple més clar és el HPPD (trastorn perceptual persistent post-al·lucinogen): distorsions visuals que reapareixen setmanes o mesos després de l'experiència. És la demostració més directa que més plasticitat no equival automàticament a “millor” plasticitat: en certs individus, els circuits de processament es consoliden de maneres no desitjades.
Perquè aquesta finestra de mal·leabilitat sigui terapèutica i no desestabilitzadora, el cribratge mèdic previ i el context són innegociables. Sense un marc de seguretat i una integració posterior, el cervell pot reforçar patrons poc adaptatius en lloc de trencar-los. Aquestes són les exclusions mèdiques i farmacològiques sistemàtiques en la recerca clínica:
Criteris d'exclusió i precaucions mèdiques
- Salut Mental: Antecedents personals o familiars de psicosi, esquizofrènia o trastorn bipolar tipus I.
- Interaccions Farmacològiques: Ús de Liti (risc de convulsions), IMAO o antidepressius serotoninèrgics.
- Condicions Físiques: Cardiopaties no controlades, epilèpsia activa o embaràs.
- Seguretat Psicològica: No es recomana l'ús sense acompanyament professional en casos de trauma complex no processat.
La precisió en el cribratge és el que separa una experiència transformadora d'un risc innecessari. Per a una anàlisi tècnica detallada de cada interacció i protocol de seguretat, podeu consultar la nostra guia completa de riscos i contraindicacions de la psilocibina.
La integració com a eix de la plasticitat post-psicodèlica
Després de l'experiència psicodèlica, el cervell roman durant dies o setmanes en un estat de plasticitat elevada. Tornant a la nostra metàfora inicial: la neu fresca cobreix els solcs antics. Però la neu no decideix per si sola quins nous camins es formen. Si no hi ha canvis en l'entorn, els hàbits o l'acompanyament terapèutic, el pes de la repetició tornarà a obrir exactament els mateixos solcs d'abans. I això té conseqüències en les dues direccions.
Per això, la integració és fonamental. L'evidència indica que la psilocibina no és una panacea, sinó un modulador: un senyal que el cervell interpreta per construir —o eliminar— connexions reals a nivell molecular, estructural i funcional.
Aquest procés pot persistir mesos després d'una única sessió, oferint implicacions terapèutiques genuïnes en depressió, ansietat i addiccions. No obstant això, els efectes depenen del context i el camp continua sent una ciència en construcció. En un territori on la biologia i l'experiència subjectiva se superposen, la precisió no és un detall: és el punt de partida.
Fonts i referències
Mecanisme molecular i neuroplasticitat
- Olson, D.E. (2021) — Proposta del concepte de psicoplastogens i el seu potencial terapèutic. Journal of Experimental Neuroscience.
- Ly, C. et al. (2018) — Evidència que els psicodèlics promouen plasticitat estructural i funcional en neurones corticals. Cell Reports.
- Vargas, M.V. et al. (2023) — Demostració que els receptors 5-HT2A intracel·lulars medien els efectes neuroplàstics. Science.
Períodes crítics
- Nardou, R. et al. (2023) — Els psicodèlics reobren el període crític d'aprenentatge de recompensa social. Nature.
Xarxa Neuronal per Defecte i entropia cerebral
- Carhart-Harris, R.L. et al. (2012) — Correlats neuronals de l'estat psicodèlic mesurats amb fMRI i reducció de la DMN. PNAS.
- Carhart-Harris, R.L. et al. (2014) — La teoria del cervell entròpic: increment de l'entropia com a substrat de l'experiència. Frontiers in Human Neuroscience.
Evidència clínica — Depressió
- Carhart-Harris, R. et al. (2021) — Assaig comparatiu entre psilocibina i escitalopram en depressió moderada-greu. New England Journal of Medicine.
- Davis, A.K. et al. (2021) — Efectes de la teràpia assistida amb psilocibina en trastorn depressiu major. JAMA Psychiatry.
Evidència clínica — Ansietat i malaltia terminal
- Griffiths, R.R. et al. (2016) — Reducció substancial i sostinguda de depressió i ansietat en pacients oncològics. Journal of Psychopharmacology.
- Ross, S. et al. (2016) — Reducció ràpida i sostinguda d'ansietat i depressió en càncer avançat. Journal of Psychopharmacology.
Evidència clínica — Addiccions
- Johnson, M.W. et al. (2014) — Psilocibina com a suport per a la cessació tabàquica: estudi pilot. Journal of Psychopharmacology.
- Bogenschutz, M.P. et al. (2015) — Estudi de concepte sobre psilocibina en dependència a l'alcohol. Journal of Psychopharmacology.
- Bogenschutz, M.P. et al. (2022) — Assaig controlat sobre psilocibina en trastorn per ús d'alcohol. JAMA Psychiatry.
Posts relacionats
-
Aplicacions terapèutiques de la psilocibina
Publicat : 2025-07-31 14:25:24 -
Psilocibina: què és, com actua i quins efectes provoca
Publicat : 2025-07-24 12:21:12 -
Mites sobre la psilocibina que la ciència desmenteix
Publicat : 2025-12-10 20:34:04























