Como a psilocibina pode remodelar o cérebro adulto
- O que é a neuroplasticidade e como funciona no cérebro adulto
- Fundamentos biológicos e farmacologia da psilocibina
- Como a psilocibina transforma o cérebro adulto
- Psilocibina como psicoPlastogénio: os mecanismos da mudança neuronal
- Por que razão a psilocibina age de forma diferente da serotonina
- O BDNF e o seu papel na plasticidade induzida pela psilocibina
- Por que razão os efeitos neuroplásticos da psilocibina são duradouros?
- Psilocibina e mudanças estruturais em pré-clínica
- Psilocibina e modulação da Rede Neuronal por Defeito
- Evidência da psilocibina em ensaios clínicos com humanos
- Depressão resistente ao tratamento
- Depressão moderada-grave: o ensaio comparativo com escitalopram
- Ansiedade e depressão associadas a doença terminal
- Perturbações por uso de substâncias
- Riscos de uma neuroplasticidade não adaptativa
- A integração como eixo da plasticidade pós-psicodélica
- Fontes e referências
- Mecanismo molecular e neuroplasticidade
- Períodos críticos
- Rede Neuronal por Defeito e entropia cerebral
- Evidência clínica — Depressão
- Evidência clínica — Ansiedade e doença terminal
- Evidência clínica — Dependências
Imagine o cérebro como uma montanha coberta de neve. Cada pensamento recorrente, cada reação automática e cada hábito mental é um trenó que desce repetidamente pelo mesmo percurso. Com o tempo, esses caminhos tornam-se sulcos profundos: eficientes e rápidos… mas cada vez mais difíceis de abandonar.
Esta imagem resume bem o que acontece em muitos estados de rigidez psicológica. O stress crónico, a ansiedade, a depressão ou mesmo a rotina quotidiana reforçam padrões de pensamento repetitivos. Não porque sejam os melhores, mas porque são os mais percorridos. O cérebro, como qualquer sistema biológico, tende a otimizar o que já conhece.
Durante décadas, assumiu-se que esta rigidez era, em grande medida, irreversível na idade adulta. Hoje sabemos que não tem de ser assim. O cérebro conserva uma capacidade notável para mudar, adaptar-se e reorganizar-se. A esta propriedade chamamos neuroplasticidade.
Nos últimos anos, os cogumelos psicodélicos (em particular as espécies do género Psilocybe) reapareceram na investigação científica como possíveis catalisadores desta plasticidade. Não apenas pelos estados alterados de consciência que produzem, mas por algo mais profundo e duradouro: a sua capacidade de induzir mudanças estruturais e funcionais no cérebro que persistem muito além da experiência aguda.
Este artigo explora o que significa realmente a neuroplasticidade, como a psilocibina age sobre o cérebro, o que diz a evidência científica atual e quais são as suas implicações, limites e riscos.
O que é a neuroplasticidade e como funciona no cérebro adulto
A neuroplasticidade é a capacidade do sistema nervoso para se reorganizar a diferentes níveis: molecular, celular, estrutural e funcional. Implica tanto a criação de novas conexões como a eliminação daquelas que deixam de ser adaptativas — um processo de ‘limpeza’ natural chamado poda sináptica que permite que o cérebro não só cresça, mas também se refine.
Durante muito tempo pensou-se que esta capacidade diminuía drasticamente após a infância, uma ideia herdada dos primeiros modelos do desenvolvimento cerebral. Hoje sabemos que o cérebro adulto continua a ser plástico, embora essa plasticidade tenda a estar mais “regulada” e menos disponível de forma espontânea.
Para compreender como os psicodélicos interagem com estes processos, é necessário distinguir vários tipos de plasticidade relevantes:
- Plasticidade estrutural: inclui o crescimento de dendrites, a formação de novas sinapses e as alterações na densidade de espinhas dendríticas. É o substrato físico da aprendizagem: cada vez que o cérebro consolida algo novo, fá-lo em parte modificando a arquitetura dos seus neurónios, adicionando ou reforçando os pontos de contacto entre eles.
- Plasticidade funcional: a reorganização das redes cerebrais e dos padrões de comunicação entre diferentes regiões. Não implica necessariamente mudanças estruturais visíveis, mas sim mudanças nos circuitos que se ativam em conjunto, com que intensidade e com que sincronia. É a plasticidade que permite, por exemplo, que uma região danificada seja parcialmente compensada por outra, ou que um hábito mental crónico se vá enfraquecendo quando deixamos de o alimentar.
- Meta-plasticidade: um conceito chave que opera a um nível superior aos anteriores: não só as conexões mudam, como também o limiar para que ocorram mudanças futuras. Ou seja, o próprio cérebro modula a facilidade ou dificuldade com que volta a moldar-se em resposta à experiência. Um cérebro que passou por períodos de stress elevado e sustentado, por exemplo, pode tornar-se menos recetivo a mudanças adaptativas; um em estado de plasticidade elevada, pelo contrário, responde com mais facilidade a novas aprendizagens e experiências.
- Reabertura de períodos críticos: Este é um dos conceitos mais vanguardistas — e também dos mais preliminares — da neurociência atual. Refere-se a janelas temporais de extrema sensibilidade ao ambiente que, biologicamente, tendem a fechar-se após a infância ou adolescência. A evidência recente sugere que os psicodélicos podem reabrir estas “portas”, devolvendo ao cérebro um estado de maleabilidade social e emocional onde é possível reescrever aprendizagens profundas — como traumas ou padrões de vinculação — que até agora eram consideradas imutáveis. É importante sublinhar, no entanto, que esta linha de investigação ainda não conta com replicações robustas em humanos e deve ser interpretada com cautela.
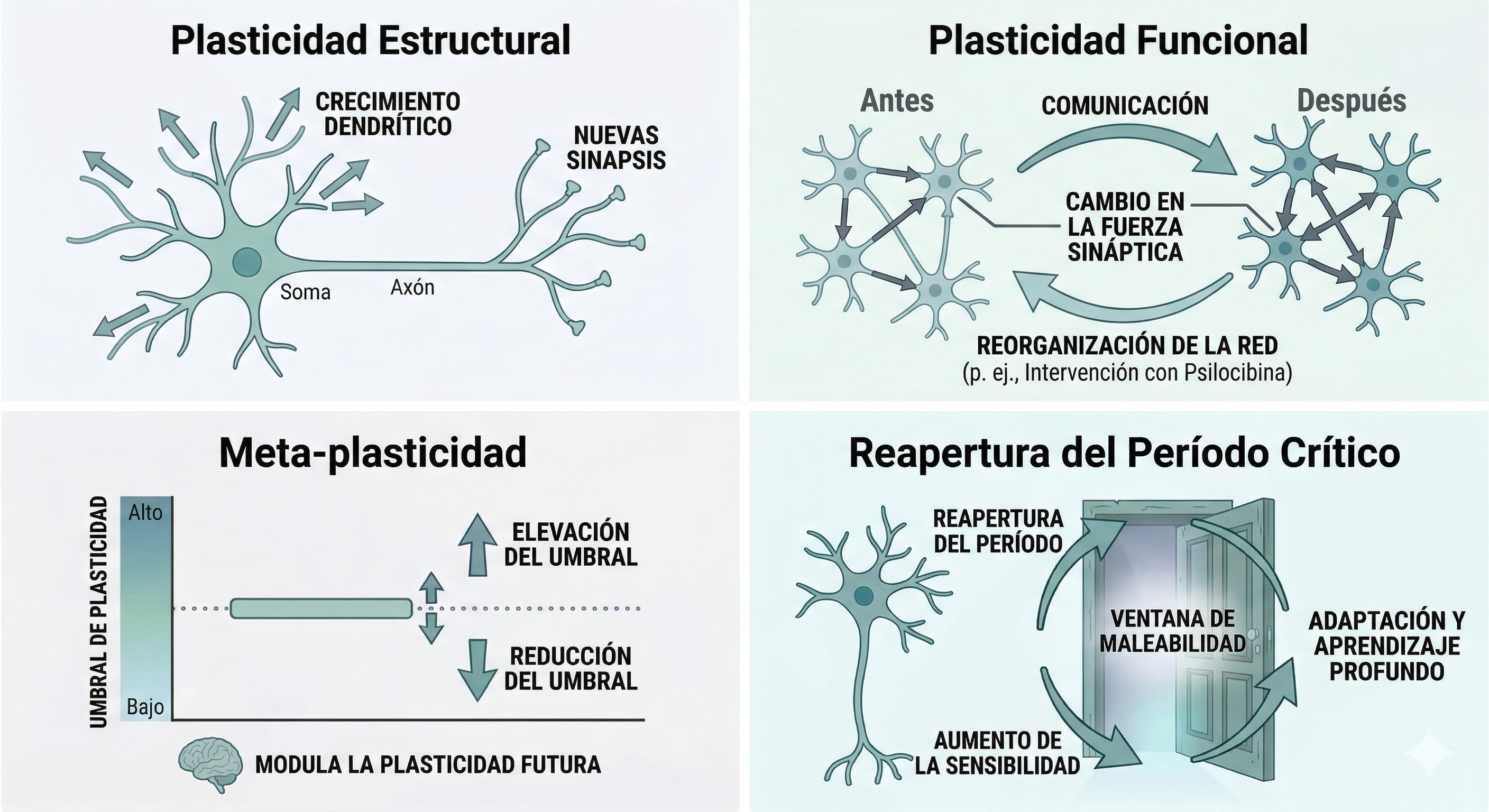
Estes diferentes tipos de plasticidade fornecem o quadro conceptual para compreender como substâncias como a psilocibina podem induzir mudanças cerebrais significativas mesmo no adulto.
Fundamentos biológicos e farmacologia da psilocibina
Os cogumelos psicodélicos, especialmente as espécies do género Psilocybe, produzem naturalmente psilocibina. É importante destacar que a psilocibina é, em rigor, um pró-fármaco: uma substância que por si mesma não é significativamente ativa, mas que o organismo metaboliza (principalmente no fígado) para a converter em psilocina, que é a molécula que realmente atravessa a barreira hematoencefálica e gera os efeitos no cérebro.
Ao contrário de muitos outros metabolitos secundários produzidos por fungos e plantas, a psilocibina apresenta uma afinidade notável pelo sistema serotoninérgico humano, em particular por certos recetores envolvidos em processos como a perceção, a cognição e a regulação emocional.
Embora estejam relacionados, a investigação atual sugere que os segundos não podem ser explicados unicamente pelos primeiros. Esta distinção é crucial, pois sugere que a verdadeira potência terapêutica da psilocibina pode residir não apenas na intensidade da experiência subjetiva, mas na «janela de oportunidade» biológica que se abre ao nível celular. Entender a substância como um modulador estrutural permite-nos separar o fenómeno da alucinação do processo de reparação e recableamento neuronal que analisaremos a seguir.
Um terceiro elemento, tão determinante como a dose ou o mecanismo molecular, é o que a investigação designa por set and setting: o set refere-se ao estado interno do participante — a sua disposição emocional, as suas expectativas e a sua história pessoal —; o setting ao ambiente físico, social e relacional em que ocorre a experiência. Nos ensaios clínicos, ambos são cuidadosamente controlados através de preparação prévia, acompanhamento profissional e sessões de integração posteriores. Esta variável não é acessória: os estudos mostram que o mesmo composto, administrado em contextos diferentes, pode produzir experiências radicalmente diferentes, e que a qualidade do set and setting prediz em parte a magnitude e a direção da mudança terapêutica.
Como a psilocibina transforma o cérebro adulto
Psilocibina como psicoPlastogénio: os mecanismos da mudança neuronal
Nos últimos anos surgiu um termo chave para descrever substâncias como a psilocibina: os psicoplastogénios. O conceito, proposto no contexto da investigação moderna por equipas como a de David E. Olson, refere-se a compostos capazes de promover de forma rápida e potente a neuroplasticidade, para além dos seus efeitos subjetivos.
Antes de abordar os mecanismos moleculares, convém assinalar uma distinção que frequentemente é omitida na divulgação sobre este tema: não existe um único “modo de utilização” da psilocibina, e os contextos de administração produzem perfis biológicos e terapêuticos muito diferentes. No âmbito clínico e de investigação distinguem-se principalmente duas abordagens:
- A dose terapêutica — a utilizada nos ensaios clínicos modernos — implica doses médias ou altas (geralmente entre 20 e 30 mg de psilocibina sintética, ou o seu equivalente em cogumelo seco) administradas em sessões únicas ou muito escassas, sempre com acompanhamento profissional e preparação prévia. Produz estados alterados de consciência com duração entre quatro e seis horas e é o modelo sobre o qual se acumula a maior parte da evidência neurobiológica e terapêutica.
- A microdosagem, por sua vez, consiste na ingestão periódica de doses sub-percetivas — habitualmente entre 0,1 e 0,3 gramas de cogumelo seco — ao longo de dias ou semanas, sem que ocorram alterações percetivas notáveis. Embora a prática tenha ganho popularidade e exista uma ampla base de utilizadores que reportam benefícios em foco, humor ou criatividade, a evidência científica sobre os seus efeitos neuroplásticos específicos é hoje consideravelmente mais limitada e menos sistemática. A grande maioria dos resultados descritos neste artigo corresponde ao modelo de dose terapêutica.
Por que razão a psilocibina age de forma diferente da serotonina
Tradicionalmente pensava-se que bastava ativar os recetores 5-HT2A situados na superfície do neurónio para desencadear os efeitos psicodélicos. No entanto, investigações recentes revelaram um matiz neurobiológico crucial: a localização.
Ao contrário da serotonina endógena, que tem dificuldade em atravessar a membrana celular devido à sua polaridade, a psilocina (e outros psicodélicos) pode cruzar esta barreira lipídica e aceder ao interior da célula. Uma vez dentro, liga-se a uma reserva de recetores 5-HT2A localizados em organelos intracelulares, como o aparelho de Golgi.
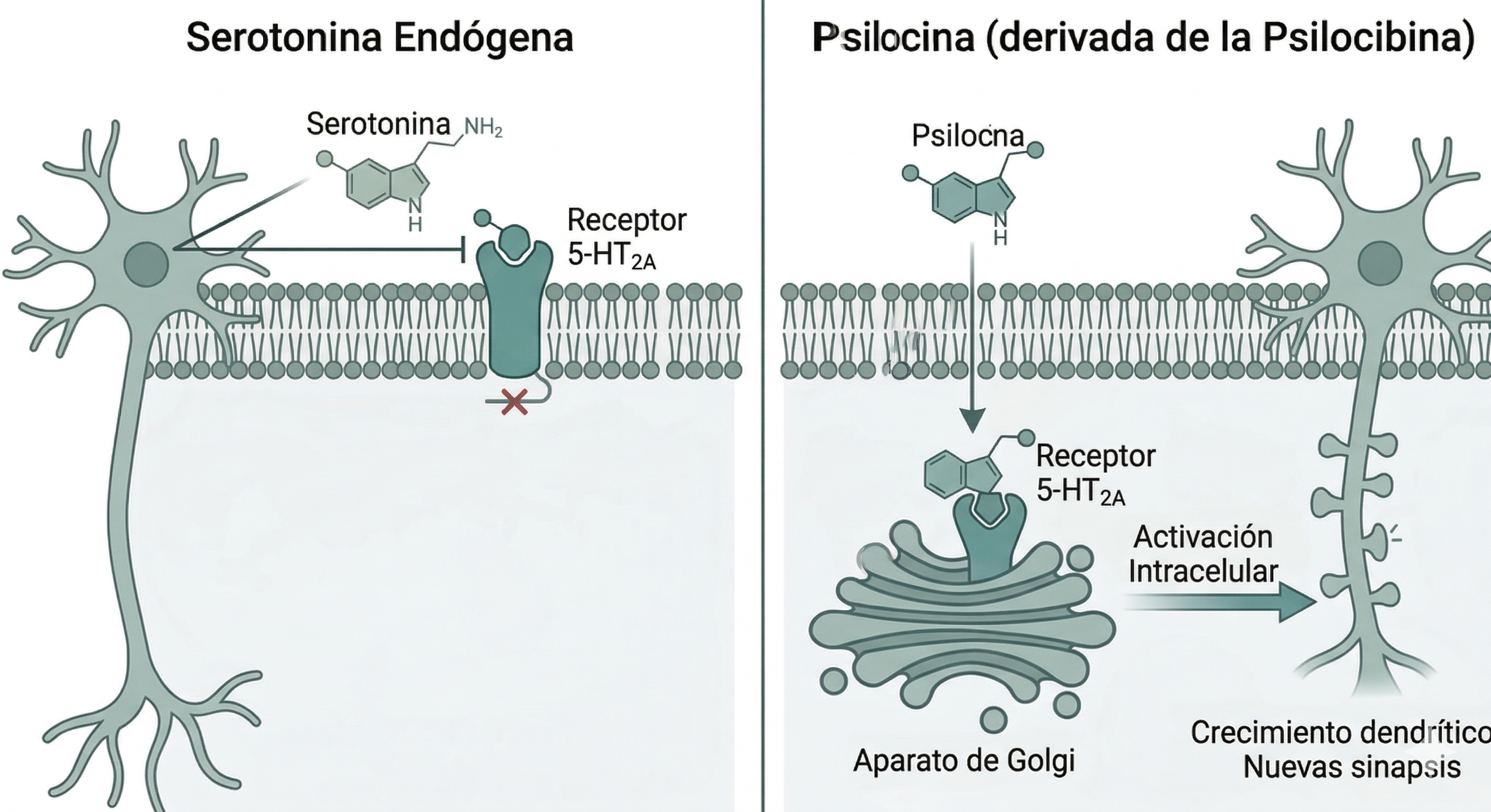
A evidência atual sugere que é precisamente esta ativação intracelular que desencadeia de forma consistente o crescimento das dendrites e a formação de novas espinhas. Isto explicaria por que razão, embora tenhamos serotonina no cérebro constantemente, esta não provoca as mudanças estruturais profundas nem os estados de plasticidade rápida que observamos com os psicodélicos.
O BDNF e o seu papel na plasticidade induzida pela psilocibina
Um dos atores chave neste processo é o BDNF (Fator Neurotrófico Derivado do Cérebro), uma proteína fundamental para o crescimento, a sobrevivência e a diferenciação neuronal. A psilocibina está associada a um aumento na expressão e libertação de BDNF, o que facilita a ativação do seu recetor TrkB e contribui para a consolidação de novas conexões sinápticas.
Alguns estudos sugerem que certos efeitos plásticos podem ocorrer de forma parcialmente independente do recetor 5-HT2A, o que aponta para mecanismos mais complexos do que o inicialmente assumido.
Estas mudanças moleculares traduzem-se potencialmente num cérebro mais flexível e capaz de reorganizar as suas redes, o que sustenta melhorias na aprendizagem, na adaptação e na regulação emocional.
Este efeito é ainda amplificado por um mecanismo que abordaremos mais adiante: a redução simultânea da atividade ruminativa da DMN, cuja hiperatividade crónica atua como supressor ativo da expressão de BDNF através do eixo do stress.
Por que razão os efeitos neuroplásticos da psilocibina são duradouros?
Embora a psilocibina seja eliminada do organismo em poucas horas, as mudanças que induz podem persistir durante semanas ou mesmo meses. Este aparente paradoxo explica-se pelo facto de a substância não atuar apenas como um estímulo transitório, mas como um desencadeador de processos biológicos que continuam a desenvolver-se uma vez terminada a fase aguda.
Um dos mecanismos envolvidos é a ativação de programas de expressão génica associados à plasticidade sináptica. A psilocibina induz a expressão de genes de resposta imediata e de outros genes envolvidos no crescimento neuronal, na estabilização de sinapses e na reorganização de circuitos. Estas mudanças moleculares podem consolidar-se ao longo do tempo através da síntese de novas proteínas e da modificação estrutural das conexões existentes.
Além disso, a formação de novas espinhas dendríticas e o reforço de determinadas sinapses não são processos efémeros. Uma vez estabelecidas, estas modificações podem integrar-se de forma relativamente estável nas redes neuronais, especialmente se forem acompanhadas de mudanças na experiência, no comportamento ou no ambiente do indivíduo.
A nível funcional, a psilocibina está também associada a uma reorganização transitória das dinâmicas de conectividade cerebral. Durante este período, o cérebro pode explorar configurações menos rígidas e mais flexíveis. Em alguns casos, certas destas configurações persistem após a experiência, dando origem a padrões de processamento mais adaptativos.
Estes dados sugerem que a duração dos efeitos não depende da presença contínua da substância, mas da capacidade da psilocibina para iniciar uma cascata de mudanças moleculares, estruturais e funcionais que, sob determinadas condições, podem consolidar-se a médio e longo prazo.
Psilocibina e mudanças estruturais em pré-clínica
Os estudos pré-clínicos têm sido fundamentais para caracterizar como a psilocibina induz mudanças plásticas ao nível celular e estrutural. Em culturas celulares, exposições breves à psilocibina ou a compostos análogos produzem aumentos significativos na complexidade dendrítica e na densidade sináptica num prazo de 24 a 72 horas. É particularmente relevante que estímulos de curta duração possam gerar efeitos comparáveis aos observados após tratamentos prolongados.
Em modelos animais, uma única administração está associada a um aumento da densidade de espinhas dendríticas em regiões chave como o córtex pré-frontal medial e o hipocampo. Estas mudanças podem persistir durante várias semanas, e mesmo mais de um mês. Além disso, em modelos de stress crónico, a psilocibina reverte a atrofia dendrítica induzida pelo stress e está associada a melhorias em indicadores de comportamento adaptativo.
Estes resultados fornecem um suporte mecanístico sólido que justifica a exploração da psilocibina em estudos clínicos em humanos.
Psilocibina e modulação da Rede Neuronal por Defeito
Para compreender os efeitos psicológicos e terapêuticos da psilocibina, é imprescindível falar da Rede Neuronal por Defeito (DMN), um conjunto de regiões cerebrais altamente interconectadas que atuam como eixo organizador da experiência interna.
A DMN está especialmente ativa quando não realizamos uma tarefa concreta orientada para o exterior. Está associada à narrativa do eu, à memória autobiográfica, ao planeamento mental e à avaliação constante de si mesmo. Quando a sua atividade é excessiva ou rígida, relaciona-se com padrões de ruminação, autocrítica e pensamento repetitivo.
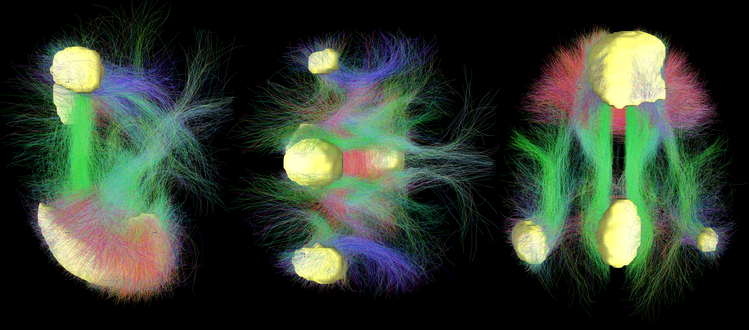
A psilocibina reduz de forma significativa a coerência e a dominância funcional desta rede. É como se o “gestor” do cérebro — o sistema que centraliza, prioriza e dá continuidade à experiência — se retirasse temporariamente. Esta diminuição do controlo hierárquico correlaciona-se com a redução da atividade sincronizada dentro da DMN e é o que muitas pessoas descrevem subjetivamente como uma dissolução do ego.
Quando este controlo se relaxa, aumenta a conectividade global entre redes cerebrais. Regiões que normalmente operam de forma mais segregada começam a trocar informação de forma mais direta. Este padrão de conectividade menos restritivo tem sido associado a fenómenos como a sinestesia, os reenquadramentos cognitivos profundos e o surgimento de perspetivas não habituais.
Este aumento de conectividade global traduz-se no que a neurociência descreve como um incremento da entropia cerebral: o cérebro opera num espaço de estados mais amplo, com padrões de ativação menos previsíveis e mais variáveis. Longe de ser um sinal de desorganização patológica, esta entropia elevada reflete um cérebro temporariamente libertado das suas rotinas percetivas e cognitivas mais rígidas — mais semelhante, em termos de dinâmica de rede, ao cérebro de uma criança a explorar o mundo do que ao de um adulto a resolver o que já conhece.
Do ponto de vista da neuroplasticidade, um cérebro menos hierárquico e menos constrangido por modelos internos dominantes é um cérebro mais maleável. Esta janela de flexibilidade é fundamental para compreender por que razão certas experiências induzidas pela psilocibina podem facilitar mudanças psicológicas duradouras.
Evidência da psilocibina em ensaios clínicos com humanos
Antes de abordar os estudos concretos, convém enquadrar o estado atual do campo. A investigação clínica com psilocibina avançou consideravelmente na última década, mas continua a operar com amostras relativamente pequenas, protocolos heterogéneos e uma limitação estrutural difícil de resolver: o verdadeiro duplo cego é praticamente impossível quando os participantes podem perceber claramente se receberam a substância ativa. Isto não invalida os resultados — a consistência dos efeitos através de diferentes grupos, instituições e metodologias é em si mesma um sinal sólido — mas exige que se leiam os resultados com a precisão que merece qualquer ciência em construção.
Depressão resistente ao tratamento
Os ensaios mais influentes provêm do grupo de Robin Carhart-Harris, iniciados no Imperial College de Londres e posteriormente continuados na Universidade da Califórnia em São Francisco. Os seus estudos com doentes que não tinham respondido a múltiplas linhas de tratamento farmacológico convencional documentaram reduções significativas na sintomatologia depressiva após uma ou duas sessões de psilocibina integradas num protocolo de apoio psicoterapêutico.
Em neuroimagem funcional, estes trabalhos revelaram uma redução persistente da atividade da DMN semanas após a intervenção, correlacionada com a melhoria clínica.
Depressão moderada-grave: o ensaio comparativo com escitalopram
O mesmo grupo liderou posteriormente um ensaio com uma população diferente: doentes com depressão moderada-grave sem critério de resistência ao tratamento. O ensaio publicado no The New England Journal of Medicine em 2021 comparou a psilocibina com o antidepressivo escitalopram e mostrou resultados comparáveis na escala de sintomas primária — embora o endpoint primário não tenha atingido significância estatística, em parte pelo tamanho amostral — e resultados superiores para o grupo de psilocibina em várias medidas secundárias de bem-estar emocional. O escitalopram apresentou uma resposta mais rápida nas primeiras semanas, o que sugere que ambas as intervenções têm perfis temporais distintos e potencialmente complementares.
Ansiedade e depressão associadas a doença terminal
O grupo de Roland Griffiths na Johns Hopkins University produziu alguns dos ensaios mais cuidadosamente desenhados do campo. Num estudo controlado com aleatorização com doentes oncológicos com diagnóstico potencialmente fatal, uma única dose alta de psilocibina produziu reduções clinicamente significativas tanto na ansiedade como na depressão, que se mantiveram estáveis em seguimentos realizados aos seis meses. Em aproximadamente 80% dos participantes os efeitos benéficos continuavam a ser percetíveis em avaliações a longo prazo, um dado de persistência incomum em psicofarmacologia. Os autores observaram ainda que a intensidade da experiência mística durante a sessão se correlacionava com a magnitude do benefício terapêutico posterior, o que alimentou o debate sobre a relevância da componente experiencial no mecanismo de ação.
Perturbações por uso de substâncias
A investigação produziu resultados preliminares notáveis. O grupo de Johns Hopkins publicou um estudo piloto sobre dependência do tabaco em que duas ou três sessões de psilocibina combinadas com terapia cognitivo-comportamental produziram taxas de abstinência aos seis meses superiores a 60%, muito acima dos referenciais históricos dos tratamentos de primeira linha. Para a perturbação por uso de álcool, um ensaio controlado da Universidade de Nova Iorque reportou reduções sustentadas e significativas no consumo face a placebo ativo. Ambas as linhas de investigação são ainda incipientes em termos de tamanho amostral e requerem replicação, mas a magnitude dos efeitos observados justifica o interesse crescente.
Técnicas de neuroimagem funcional e estrutural mostram alterações na conectividade entre regiões pré-frontais e subcorticais semanas após uma única administração. Estas modificações afetam circuitos envolvidos na regulação emocional, na tomada de decisões e na resposta ao stress. Do mesmo modo, foram descritas variações na espessura cortical em áreas relacionadas com o controlo cognitivo e a integração emocional.
A nível psicológico, foram documentadas melhorias sustentadas na flexibilidade cognitiva, na empatia emocional e no bem-estar subjetivo. Estas mudanças não são acompanhadas de deterioração das funções cognitivas básicas, como a memória de trabalho ou a atenção, o que reforça o perfil de segurança observado nos estudos controlados.
Em contextos terapêuticos controlados, especialmente na depressão resistente ou na ansiedade, os efeitos benéficos podem manter-se durante meses e mesmo até um ano após uma ou duas sessões, sempre integradas num quadro de acompanhamento psicológico.
| Condição | Instituição | Resultado Chave |
|---|---|---|
| Depressão Resistente | Imperial College / UCSF | Melhoria rápida; superior a fármacos comuns no bem-estar a longo prazo. |
| Ansiedade Terminal | Johns Hopkins University | 80% de sucesso com melhoria clínica sustentada após 6 meses. |
| Dependência do Tabaco | Johns Hopkins University | 60% de abstinência aos 6 meses (duplica a eficácia convencional). |
| Uso de Álcool | NYU | Descida significativa nos dias de consumo excessivo face a placebo. |
Riscos de uma neuroplasticidade não adaptativa
A psilocibina induz mudanças cerebrais reais. Isso significa que os riscos também são reais. O exemplo mais claro é o HPPD (perturbação percetiva persistente pós-alucinogénio): distorções visuais que reaparecem semanas ou meses após a experiência. É a demonstração mais direta de que mais plasticidade não equivale automaticamente a “melhor” plasticidade: em certos indivíduos, os circuitos de processamento consolidam-se de formas indesejadas.
Para que esta janela de maleabilidade seja terapêutica e não desestabilizadora, o rastreio médico prévio e o contexto são inegociáveis. Sem um quadro de segurança e uma integração posterior, o cérebro pode reforçar padrões pouco adaptativos em vez de os quebrar. Estes são os critérios de exclusão médica e farmacológica sistemáticos na investigação clínica:
Critérios de exclusão e precauções médicas
- Saúde Mental: Antecedentes pessoais ou familiares de psicose, esquizofrenia ou perturbação bipolar tipo I.
- Interações Farmacológicas: Uso de Lítio (risco de convulsões), IMAOs ou antidepressivos serotoninérgicos.
- Condições Físicas: Cardiopatias não controladas, epilepsia ativa ou gravidez.
- Segurança Psicológica: Não é recomendado o uso sem acompanhamento profissional em casos de trauma complexo não processado.
A precisão no rastreio é o que separa uma experiência transformadora de um risco desnecessário. Para uma análise técnica detalhada de cada interação e protocolo de segurança, pode consultar o nosso guia completo de riscos e contraindicações da psilocibina.
A integração como eixo da plasticidade pós-psicodélica
Após a experiência psicodélica, o cérebro permanece durante dias ou semanas num estado de plasticidade elevada. Voltando à nossa metáfora inicial: a neve fresca cobre os sulcos antigos. Mas a neve não decide sozinha que novos caminhos se formam. Se não houver mudanças no ambiente, nos hábitos ou no acompanhamento terapêutico, o peso da repetição voltará a abrir exatamente os mesmos sulcos de antes. E isso tem consequências em ambas as direções.
Por isso, a integração é fundamental. A evidência indica que a psilocibina não é uma panaceia, mas um modulador: um sinal que o cérebro interpreta para construir — ou eliminar — conexões reais ao nível molecular, estrutural e funcional.
Este processo pode persistir meses após uma única sessão, oferecendo implicações terapêuticas genuínas na depressão, na ansiedade e nas dependências. No entanto, os efeitos dependem do contexto e o campo continua a ser uma ciência em construção. Num território onde a biologia e a experiência subjetiva se sobrepõem, a precisão não é um detalhe: é o ponto de partida.
Fontes e referências
Mecanismo molecular e neuroplasticidade
- Olson, D.E. (2021) — Proposta do conceito de psicoplastogénios e o seu potencial terapêutico. Journal of Experimental Neuroscience.
- Ly, C. et al. (2018) — Evidência de que os psicodélicos promovem plasticidade estrutural e funcional em neurónios corticais. Cell Reports.
- Vargas, M.V. et al. (2023) — Demonstração de que os recetores 5-HT2A intracelulares medeiam os efeitos neuroplásticos. Science.
Períodos críticos
- Nardou, R. et al. (2023) — Os psicodélicos reabrem o período crítico de aprendizagem de recompensa social. Nature.
Rede Neuronal por Defeito e entropia cerebral
- Carhart-Harris, R.L. et al. (2012) — Correlatos neuronais do estado psicodélico medidos com fMRI e redução da DMN. PNAS.
- Carhart-Harris, R.L. et al. (2014) — A teoria do cérebro entrópico: incremento da entropia como substrato da experiência. Frontiers in Human Neuroscience.
Evidência clínica — Depressão
- Carhart-Harris, R. et al. (2021) — Ensaio comparativo entre psilocibina e escitalopram na depressão moderada-grave. New England Journal of Medicine.
- Davis, A.K. et al. (2021) — Efeitos da terapia assistida com psilocibina na perturbação depressiva major. JAMA Psychiatry.
Evidência clínica — Ansiedade e doença terminal
- Griffiths, R.R. et al. (2016) — Redução substancial e sustentada de depressão e ansiedade em doentes oncológicos. Journal of Psychopharmacology.
- Ross, S. et al. (2016) — Redução rápida e sustentada de ansiedade e depressão no cancro avançado. Journal of Psychopharmacology.
Evidência clínica — Dependências
- Johnson, M.W. et al. (2014) — Psilocibina como apoio à cessação tabágica: estudo piloto. Journal of Psychopharmacology.
- Bogenschutz, M.P. et al. (2015) — Estudo de conceito sobre psilocibina na dependência do álcool. Journal of Psychopharmacology.
- Bogenschutz, M.P. et al. (2022) — Ensaio controlado sobre psilocibina na perturbação por uso de álcool. JAMA Psychiatry.
Artigos relacionados
-
Aplicações terapêuticas da psilocibina
Publicado em: 2025-07-31 14:25:24 -
Psilocibina: o que é, como atua e quais efeitos provoca
Publicado em: 2025-07-24 12:21:12 -
Mitos sobre a psilocibina que a ciência desmente
Publicado em: 2025-12-10 20:34:04























