Come la psilocibina può rimodellare il cervello adulto
- Cos'è la neuroplasticità e come funziona nel cervello adulto
- Fondamenti biologici e farmacologia della psilocibina
- Come la psilocibina trasforma il cervello adulto
- La psilocibina come psicoplastogeno: i meccanismi del cambiamento neuronale
- Perché la psilocibina agisce diversamente dalla serotonina
- Il BDNF e il suo ruolo nella plasticità indotta dalla psilocibina
- Perché gli effetti neuroplastici della psilocibina sono duraturi?
- Psilocibina e cambiamenti strutturali in studi preclinici
- Psilocibina e modulazione della Rete in Modalità Default
- Evidenze della psilocibina negli studi clinici sull'essere umano
- Depressione resistente al trattamento
- Depressione moderata-grave: lo studio comparativo con escitalopram
- Ansia e depressione associate a malattia terminale
- Disturbi da uso di sostanze
- Rischi di una neuroplasticità non adattiva
- L'integrazione come asse della plasticità post-psichedelica
- Fonti e riferimenti
- Meccanismo molecolare e neuroplasticità
- Periodi critici
- Rete in Modalità Default ed entropia cerebrale
- Evidenza clinica — Depressione
- Evidenza clinica — Ansia e malattia terminale
- Evidenza clinica — Dipendenze
Immagina il cervello come una montagna coperta di neve. Ogni pensiero ricorrente, ogni reazione automatica e ogni abitudine mentale è una slitta che scende ancora e ancora lungo lo stesso percorso. Con il tempo, quei sentieri diventano solchi profondi: efficienti e rapidi… ma sempre più difficili da abbandonare.
Questa immagine riassume bene ciò che accade in molti stati di rigidità psicologica. Lo stress cronico, l'ansia, la depressione o persino la routine quotidiana rinforzano schemi di pensiero ripetitivi. Non perché siano i migliori, ma perché sono i più battuti. Il cervello, come qualsiasi sistema biologico, tende a ottimizzare ciò che già conosce.
Per decenni si è dato per scontato che questa rigidità fosse, in larga misura, irreversibile nell'età adulta. Oggi sappiamo che non deve essere necessariamente così. Il cervello conserva una notevole capacità di cambiare, adattarsi e riorganizzarsi. A questa proprietà la chiamiamo neuroplasticità.
Negli ultimi anni, i funghi psicodelici (in particolare le specie del genere Psilocybe) sono ricomparsi nella ricerca scientifica come possibili catalizzatori di questa plasticità. Non solo per gli stati alterati di coscienza che producono, ma per qualcosa di più profondo e duraturo: la loro capacità di indurre cambiamenti strutturali e funzionali nel cervello che persistono ben oltre l'esperienza acuta.
Questo articolo esplora cosa significa realmente la neuroplasticità, come agisce la psilocibina sul cervello, cosa dice l'evidenza scientifica attuale e quali sono le sue implicazioni, limiti e rischi.
Cos'è la neuroplasticità e come funziona nel cervello adulto
La neuroplasticità è la capacità del sistema nervoso di riorganizzarsi a diversi livelli: molecolare, cellulare, strutturale e funzionale. Implica sia la creazione di nuove connessioni sia l'eliminazione di quelle che cessano di essere adattive — un processo di ‘pulizia’ naturale chiamato potatura sinaptica che consente al cervello non solo di crescere, ma di raffinarsi.
Per molto tempo si è pensato che questa capacità diminuisse drasticamente dopo l'infanzia, un'idea ereditata dai primi modelli dello sviluppo cerebrale. Oggi sappiamo che il cervello adulto rimane plastico, sebbene tale plasticità tenda a essere più “regolata” e meno disponibile in forma spontanea.
Per comprendere come gli psichedelici interagiscono con questi processi, dobbiamo distinguere diversi tipi di plasticità rilevanti:
- Plasticità strutturale: comprende la crescita dei dendriti, la formazione di nuove sinapsi e i cambiamenti nella densità delle spine dendritiche. È il substrato fisico dell'apprendimento: ogni volta che il cervello consolida qualcosa di nuovo, lo fa in parte modificando l'architettura dei suoi neuroni, aggiungendo o rafforzando i punti di contatto tra loro.
- Plasticità funzionale: la riorganizzazione delle reti cerebrali e dei pattern di comunicazione tra le diverse regioni. Non implica necessariamente cambiamenti strutturali visibili, ma cambiamenti in quali circuiti si attivano insieme, con quale intensità e con quale sincronia. È la plasticità che permette, ad esempio, che una regione danneggiata venga parzialmente compensata da un'altra, o che un'abitudine mentale cronica si indebolisca progressivamente quando smettiamo di alimentarla.
- Meta-plasticità: un concetto chiave che opera a un livello superiore ai precedenti: non cambiano solo le connessioni, ma anche la soglia affinché si verifichino cambiamenti futuri. Vale a dire, il cervello stesso modula quanto gli sia facile o difficile rimodellarsi in risposta all'esperienza. Un cervello che ha attraversato periodi di stress elevato e prolungato, ad esempio, può diventare meno ricettivo ai cambiamenti adattivi; uno in uno stato di plasticità elevata, al contrario, risponde più facilmente a nuovi apprendimenti ed esperienze.
- Riapertura dei periodi critici: Questo è uno dei concetti più all'avanguardia — e anche dei più preliminari — della neuroscienze attuale. Si riferisce a finestre temporali di estrema sensibilità all'ambiente che, biologicamente, tendono a chiudersi dopo l'infanzia o l'adolescenza. Le evidenze recenti suggeriscono che gli psichedelici possano riaprire queste “porte”, riportando il cervello a uno stato di malleabilità sociale ed emotiva in cui è possibile riscrivere apprendimenti profondi — come traumi o pattern di attaccamento — che fino a oggi si consideravano immutabili. È importante sottolineare, tuttavia, che questa linea di ricerca non dispone ancora di replicazioni robuste negli esseri umani e deve essere interpretata con cautela.
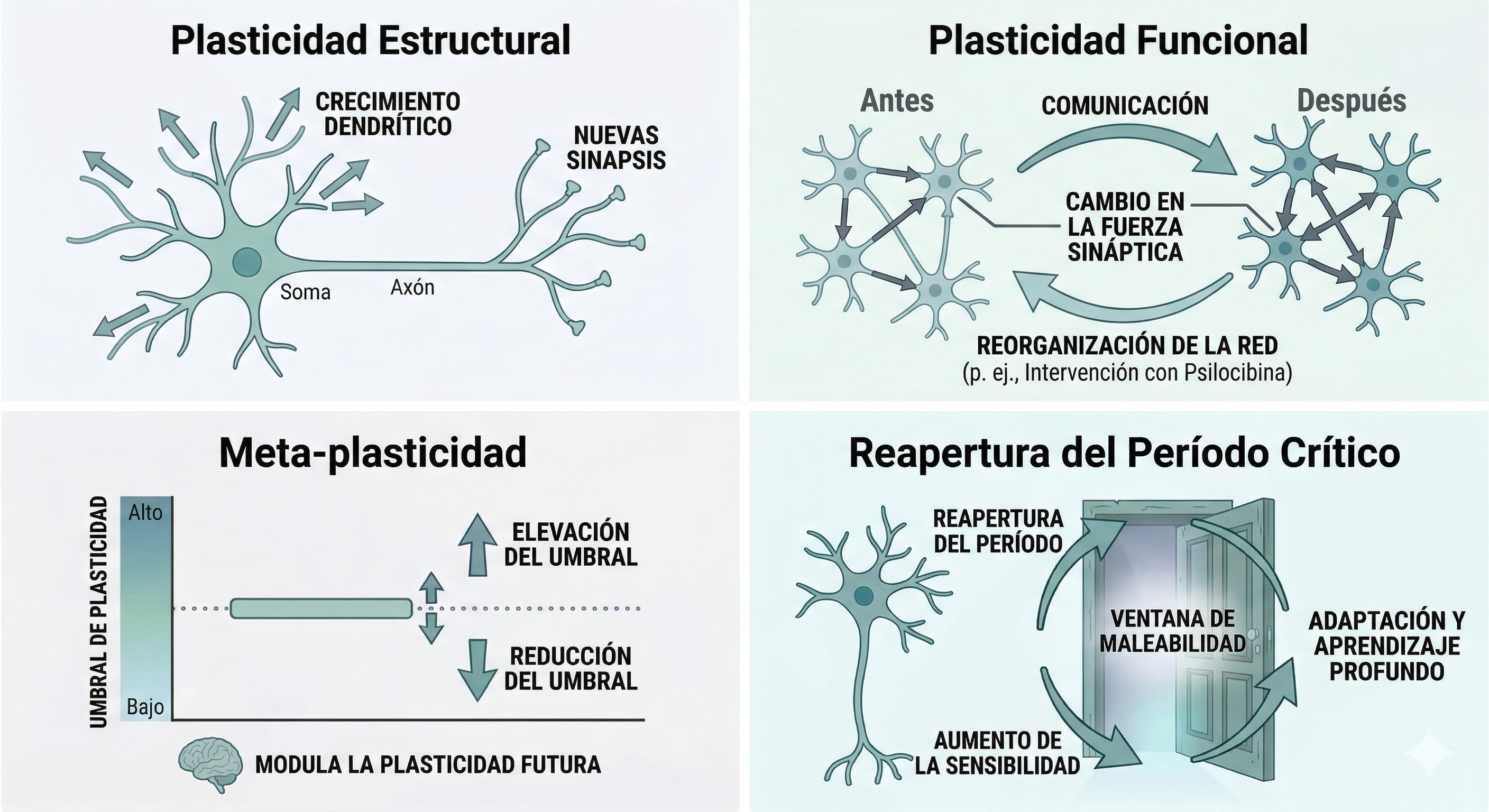
Questi diversi tipi di plasticità forniscono il quadro concettuale per comprendere come sostanze come la psilocibina possano indurre cambiamenti cerebrali significativi anche nell'adulto.
Fondamenti biologici e farmacologia della psilocibina
I funghi psicodelici, specialmente le specie del genere Psilocybe, producono naturalmente psilocibina. È importante sottolineare che la psilocibina è, a rigore, un profarmaco: una sostanza che di per sé non è significativamente attiva, ma che l'organismo metabolizza (principalmente nel fegato) per convertirla in psilocina, la molecola che attraversa realmente la barriera ematoencefalica e genera gli effetti nel cervello.
A differenza di molti altri metaboliti secondari prodotti da funghi e piante, la psilocibina mostra una notevole affinità per il sistema serotoninergico umano, in particolare per certi recettori coinvolti in processi come la percezione, la cognizione e la regolazione emotiva.
Sebbene siano correlati, la ricerca attuale suggerisce che i secondi non possono essere spiegati unicamente dai primi. Questa distinzione è cruciale, poiché suggerisce che la vera potenza terapeutica della psilocibina potrebbe risiedere non solo nell'intensità dell'esperienza soggettiva, ma nella «finestra di opportunità» biologica che si apre a livello cellulare. Comprendere la sostanza come un modulatore strutturale ci consente di separare il fenomeno dell'allucinazione dal processo di riparazione e ricablaggio neuronale che analizzeremo di seguito.
Un terzo elemento, tanto determinante quanto la dose o il meccanismo molecolare, è ciò che la ricerca definisce set and setting: il set si riferisce allo stato interno del partecipante — la sua disposizione emotiva, le sue aspettative e la sua storia personale —; il setting all'ambiente fisico, sociale e relazionale in cui si svolge l'esperienza. Negli studi clinici, entrambi vengono attentamente controllati attraverso la preparazione preliminare, l'accompagnamento professionale e le sessioni di integrazione successive. Questa variabile non è accessoria: gli studi mostrano che lo stesso composto, somministrato in contesti diversi, può produrre esperienze radicalmente differenti, e che la qualità del set and setting predice in parte la portata e la direzione del cambiamento terapeutico.
Come la psilocibina trasforma il cervello adulto
La psilocibina come psicoplastogeno: i meccanismi del cambiamento neuronale
Negli ultimi anni è emerso un termine chiave per descrivere sostanze come la psilocibina: i psicoplastogeni. Il concetto, proposto nel contesto della ricerca moderna da gruppi come quello di David E. Olson, si riferisce a composti capaci di promuovere in modo rapido e potente la neuroplasticità, al di là dei loro effetti soggettivi.
Prima di esaminare i meccanismi molecolari, vale la pena segnalare una distinzione che spesso viene omessa nella divulgazione su questo argomento: non esiste un unico “modo d'uso” della psilocibina, e i contesti di somministrazione producono profili biologici e terapeutici molto diversi. In ambito clinico e di ricerca si distinguono principalmente due approcci:
- La dose terapeutica — quella impiegata negli studi clinici moderni — prevede dosi medie o alte (generalmente tra 20 e 30 mg di psilocibina sintetica, o il suo equivalente in fungo essiccato) somministrate in sessioni singole o molto rare, sempre con accompagnamento professionale e preparazione preliminare. Produce stati alterati di coscienza della durata di quattro-sei ore ed è il modello su cui si accumula la maggior parte delle evidenze neurobiologiche e terapeutiche.
- Il microdosaggio, invece, consiste nell'assunzione periodica di dosi sub-percettive — solitamente tra 0,1 e 0,3 grammi di fungo essiccato — nell'arco di giorni o settimane, senza che si producano alterazioni percettive rilevanti. Sebbene la pratica abbia guadagnato popolarità ed esista un'ampia base di utenti che riferiscono benefici in termini di concentrazione, umore o creatività, le evidenze scientifiche sui suoi specifici effetti neuroplastici sono oggi considerevolmente più limitate e meno sistematiche. La grande maggioranza dei risultati descritti in questo articolo corrisponde al modello della dose terapeutica.
Perché la psilocibina agisce diversamente dalla serotonina
Tradizionalmente si pensava che fosse sufficiente attivare i recettori 5-HT2A situati sulla superficie del neurone per innescare gli effetti psicodelici. Tuttavia, ricerche recenti hanno rivelato una sfumatura neurobiologica cruciale: la localizzazione.
A differenza della serotonina endogena, che fatica ad attraversare la membrana cellulare a causa della sua polarità, la psilocina (e altri psichedelici) può attraversare questa barriera lipidica e accedere all'interno della cellula. Una volta dentro, si lega a una riserva di recettori 5-HT2A ubicati in organelli intracellulari, come l'apparato del Golgi.
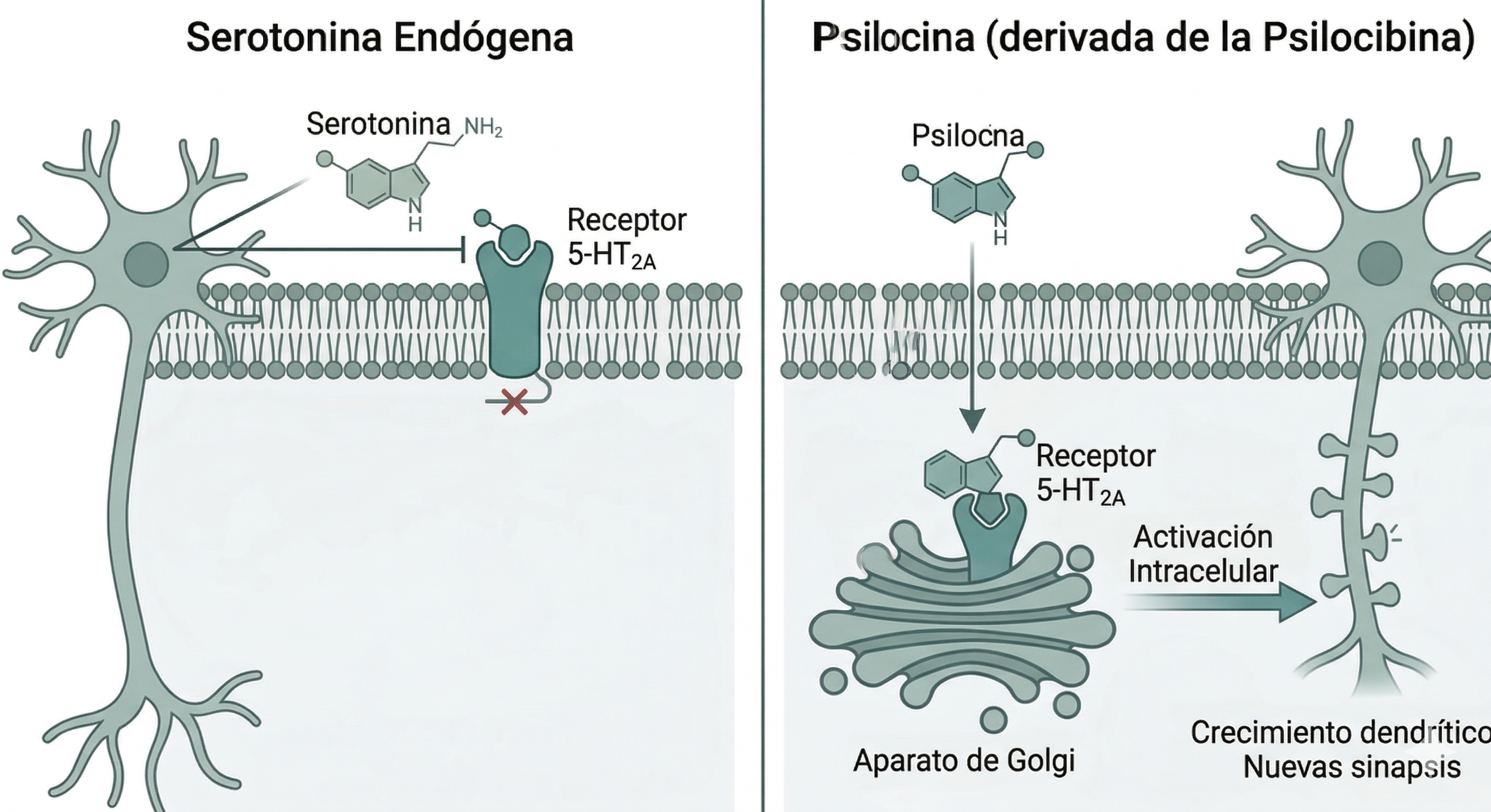
Le evidenze attuali suggeriscono che è precisamente questa attivazione intracellulare a innescare in modo consistente la crescita dei dendriti e la formazione di nuove spine. Questo spiegherebbe perché, pur avendo serotonina nel cervello costantemente, essa non provoca i profondi cambiamenti strutturali né gli stati di plasticità rapida che osserviamo con gli psichedelici.
Il BDNF e il suo ruolo nella plasticità indotta dalla psilocibina
Uno degli attori chiave in questo processo è il BDNF (Fattore Neurotrofico Derivato dal Cervello), una proteina fondamentale per la crescita, la sopravvivenza e la differenziazione neuronale. La psilocibina è associata a un aumento nell'espressione e nel rilascio di BDNF, il che facilita l'attivazione del suo recettore TrkB e contribuisce al consolidamento di nuove connessioni sinaptiche.
Alcuni studi suggeriscono che certi effetti plastici possano verificarsi in modo parzialmente indipendente dal recettore 5-HT2A, il che indica meccanismi più complessi di quanto inizialmente ipotizzato.
Questi cambiamenti molecolari si traducono potenzialmente in un cervello più flessibile e capace di riorganizzare le proprie reti, sostenendo miglioramenti nell'apprendimento, nell'adattamento e nella regolazione emotiva.
Questo effetto è inoltre amplificato da un meccanismo che esamineremo più avanti: la riduzione simultanea dell'attività ruminativa del DMN, la cui iperattività cronica agisce come soppressore attivo dell'espressione del BDNF attraverso l'asse dello stress.
Perché gli effetti neuroplastici della psilocibina sono duraturi?
Sebbene la psilocibina venga eliminata dall'organismo nell'arco di poche ore, i cambiamenti che induce possono persistere per settimane o anche mesi. Questo apparente paradosso si spiega perché la sostanza non agisce unicamente come stimolo transitorio, ma come innesco di processi biologici che continuano a svilupparsi una volta terminata la fase acuta.
Uno dei meccanismi coinvolti è l'attivazione di programmi di espressione genica associati alla plasticità sinaptica. La psilocibina induce l'espressione di geni di risposta immediata e di altri geni coinvolti nella crescita neuronale, nella stabilizzazione delle sinapsi e nella riorganizzazione dei circuiti. Questi cambiamenti molecolari possono consolidarsi nel tempo attraverso la sintesi di nuove proteine e la modificazione strutturale delle connessioni esistenti.
Inoltre, la formazione di nuove spine dendritiche e il rafforzamento di determinate sinapsi non sono processi effimeri. Una volta stabilite, queste modificazioni possono integrarsi in modo relativamente stabile nelle reti neuronali, specialmente se accompagnate da cambiamenti nell'esperienza, nel comportamento o nell'ambiente dell'individuo.
A livello funzionale, la psilocibina è anche associata a una riorganizzazione transitoria delle dinamiche di connettività cerebrale. Durante questo periodo, il cervello può esplorare configurazioni meno rigide e più flessibili. In alcuni casi, alcune di queste configurazioni persistono dopo l'esperienza, dando luogo a schemi di elaborazione più adattivi.
Questi dati suggeriscono che la durata degli effetti non dipende dalla presenza continua della sostanza, ma dalla capacità della psilocibina di avviare una cascata di cambiamenti molecolari, strutturali e funzionali che, in determinate condizioni, possono consolidarsi nel medio e lungo termine.
Psilocibina e cambiamenti strutturali in studi preclinici
Gli studi preclinici sono stati fondamentali per caratterizzare come la psilocibina induca cambiamenti plastici a livello cellulare e strutturale. In colture cellulari, brevi esposizioni alla psilocibina o a composti analoghi producono aumenti significativi della complessità dendritica e della densità sinaptica nell'arco di 24-72 ore. È particolarmente rilevante che stimoli di breve durata possano generare effetti paragonabili a quelli osservati dopo trattamenti prolungati.
In modelli animali, una singola somministrazione è associata a un aumento della densità delle spine dendritiche in regioni chiave come la corteccia prefrontale mediale e l'ippocampo. Questi cambiamenti possono persistere per diverse settimane, e anche per più di un mese. Inoltre, in modelli di stress cronico, la psilocibina inverte l'atrofia dendritica indotta dallo stress ed è associata a miglioramenti negli indicatori di comportamento adattivo.
Questi risultati forniscono un solido supporto meccanicistico che giustifica l'esplorazione della psilocibina in studi clinici nell'essere umano.
Psilocibina e modulazione della Rete in Modalità Default
Per comprendere gli effetti psicologici e terapeutici della psilocibina, è indispensabile parlare della Rete in Modalità Default (DMN), un insieme di regioni cerebrali altamente interconnesse che agiscono come asse organizzatore dell'esperienza interna.
Il DMN è particolarmente attivo quando non stiamo svolgendo un compito concreto orientato all'esterno. È associato alla narrativa del sé, alla memoria autobiografica, alla pianificazione mentale e alla costante valutazione di se stessi. Quando la sua attività è eccessiva o rigida, è correlato a schemi di ruminazione, autocritica e pensiero ripetitivo.
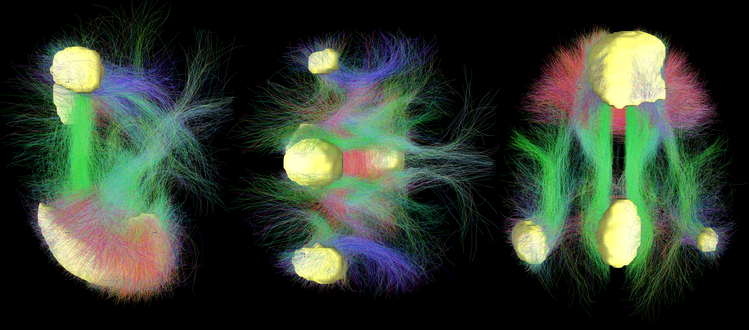
La psilocibina riduce significativamente la coerenza e la dominanza funzionale di questa rete. È come se il “direttore” del cervello — il sistema che centralizza, prioritizza e dà continuità all'esperienza — si ritirasse temporaneamente. Questo calo del controllo gerarchico si correla con la diminuzione dell'attività sincronizzata all'interno del DMN ed è ciò che molte persone descrivono soggettivamente come una dissoluzione dell'ego.
Quando questo controllo si allenta, aumenta la connettività globale tra le reti cerebrali. Regioni che normalmente operano in modo più segregato iniziano a scambiare informazioni in maniera più diretta. Questo schema di connettività meno restrittivo è stato associato a fenomeni come la sinestesia, i profondi riformulazioni cognitive e l'emergere di prospettive insolite.
Questo aumento di connettività globale si traduce in ciò che la neuroscienze descrive come un incremento dell'entropia cerebrale: il cervello opera in uno spazio di stati più ampio, con schemi di attivazione meno prevedibili e più variabili. Lungi dall'essere un segno di disorganizzazione patologica, questa elevata entropia riflette un cervello temporaneamente liberato dalle sue routine percettive e cognitive più rigide — più simile, in termini di dinamica di rete, al cervello di un bambino che esplora il mondo che a quello di un adulto che risolve il familiare.
Dal punto di vista della neuroplasticità, un cervello meno gerarchico e meno vincolato da modelli interni dominanti è un cervello più malleabile. Questa finestra di flessibilità è fondamentale per comprendere perché certe esperienze indotte dalla psilocibina possano facilitare cambiamenti psicologici duraturi.
Evidenze della psilocibina negli studi clinici sull'essere umano
Prima di esaminare gli studi concreti, è opportuno inquadrare lo stato attuale del settore. La ricerca clinica con psilocibina ha compiuto notevoli progressi nell'ultimo decennio, ma continua a operare con campioni relativamente piccoli, protocolli eterogenei e un limite strutturale difficile da risolvere: il vero doppio cieco è praticamente impossibile quando i partecipanti possono chiaramente percepire se hanno ricevuto la sostanza attiva. Questo non invalida i risultati — la coerenza degli effetti attraverso diversi gruppi, istituzioni e metodologie è di per sé un segnale solido — ma richiede di leggere i risultati con la precisione che merita qualsiasi scienza in costruzione.
Depressione resistente al trattamento
Gli studi più influenti provengono dal gruppo di Robin Carhart-Harris, avviati all'Imperial College di Londra e successivamente proseguiti all'Università della California di San Francisco. Le loro ricerche con pazienti che non avevano risposto a molteplici linee di trattamento farmacologico convenzionale hanno documentato riduzioni significative della sintomatologia depressiva dopo una o due sessioni di psilocibina integrate in un protocollo di supporto psicoterapeutico.
Nella neuroimmagine funzionale, questi lavori hanno rivelato una riduzione persistente dell'attività del DMN settimane dopo l'intervento, correlata con il miglioramento clinico.
Depressione moderata-grave: lo studio comparativo con escitalopram
Lo stesso gruppo ha successivamente condotto uno studio con una popolazione diversa: pazienti con depressione moderata-grave senza criterio di resistenza al trattamento. Lo studio pubblicato sul New England Journal of Medicine nel 2021 ha confrontato la psilocibina con l'antidepressivo escitalopram e ha mostrato risultati comparabili sulla scala dei sintomi primaria — sebbene l'endpoint primario non abbia raggiunto la significatività statistica, in parte a causa della dimensione del campione — e risultati superiori per il gruppo psilocibina su diverse misure secondarie di benessere emotivo. L'escitalopram ha mostrato una risposta più rapida nelle prime settimane, il che suggerisce che i due interventi abbiano profili temporali distinti e potenzialmente complementari.
Ansia e depressione associate a malattia terminale
Il gruppo di Roland Griffiths alla Johns Hopkins University ha prodotto alcuni degli studi più accuratamente progettati del settore. In uno studio controllato randomizzato con pazienti oncologici con diagnosi potenzialmente letale, una singola dose elevata di psilocibina ha prodotto riduzioni clinicamente significative sia dell'ansia che della depressione, rimaste stabili nei follow-up effettuati a sei mesi. In circa l'80% dei partecipanti gli effetti benefici erano ancora percepibili nelle valutazioni a lungo termine, un dato di persistenza insolito in psicofarmacologia. Gli autori hanno inoltre osservato che l'intensità dell'esperienza mistica durante la sessione si correlava con la portata del successivo beneficio terapeutico, alimentando il dibattito sulla rilevanza della componente esperienziale nel meccanismo d'azione.
Disturbi da uso di sostanze
La ricerca ha prodotto risultati preliminari notevoli. Il gruppo di Johns Hopkins ha pubblicato uno studio pilota sulla dipendenza da tabacco in cui due o tre sessioni di psilocibina combinate con terapia cognitivo-comportamentale hanno prodotto tassi di astinenza a sei mesi superiori al 60%, ben al di sopra dei valori di riferimento storici dei trattamenti di prima linea. Per il disturbo da uso di alcol, uno studio controllato della New York University ha riportato riduzioni sostenute e significative del consumo rispetto al placebo attivo. Entrambe le linee di ricerca sono ancora agli inizi in termini di dimensione del campione e richiedono replicazione, ma l'entità degli effetti osservati giustifica il crescente interesse.
Tecniche di neuroimmagine funzionale e strutturale mostrano cambiamenti nella connettività tra regioni prefrontali e sottocorticali settimane dopo una singola somministrazione. Queste modificazioni interessano circuiti coinvolti nella regolazione emotiva, nel processo decisionale e nella risposta allo stress. Sono state inoltre descritte variazioni nello spessore corticale in aree correlate al controllo cognitivo e all'integrazione emotiva.
A livello psicologico, sono stati documentati miglioramenti sostenuti nella flessibilità cognitiva, nell'empatia emotiva e nel benessere soggettivo. Questi cambiamenti non sono accompagnati da un deterioramento delle funzioni cognitive di base, come la memoria di lavoro o l'attenzione, il che rafforza il profilo di sicurezza osservato negli studi controllati.
In contesti terapeutici controllati, specialmente nella depressione resistente o nell'ansia, gli effetti benefici possono mantenersi per mesi e anche fino a un anno dopo una o due sessioni, sempre integrate in un quadro di accompagnamento psicologico.
| Condizione | Istituzione | Risultato Chiave |
|---|---|---|
| Depressione Resistente | Imperial College / UCSF | Miglioramento rapido; superiore ai farmaci comuni nel benessere a lungo termine. |
| Ansia Terminale | Johns Hopkins University | 80% di successo con miglioramento clinico sostenuto dopo 6 mesi. |
| Dipendenza da Tabacco | Johns Hopkins University | 60% di astinenza a 6 mesi (doppia l'efficacia convenzionale). |
| Uso di Alcol | NYU | Diminuzione significativa dei giorni di consumo eccessivo rispetto al placebo. |
Rischi di una neuroplasticità non adattiva
La psilocibina induce cambiamenti cerebrali reali. Ciò significa che i rischi sono anch'essi reali. L'esempio più chiaro è l'HPPD (disturbo percettivo persistente post-allucinogeno): distorsioni visive che ricompaiono settimane o mesi dopo l'esperienza. È la dimostrazione più diretta che una maggiore plasticità non equivale automaticamente a una plasticità “migliore”: in certi individui, i circuiti di elaborazione si consolidano in modi indesiderati.
Affinché questa finestra di malleabilità sia terapeutica e non destabilizzante, lo screening medico preliminare e il contesto sono imprescindibili. Senza un quadro di sicurezza e un'integrazione successiva, il cervello può rinforzare schemi poco adattivi invece di romperli. Questi sono i criteri di esclusione medica e farmacologica sistematici nella ricerca clinica:
Criteri di esclusione e precauzioni mediche
- Salute Mentale: Anamnesi personale o familiare di psicosi, schizofrenia o disturbo bipolare di tipo I.
- Interazioni Farmacologiche: Uso di Litio (rischio di convulsioni), IMAO o antidepressivi serotoninergici.
- Condizioni Fisiche: Cardiopatie non controllate, epilessia attiva o gravidanza.
- Sicurezza Psicologica: L'uso senza accompagnamento professionale non è raccomandato nei casi di trauma complesso non elaborato.
La precisione nello screening è ciò che separa un'esperienza trasformativa da un rischio inutile. Per un'analisi tecnica dettagliata di ogni interazione e protocollo di sicurezza, è possibile consultare la nostra guida completa ai rischi e alle controindicazioni della psilocibina.
L'integrazione come asse della plasticità post-psichedelica
Dopo l'esperienza psichedelica, il cervello rimane per giorni o settimane in uno stato di plasticità elevata. Tornando alla nostra metafora iniziale: la neve fresca copre i solchi antichi. Ma la neve non decide da sola quali nuovi percorsi si formano. Se non ci sono cambiamenti nell'ambiente, nelle abitudini o nell'accompagnamento terapeutico, il peso della ripetizione riaprirà esattamente gli stessi solchi di prima. E questo ha conseguenze in entrambe le direzioni.
Per questo motivo, l'integrazione è fondamentale. Le evidenze indicano che la psilocibina non è una panacea, ma un modulatore: un segnale che il cervello interpreta per costruire — o eliminare — connessioni reali a livello molecolare, strutturale e funzionale.
Questo processo può persistere per mesi dopo una singola sessione, offrendo genuine implicazioni terapeutiche nella depressione, nell'ansia e nelle dipendenze. Tuttavia, gli effetti dipendono dal contesto e il settore rimane una scienza in costruzione. In un territorio in cui biologia ed esperienza soggettiva si sovrappongono, la precisione non è un dettaglio: è il punto di partenza.
Fonti e riferimenti
Meccanismo molecolare e neuroplasticità
- Olson, D.E. (2021) — Proposta del concetto di psicoplastogeni e il loro potenziale terapeutico. Journal of Experimental Neuroscience.
- Ly, C. et al. (2018) — Evidenza che gli psichedelici promuovono la plasticità strutturale e funzionale nei neuroni corticali. Cell Reports.
- Vargas, M.V. et al. (2023) — Dimostrazione che i recettori 5-HT2A intracellulari mediano gli effetti neuroplastici. Science.
Periodi critici
- Nardou, R. et al. (2023) — Gli psichedelici riaprono il periodo critico dell'apprendimento della ricompensa sociale. Nature.
Rete in Modalità Default ed entropia cerebrale
- Carhart-Harris, R.L. et al. (2012) — Correlati neurali dello stato psichedelico misurati con fMRI e riduzione del DMN. PNAS.
- Carhart-Harris, R.L. et al. (2014) — La teoria del cervello entropico: incremento dell'entropia come substrato dell'esperienza. Frontiers in Human Neuroscience.
Evidenza clinica — Depressione
- Carhart-Harris, R. et al. (2021) — Studio comparativo tra psilocibina ed escitalopram nella depressione moderata-grave. New England Journal of Medicine.
- Davis, A.K. et al. (2021) — Effetti della terapia assistita con psilocibina nel disturbo depressivo maggiore. JAMA Psychiatry.
Evidenza clinica — Ansia e malattia terminale
- Griffiths, R.R. et al. (2016) — Riduzione sostanziale e sostenuta di depressione e ansia in pazienti oncologici. Journal of Psychopharmacology.
- Ross, S. et al. (2016) — Riduzione rapida e sostenuta di ansia e depressione nel cancro avanzato. Journal of Psychopharmacology.
Evidenza clinica — Dipendenze
- Johnson, M.W. et al. (2014) — Psilocibina come supporto alla cessazione del tabagismo: studio pilota. Journal of Psychopharmacology.
- Bogenschutz, M.P. et al. (2015) — Studio di concetto sulla psilocibina nella dipendenza da alcol. Journal of Psychopharmacology.
- Bogenschutz, M.P. et al. (2022) — Studio controllato sulla psilocibina nel disturbo da uso di alcol. JAMA Psychiatry.
Articoli in relazione
-
Applicazioni terapeutiche della psilocibina
Pubblicato: 31/07/2025 14:25:24 -
Psilocibina: cos'è, come agisce e quali effetti provoca
Pubblicato: 24/07/2025 12:21:12 -
Miti sulla psilocibina che la scienza ha smentito
Pubblicato: 10/12/2025 20:34:04























