Cómo la psilocibina puede remodelar el cerebro adulto
- Qué es la neuroplasticidad y cómo funciona en el cerebro adulto
- Fundamentos biológicos y farmacología de la psilocibina
- Cómo la psilocibina transforma el cerebro adulto
- Psilocibina como psicoplastógeno: los mecanismos del cambio neuronal
- Por qué la psilocibina actúa diferente a la serotonina
- El BDNF y su papel en la plasticidad inducida por psilocibina
- ¿Por qué los efectos neuroplásticos de la psilocibina son duraderos?
- Psilocibina y cambios estructurales en preclínica
- Psilocibina y modulación de la Red Neuronal por Defecto
- Evidencia de la psilocibina en ensayos clínicos con humanos
- Depresión resistente al tratamiento
- Depresión moderada-grave: el ensayo comparativo con escitalopram
- Ansiedad y depresión asociadas a enfermedad terminal
- Trastornos por uso de sustancias
- Riesgos de una neuroplasticidad no adaptativa
- La integración como eje de la plasticidad post-psicodélica
- Fuentes y referencias
- Mecanismo molecular y neuroplasticidad
- Periodos críticos
- Red Neuronal por Defecto y entropía cerebral
- Evidencia clínica — Depresión
- Evidencia clínica — Ansiedad y enfermedad terminal
- Evidencia clínica — Adicciones
Imagina el cerebro como una montaña cubierta de nieve. Cada pensamiento recurrente, cada reacción automática y cada hábito mental es un trineo que desciende una y otra vez por el mismo recorrido. Con el tiempo, esos caminos se convierten en surcos profundos: eficientes y rápidos… pero cada vez más difíciles de abandonar.
Esta imagen resume bien lo que ocurre en muchos estados de rigidez psicológica. El estrés crónico, la ansiedad, la depresión o incluso la rutina cotidiana refuerzan patrones de pensamiento repetitivos. No porque sean los mejores, sino porque son los más transitados. El cerebro, como cualquier sistema biológico, tiende a optimizar lo conocido.
Durante décadas se asumió que esta rigidez era, en gran medida, irreversible en la edad adulta. Hoy sabemos que no tiene por qué serlo. El cerebro conserva una capacidad notable para cambiar, adaptarse y reorganizarse. A esta propiedad la llamamos neuroplasticidad.
En los últimos años, los hongos psicodélicos (en particular las especies del género Psilocybe) han reaparecido en la investigación científica como posibles catalizadores de esta plasticidad. No solo por los estados alterados de conciencia que producen, sino por algo más profundo y duradero: su capacidad para inducir cambios estructurales y funcionales en el cerebro que persisten mucho más allá de la experiencia aguda.
Este artículo explora qué significa realmente la neuroplasticidad, cómo actúa la psilocibina sobre el cerebro, qué dice la evidencia científica actual y cuáles son sus implicaciones, límites y riesgos.
Qué es la neuroplasticidad y cómo funciona en el cerebro adulto
La neuroplasticidad es la capacidad del sistema nervioso para reorganizarse a distintos niveles: molecular, celular, estructural y funcional. Implica tanto la creación de nuevas conexiones como la eliminación de aquellas que dejan de ser adaptativas —un proceso de 'limpieza' natural llamado poda sináptica que permite que el cerebro no solo crezca, sino que se refine.
Durante mucho tiempo se pensó que esta capacidad se reducía drásticamente tras la infancia, una idea heredada de los primeros modelos del desarrollo cerebral. Hoy sabemos que el cerebro adulto sigue siendo plástico, aunque esa plasticidad suele estar más "regulada" y menos disponible de forma espontánea.
Para comprender cómo los psicodélicos interactúan con estos procesos, debemos distinguir varios tipos de plasticidad relevantes:
- Plasticidad estructural: incluye el crecimiento de dendritas, la formación de nuevas sinapsis y los cambios en la densidad de espinas dendríticas. Es el sustrato físico del aprendizaje: cada vez que el cerebro consolida algo nuevo, lo hace en parte modificando la arquitectura de sus neuronas, añadiendo o reforzando los puntos de contacto entre ellas.
- Plasticidad funcional: la reorganización de las redes cerebrales y de los patrones de comunicación entre distintas regiones. No implica necesariamente cambios estructurales visibles, sino cambios en qué circuitos se activan juntos, con qué intensidad y con qué sincronía. Es la plasticidad que permite, por ejemplo, que una región dañada sea parcialmente compensada por otra, o que un hábito mental crónico se vaya debilitando cuando dejamos de alimentarlo.
- Meta-plasticidad: un concepto clave que opera a un nivel superior a los anteriores: no solo cambian las conexiones, sino el umbral para que ocurran futuros cambios. Es decir, el propio cerebro modula cuán fácil o difícil le resulta volver a moldearse en respuesta a la experiencia. Un cerebro que ha pasado por períodos de alto estrés sostenido, por ejemplo, puede volverse menos receptivo a los cambios adaptativos; uno en un estado de plasticidad elevada, al contrario, responde con más facilidad a nuevos aprendizajes y experiencias.
- Reapertura de periodos críticos: Este es uno de los conceptos más vanguardistas —y también de los más preliminares— de la neurociencia actual. Se refiere a ventanas temporales de extrema sensibilidad al entorno que, biológicamente, suelen cerrarse tras la infancia o adolescencia. La evidencia reciente sugiere que los psicodélicos pueden volver a abrir estas "puertas", devolviendo al cerebro a un estado de maleabilidad social y emocional donde es posible reescribir aprendizajes profundos —como traumas o patrones de apego— que hasta ahora se consideraban inmutables. Es importante subrayar, no obstante, que esta línea de investigación todavía no cuenta con replicaciones robustas en humanos y debe interpretarse con cautela.
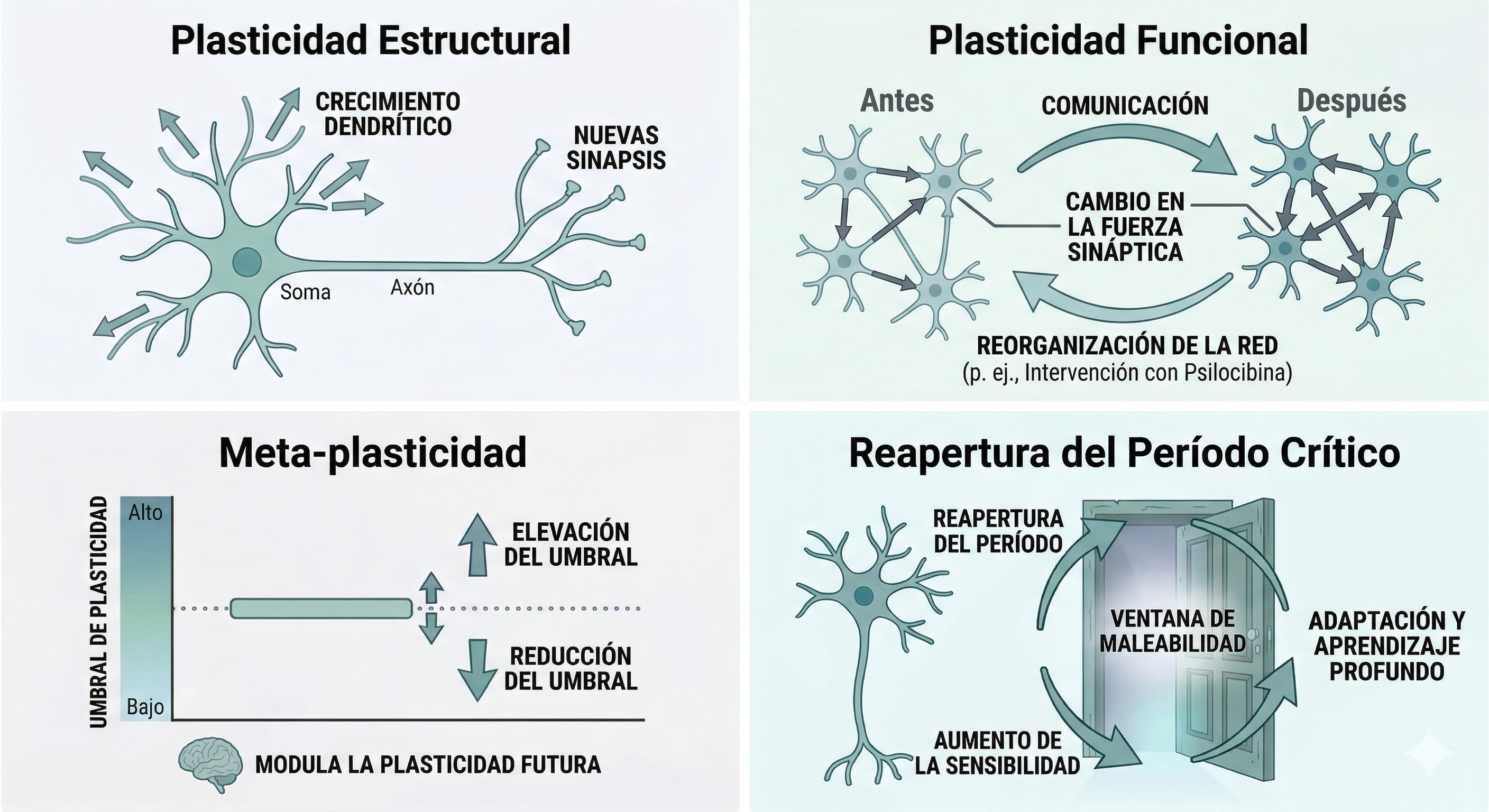
Estos diferentes tipos de plasticidad proporcionan el marco conceptual para entender cómo sustancias como la psilocibina pueden inducir cambios cerebrales significativos incluso en el adulto.
Fundamentos biológicos y farmacología de la psilocibina
Los hongos psicodélicos, especialmente las especies del género Psilocybe, producen de forma natural psilocibina. Es importante destacar que la psilocibina es, en rigor, un profármaco: una sustancia que por sí misma no es significativamente activa, pero que el cuerpo metaboliza (principalmente en el hígado) para convertirla en psilocina, que es la molécula que realmente atraviesa la barrera hematoencefálica y genera los efectos en el cerebro.
A diferencia de muchos otros metabolitos secundarios producidos por hongos y plantas, la psilocibina muestra una afinidad notable por el sistema serotoninérgico humano, en particular por ciertos receptores implicados en procesos como la percepción, la cognición y la regulación emocional.
Aunque están relacionados, la investigación actual sugiere que los segundos no pueden explicarse únicamente por los primeros. Esta distinción es crucial, ya que sugiere que la verdadera potencia terapéutica de la psilocibina podría residir no solo en la intensidad de la experiencia subjetiva, sino en la «ventana de oportunidad» biológica que se abre a nivel celular. Entender la sustancia como un modulador estructural nos permite separar el fenómeno de la alucinación del proceso de reparación y recableado neuronal que analizaremos a continuación.
Un tercer elemento, tan determinante como la dosis o el mecanismo molecular, es lo que la investigación denomina set and setting: el set hace referencia al estado interno del participante —su disposición emocional, sus expectativas y su historia personal—; el setting al entorno físico, social y relacional en que ocurre la experiencia. En los ensayos clínicos, ambos se controlan cuidadosamente mediante preparación previa, acompañamiento profesional y sesiones de integración posteriores. Esta variable no es accesoria: los estudios muestran que el mismo compuesto, administrado en contextos distintos, puede producir experiencias radicalmente diferentes, y que la calidad del set and setting predice en parte la magnitud y la dirección del cambio terapéutico.
Cómo la psilocibina transforma el cerebro adulto
Psilocibina como psicoplastógeno: los mecanismos del cambio neuronal
En los últimos años ha surgido un término clave para describir a sustancias como la psilocibina: los psicoplastógenos. El concepto, propuesto en el contexto de la investigación moderna por equipos como el de David E. Olson, se refiere a compuestos capaces de promover de forma rápida y potente la neuroplasticidad, más allá de sus efectos subjetivos.
Antes de entrar en los mecanismos moleculares, conviene señalar una distinción que a menudo se omite en la divulgación sobre este tema: no existe un único "modo de uso" de la psilocibina, y los contextos de administración producen perfiles biológicos y terapéuticos muy diferentes. En el ámbito clínico e investigador se distinguen principalmente dos aproximaciones:
- La dosis terapéutica —la empleada en los ensayos clínicos modernos— implica dosis medias o altas (generalmente entre 20 y 30 mg de psilocibina sintética, o su equivalente en hongo seco) administradas en sesiones únicas o muy escasas, siempre con acompañamiento profesional y preparación previa. Produce estados alterados de conciencia de entre cuatro y seis horas de duración y es el modelo sobre el que se acumula la mayor parte de la evidencia neurobiológica y terapéutica.
- La microdosificación, por su parte, consiste en la ingesta periódica de dosis subperceptuales —habitualmente entre 0,1 y 0,3 gramos de hongo seco— a lo largo de días o semanas, sin que se produzcan alteraciones perceptivas notables. Aunque la práctica ha ganado popularidad y existe una base amplia de usuarios que reportan beneficios en foco, estado de ánimo o creatividad, la evidencia científica sobre sus efectos neuroplásticos específicos es hoy considerablemente más limitada y menos sistemática. La gran mayoría de los hallazgos que se describen en este artículo corresponden al modelo de dosis terapéutica.
Por qué la psilocibina actúa diferente a la serotonina
Tradicionalmente se pensaba que bastaba con activar los receptores 5-HT2A situados en la superficie de la neurona para desencadenar los efectos psicodélicos. Sin embargo, investigaciones recientes han revelado un matiz neurobiológico crucial: la localización.
A diferencia de la serotonina endógena, que tiene dificultades para atravesar la membrana celular debido a su polaridad, la psilocina (y otros psicodélicos) puede cruzar esta barrera lipídica y acceder al interior de la célula. Una vez dentro, se une a una reserva de receptores 5-HT2A ubicados en organelos intracelulares, como el aparato de Golgi.
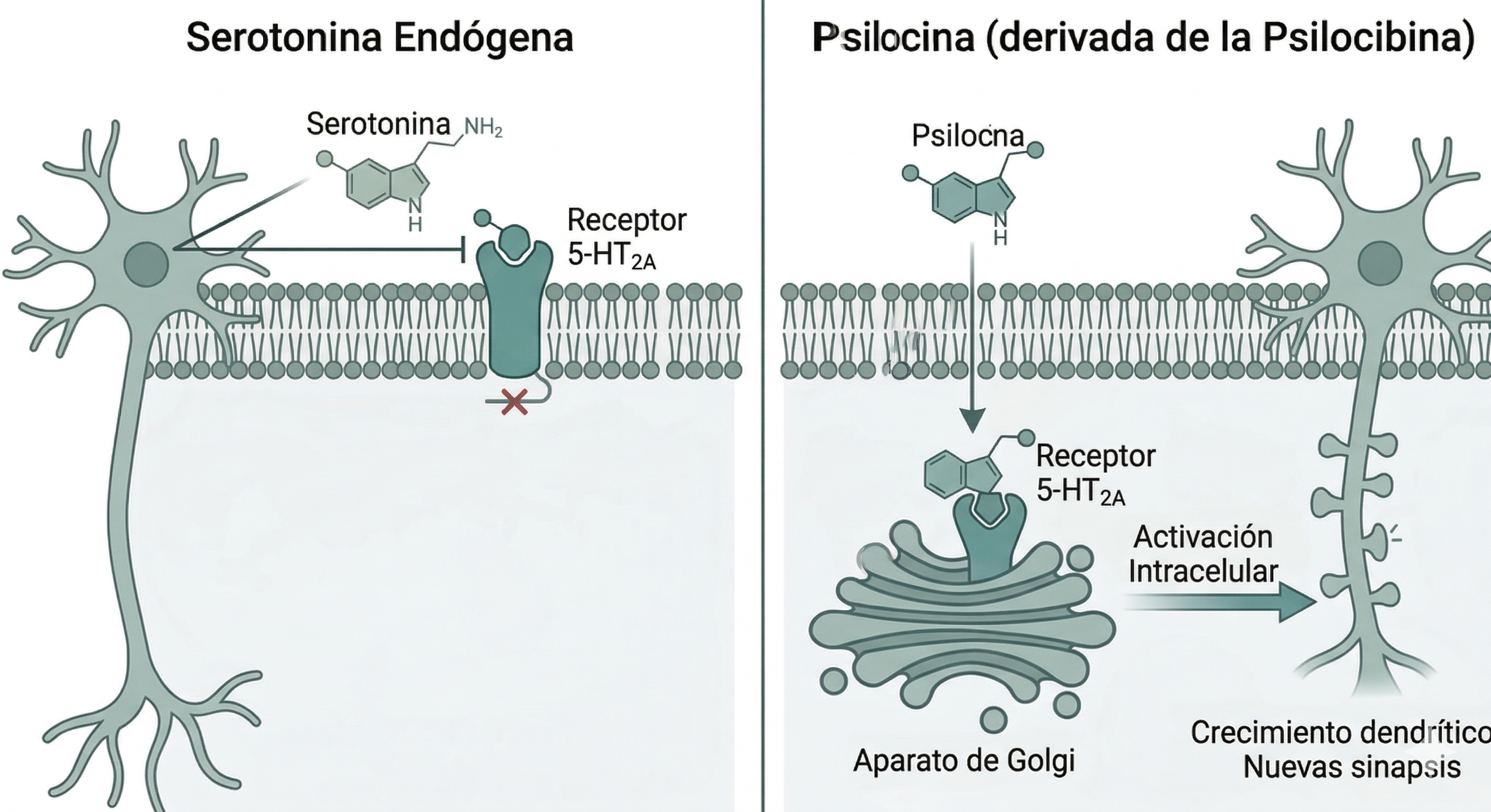
La evidencia actual sugiere que es precisamente esta activación intracelular la que desencadena de forma consistente el crecimiento de las dendritas y la formación de nuevas espinas. Esto explicaría por qué, aunque tenemos serotonina en el cerebro constantemente, esta no provoca los cambios estructurales profundos ni los estados de plasticidad rápida que observamos con los psicodélicos.
El BDNF y su papel en la plasticidad inducida por psilocibina
Uno de los actores clave en este proceso es el BDNF (Factor Neurotrófico Derivado del Cerebro), una proteína fundamental para el crecimiento, la supervivencia y la diferenciación neuronal. La psilocibina se asocia con un aumento en la expresión y liberación de BDNF, lo que facilita la activación de su receptor TrkB y contribuye a la consolidación de nuevas conexiones sinápticas.
Algunos estudios sugieren que ciertos efectos plásticos pueden producirse de forma parcialmente independiente del receptor 5-HT2A, lo que apunta a mecanismos más complejos de lo que se asumía inicialmente.
Estos cambios moleculares se traducen potencialmente en un cerebro más flexible y capaz de reorganizar sus redes, lo que sustenta mejoras en aprendizaje, adaptación y regulación emocional.
Este efecto se ve además potenciado por un mecanismo que abordaremos más adelante: la reducción simultánea de la actividad rumiante de la DMN, cuya hiperactividad crónica actúa como supresor activo de la expresión de BDNF a través del eje del estrés.
¿Por qué los efectos neuroplásticos de la psilocibina son duraderos?
Aunque la psilocibina se elimina del organismo en cuestión de horas, los cambios que induce pueden persistir durante semanas o incluso meses. Esta aparente paradoja se explica porque la sustancia no actúa únicamente como un estímulo transitorio, sino como un desencadenante de procesos biológicos que continúan desarrollándose una vez finalizada la fase aguda.
Uno de los mecanismos implicados es la activación de programas de expresión génica asociados a la plasticidad sináptica. La psilocibina induce la expresión de genes de respuesta inmediata y de otros genes implicados en el crecimiento neuronal, la estabilización de sinapsis y la reorganización de circuitos. Estos cambios moleculares pueden consolidarse con el tiempo mediante la síntesis de nuevas proteínas y la modificación estructural de las conexiones existentes.
Además, la formación de nuevas espinas dendríticas y el fortalecimiento de determinadas sinapsis no son procesos efímeros. Una vez establecidas, estas modificaciones pueden integrarse de forma relativamente estable en las redes neuronales, especialmente si van acompañadas de cambios en la experiencia, el comportamiento o el entorno del individuo.
A nivel funcional, la psilocibina también se asocia con una reorganización transitoria de las dinámicas de conectividad cerebral. Durante este periodo, el cerebro puede explorar configuraciones menos rígidas y más flexibles. En algunos casos, ciertas de estas configuraciones persisten tras la experiencia, dando lugar a patrones de procesamiento más adaptativos.
Estos datos sugieren que la duración de los efectos no depende de la presencia continua de la sustancia, sino de la capacidad de la psilocibina para iniciar una cascada de cambios moleculares, estructurales y funcionales que, bajo determinadas condiciones, pueden consolidarse a medio y largo plazo.
Psilocibina y cambios estructurales en preclínica
Los estudios preclínicos han sido fundamentales para caracterizar cómo la psilocibina induce cambios plásticos a nivel celular y estructural. En cultivos celulares, exposiciones breves a psilocibina o a compuestos análogos producen aumentos significativos en la complejidad dendrítica y en la densidad sináptica en un plazo de 24 a 72 horas. Resulta especialmente relevante que estímulos de corta duración puedan generar efectos comparables a los observados tras tratamientos prolongados.
En modelos animales, una única administración se asocia con un aumento de la densidad de espinas dendríticas en regiones clave como la corteza prefrontal medial y el hipocampo. Estos cambios pueden persistir durante varias semanas, e incluso más de un mes. Además, en modelos de estrés crónico, la psilocibina revierte la atrofia dendrítica inducida por el estrés y se asocia con mejoras en indicadores de comportamiento adaptativo.
Estos hallazgos proporcionan un soporte mecanístico sólido que justifica la exploración de la psilocibina en estudios clínicos en humanos.
Psilocibina y modulación de la Red Neuronal por Defecto
Para comprender los efectos psicológicos y terapéuticos de la psilocibina, es imprescindible hablar de la Red Neuronal por Defecto (DMN), un conjunto de regiones cerebrales altamente interconectadas que actúan como un eje organizador de la experiencia interna.
La DMN está especialmente activa cuando no realizamos una tarea concreta orientada al exterior. Se asocia con la narrativa del yo, la memoria autobiográfica, la planificación mental y la evaluación constante de uno mismo. Cuando su actividad es excesiva o rígida, se relaciona con patrones de rumiación, autocrítica y pensamiento repetitivo.
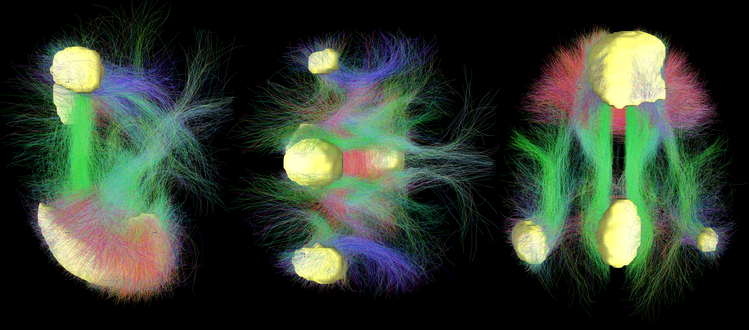
La psilocibina reduce de forma significativa la coherencia y la dominancia funcional de esta red. Es como si el "gerente" del cerebro —el sistema que centraliza, prioriza y da continuidad a la experiencia— se retirara temporalmente. Este descenso en el control jerárquico se correlaciona con la disminución de la actividad sincronizada dentro de la DMN y es lo que muchas personas describen subjetivamente como una disolución del ego.
Cuando este control se relaja, aumenta la conectividad global entre redes cerebrales. Regiones que normalmente operan de forma más segregada comienzan a intercambiar información de manera más directa. Este patrón de conectividad menos restrictivo se ha asociado a fenómenos como la sinestesia, los reencuadres cognitivos profundos y la emergencia de perspectivas no habituales.
Este aumento de conectividad global se traduce en lo que la neurociencia describe como un incremento de la entropía cerebral: el cerebro opera en un espacio de estados más amplio, con patrones de activación menos predecibles y más variables. Lejos de ser un signo de desorganización patológica, esta entropía elevada refleja un cerebro temporalmente liberado de sus rutinas perceptivas y cognitivas más rígidas —más parecido, en términos de dinámica de red, al cerebro de un niño explorando el mundo que al de un adulto resolviendo lo conocido.
Desde el punto de vista de la neuroplasticidad, un cerebro menos jerárquico y menos constreñido por modelos internos dominantes es un cerebro más maleable. Esta ventana de flexibilidad es clave para entender por qué ciertas experiencias inducidas por la psilocibina pueden facilitar cambios psicológicos duraderos.
Evidencia de la psilocibina en ensayos clínicos con humanos
Antes de entrar en los estudios concretos, conviene enmarcar el estado actual del campo. La investigación clínica con psilocibina ha avanzado notablemente en la última década, pero sigue operando con muestras relativamente pequeñas, protocolos heterogéneos y una limitación estructural difícil de resolver: el ciego doble verdadero es prácticamente imposible cuando los participantes pueden percibir con claridad si recibieron la sustancia activa. Esto no invalida los hallazgos —la consistencia de los efectos a través de distintos grupos, instituciones y metodologías es en sí misma una señal sólida— pero sí exige leer los resultados con la precisión que merece cualquier ciencia en construcción.
Depresión resistente al tratamiento
Los ensayos más influyentes provienen del grupo de Robin Carhart-Harris, iniciados en el Imperial College de Londres y posteriormente continuados en la Universidad de California San Francisco. Sus estudios con pacientes que no habían respondido a múltiples líneas de tratamiento farmacológico convencional documentaron reducciones significativas en la sintomatología depresiva tras una o dos sesiones de psilocibina integradas en un protocolo de apoyo psicoterapéutico.
En neuroimagen funcional, estos trabajos revelaron una reducción persistente de la actividad de la DMN semanas después de la intervención, correlacionada con la mejoría clínica.
Depresión moderada-grave: el ensayo comparativo con escitalopram
El mismo grupo lideró posteriormente un ensayo con una población diferente: pacientes con depresión moderada-grave sin criterio de resistencia al tratamiento. El ensayo publicado en The New England Journal of Medicine en 2021 comparó psilocibina con el antidepresivo escitalopram y mostró resultados comparables en la escala de síntomas primaria —si bien el endpoint primario no alcanzó significación estadística, en parte por el tamaño muestral— y resultados superiores para el grupo de psilocibina en varias medidas secundarias de bienestar emocional. El escitalopram presentó respuesta más rápida en las primeras semanas, lo que sugiere que ambas intervenciones tienen perfiles temporales distintos y potencialmente complementarios.
Ansiedad y depresión asociadas a enfermedad terminal
El grupo de Roland Griffiths en la Johns Hopkins University ha producido algunos de los ensayos más cuidadosamente diseñados del campo. En un estudio controlado con aleatorización con pacientes oncológicos con diagnóstico potencialmente mortal, una única dosis alta de psilocibina produjo reducciones clínicamente significativas tanto en ansiedad como en depresión, que se mantuvieron estables en seguimientos realizados a los seis meses. En aproximadamente el 80 % de los participantes los efectos beneficiosos seguían siendo perceptibles en evaluaciones a largo plazo, un dato de persistencia inusual en psicofarmacología. Los autores observaron además que la intensidad de la experiencia mística durante la sesión correlacionaba con la magnitud del beneficio terapéutico posterior, lo que ha alimentado el debate sobre la relevancia del componente experiencial en el mecanismo de acción.
Trastornos por uso de sustancias
La investigación ha arrojado resultados preliminares notables. El grupo de Johns Hopkins publicó un estudio piloto sobre dependencia al tabaco en el que dos o tres sesiones de psilocibina combinadas con terapia cognitivo-conductual produjeron tasas de abstinencia a los seis meses superiores al 60 %, muy por encima de los referentes históricos de los tratamientos de primera línea. Para el trastorno por uso de alcohol, un ensayo controlado de la Universidad de Nueva York reportó reducciones sostenidas y significativas en el consumo frente a placebo activo. Ambas líneas de investigación son todavía incipientes en términos de tamaño muestral y requieren replicación, pero la magnitud de los efectos observados justifica el interés creciente.
Técnicas de neuroimagen funcional y estructural muestran cambios en la conectividad entre regiones prefrontales y subcorticales semanas después de una única administración. Estas modificaciones afectan a circuitos implicados en la regulación emocional, la toma de decisiones y la respuesta al estrés. Asimismo, se han descrito variaciones en el grosor cortical en áreas relacionadas con el control cognitivo y la integración emocional.
A nivel psicológico, se han documentado mejoras sostenidas en flexibilidad cognitiva, empatía emocional y bienestar subjetivo. Estos cambios no van acompañados de un deterioro de las funciones cognitivas básicas, como la memoria de trabajo o la atención, lo que refuerza el perfil de seguridad observado en los estudios controlados.
En contextos terapéuticos controlados, especialmente en depresión resistente o ansiedad, los efectos beneficiosos pueden mantenerse durante meses e incluso hasta un año tras una o dos sesiones, siempre integradas en un marco de acompañamiento psicológico.
| Condición | Institución | Resultado Clave |
|---|---|---|
| Depresión Resistente | Imperial College / UCSF | Mejoría rápida; superior a fármacos comunes en bienestar a largo plazo. |
| Ansiedad Terminal | Johns Hopkins University | 80% de éxito con mejoría clínica sostenida tras 6 meses. |
| Adicción al Tabaco | Johns Hopkins University | 60% de abstinencia a los 6 meses (dobla la eficacia convencional). |
| Uso de Alcohol | NYU | Descenso significativo en días de consumo excesivo frente a placebo. |
Riesgos de una neuroplasticidad no adaptativa
La psilocibina induce cambios cerebrales reales. Eso significa que los riesgos también son reales. El ejemplo más claro es el HPPD (trastorno perceptual persistente post-alucinógeno): distorsiones visuales que reaparecen semanas o meses después de la experiencia. Es la demostración más directa de que más plasticidad no equivale automáticamente a "mejor" plasticidad: en ciertos individuos, los circuitos de procesamiento se consolidan de maneras no deseadas.
Para que esta ventana de maleabilidad sea terapéutica y no desestabilizadora, el cribado médico previo y el contexto son innegociables. Sin un marco de seguridad y una integración posterior, el cerebro puede reforzar patrones poco adaptativos en lugar de romperlos. Estas son las exclusiones médicas y farmacológicas sistemáticas en la investigación clínica:
Criterios de exclusión y precauciones médicas
- Salud Mental: Antecedentes personales o familiares de psicosis, esquizofrenia o trastorno bipolar tipo I.
- Interacciones Farmacológicas: Uso de Litio (riesgo de convulsiones), IMAO o antidepresivos serotoninérgicos.
- Condiciones Físicas: Cardiopatías no controladas, epilepsia activa o embarazo.
- Seguridad Psicológica: No se recomienda el uso sin acompañamiento profesional en casos de trauma complejo no procesado.
La precisión en el cribado es lo que separa una experiencia transformadora de un riesgo innecesario. Para un análisis técnico detallado de cada interacción y protocolo de seguridad, puedes consultar nuestra guía completa de riesgos y contraindicaciones de la psilocibina.
La integración como eje de la plasticidad post-psicodélica
Tras la experiencia psicodélica, el cerebro permanece durante días o semanas en un estado de plasticidad elevada. Volviendo a nuestra metáfora inicial: la nieve fresca cubre los surcos antiguos. Pero la nieve no decide por sí sola qué nuevos caminos se forman. Si no hay cambios en el entorno, los hábitos o el acompañamiento terapéutico, el peso de la repetición volverá a abrir exactamente los mismos surcos de antes. Y eso tiene consecuencias en ambas direcciones.
Por eso, la integración es fundamental. La evidencia indica que la psilocibina no es una panacea, sino un modulador: una señal que el cerebro interpreta para construir —o eliminar— conexiones reales a nivel molecular, estructural y funcional.
Este proceso puede persistir meses tras una única sesión, ofreciendo implicaciones terapéuticas genuinas en depresión, ansiedad y adicciones. Sin embargo, los efectos dependen del contexto y el campo sigue siendo una ciencia en construcción. En un territorio donde la biología y la experiencia subjetiva se superponen, la precisión no es un detalle: es el punto de partida.
Fuentes y referencias
Mecanismo molecular y neuroplasticidad
- Olson, D.E. (2021) — Propuesta del concepto de psicoplastógenos y su potencial terapéutico. Journal of Experimental Neuroscience.
- Ly, C. et al. (2018) — Evidencia de que los psicodélicos promueven plasticidad estructural y funcional en neuronas corticales. Cell Reports.
- Vargas, M.V. et al. (2023) — Demostración de que los receptores 5-HT2A intracelulares median los efectos neuroplásticos. Science.
Periodos críticos
- Nardou, R. et al. (2023) — Los psicodélicos reabren el periodo crítico de aprendizaje de recompensa social. Nature.
Red Neuronal por Defecto y entropía cerebral
- Carhart-Harris, R.L. et al. (2012) — Correlatos neurales del estado psicodélico medidos con fMRI y reducción de la DMN. PNAS.
- Carhart-Harris, R.L. et al. (2014) — La teoría del cerebro entrópico: incremento de la entropía como sustrato de la experiencia. Frontiers in Human Neuroscience.
Evidencia clínica — Depresión
- Carhart-Harris, R. et al. (2021) — Ensayo comparativo entre psilocibina y escitalopram en depresión moderada-grave. New England Journal of Medicine.
- Davis, A.K. et al. (2021) — Efectos de la terapia asistida con psilocibina en trastorno depresivo mayor. JAMA Psychiatry.
Evidencia clínica — Ansiedad y enfermedad terminal
- Griffiths, R.R. et al. (2016) — Reducción sustancial y sostenida de depresión y ansiedad en pacientes oncológicos. Journal of Psychopharmacology.
- Ross, S. et al. (2016) — Reducción rápida y sostenida de ansiedad y depresión en cáncer avanzado. Journal of Psychopharmacology.
Evidencia clínica — Adicciones
- Johnson, M.W. et al. (2014) — Psilocibina como apoyo para la cesación tabáquica: estudio piloto. Journal of Psychopharmacology.
- Bogenschutz, M.P. et al. (2015) — Estudio de concepto sobre psilocibina en dependencia al alcohol. Journal of Psychopharmacology.
- Bogenschutz, M.P. et al. (2022) — Ensayo controlado sobre psilocibina en trastorno por uso de alcohol. JAMA Psychiatry.
Artículos relacionados
-
Aplicaciones terapéuticas de la psilocibina
Publicado : 31/07/2025 14:25:24 -
Psilocibina: qué es, cómo actúa y qué efectos provoca
Publicado : 24/07/2025 12:21:12 -
Mitos sobre la psilocibina que la ciencia desmiente
Publicado : 10/12/2025 20:34:04























