Guida agli alcaloidi dei funghi psilocibici
- Perché due funghi identici producono esperienze diverse
- Come i funghi producono la psilocibina: origine molecolare ed evoluzione
- Gli alcaloidi del fungo, molecola per molecola
- Psilocibina: il profarmaco che viaggia
- Psilocina: ciò che il cervello riceve
- Baeocistina: la terza incomoda
- Norbaeocistina: la più basilare e la meno nota
- Aeruginascina: l'alcaloide che cambia il tono emotivo
- Tabella comparativa degli alcaloidi dei funghi psilocibini
- Una nota sulle β-carboline
- Potenza per specie e fattori che determinano la concentrazione alcaloide
- Variabili che influenzano la concentrazione alcaloide
- L'effetto entourage come ipotesi scientifica
- Equivalenze di dose tra fungo essiccato e composto isolato
- Biosintesi eterologa, nuove specie e psychoplastogens
- Produrre ciò che la natura sintetizza
- La diversità alcaloide che non abbiamo ancora esplorato
- Separare l'effetto terapeutico da quello psicoattivo
- Una molecola dominante, una complessità irrisolta
- Riferimenti
Perché due funghi identici producono esperienze diverse
Immagina di avere davanti a te due campioni di fungo essiccato. Li analizzi in laboratorio: stesso contenuto di psilocibina, stesso peso, stessa specie. Li somministri a due volontari con lo stesso set and setting, la stessa preparazione, lo stesso accompagnamento terapeutico. E i risultati sono diversi: uno descrive un'esperienza marcatamente ansiosa, l'altro parla di euforia e apertura emotiva prolungata.
Com'è possibile?
Per decenni, la risposta convenzionale è stata: «variabili psicologiche del soggetto». E senza dubbio il set —lo stato mentale previo— è un fattore determinante. Ma esiste un'altra risposta che la scienza costruisce in silenzio da anni, e che obbliga a ripensare il modo in cui leggiamo l'etichetta di un fungo: i funghi psilocibini non contengono un unico composto attivo. Contengono una famiglia di alcaloidi che agiscono in concerto, e questa orchestrazione chimica può essere altrettanto responsabile del profilo dell'esperienza quanto la psicologia del consumatore.

Questa guida scompone quella famiglia, molecola per molecola, perché ciò che i trial clinici stanno somministrando —psilocibina sintetica pura— è una versione deliberatamente semplificata di ciò che il fungo contiene.
Come i funghi producono la psilocibina: origine molecolare ed evoluzione
Prima di parlare degli effetti, vale la pena capire da dove vengono questi composti e perché un fungo li produce.
Gli alcaloidi psicoattivi dei funghi psilocibini sono derivati del triptofano, uno dei venti aminoacidi essenziali che gli organismi viventi usano per costruire proteine. Strutturalmente, condividono tutti un nucleo indolico — lo stesso scheletro molecolare della serotonina, il principale neurotrasmettitore dell'umore — ed è questa similitudine strutturale che permette loro di interagire con i recettori cerebrali progettati per la serotonina. Sono, in senso letterale, molecole che il cervello scambia con il proprio linguaggio interno.
Il macchinario biosintetico che fabbrica queste molecole è stato descritto in dettaglio nel 2017 da Fricke et al. su Angewandte Chemie: una catena di quattro enzimi codificati dal cluster genico denominato psi, che trasforma il triptofano in psilocibina attraverso quattro passaggi successivi. Ogni enzima ha una funzione specifica: PsiD decarbossila il triptofano, PsiK aggiunge il gruppo fosfato, PsiM introduce i gruppi metile, e PsiH esegue l'idrossilazione finale. È un processo modulare, elegante nella sua logica, che la biotecnologia ha già riprodotto in lieviti e batteri di laboratorio.
Ma la scoperta più sconcertante su questa via biosintetica è arrivata nel 2025, in uno studio pubblicato su Nature Chemical Biology da Heim et al.: i funghi del genere Psilocybe e quelli del genere Conocybe —due lignaggi evolutivamente distanti all'interno del regno dei funghi— hanno sviluppato la capacità di sintetizzare la psilocibina in modo completamente indipendente. Non hanno ereditato gli stessi enzimi da un antenato comune: hanno inventato enzimi diversi che eseguono le stesse trasformazioni chimiche per arrivare allo stesso prodotto finale.
Questo si chiama evoluzione convergente, ed è relativamente rara in biochimica. Che accada con una molecola così specifica e farmacologicamente attiva come la psilocibina suggerisce che esiste una potente pressione selettiva che ne favorisce la sintesi. L'ipotesi più diffusa è che serva come difesa contro predatori o parassiti, sebbene rimanga un'area di ricerca attiva. Ciò che è innegabile è il dato in sé: due organismi senza relazione ancestrale diretta hanno «scoperto», separatamente, la stessa soluzione chimica. In termini di complessità biochimica, è una scoperta della stessa famiglia concettuale dell'occhio del polpo e dell'occhio umano. La vita, quando ha bisogno di qualcosa, tende a trovarlo attraverso percorsi molteplici.
L'enigma evolutivo della psilocibina
La psilocibina non appartiene a un solo fungo. Appare in specie separate da milioni di anni di evoluzione. Questo articolo esplora come la biologia ha trovato (e condiviso) la stessa soluzione ancora e ancora.
Read moreGli alcaloidi del fungo, molecola per molecola
Psilocibina: il profarmaco che viaggia
C₁₂H₁₇N₂O₄P · 4-fosforiloss-N,N-dimetiltriptamina · 4-PO-DMT
La psilocibina è l'alcaloide più abbondante e più stabile della famiglia. A temperatura ambiente si presenta come un solido cristallino bianco che, in assenza di umidità estrema e luce diretta, mantiene tra il 90 e il 95% della sua attività per uno o due anni.
Ma la psilocibina, da sola, non fa nulla nel cervello.
È ciò che i farmacologi chiamano un profarmaco: una molecola inattiva progettata per essere convertita nella sua forma attiva dal metabolismo dell'organismo ricevente. Quando viene ingerita per via orale, la psilocibina viene assorbita nel tratto gastrointestinale e arriva al fegato, dove le fosfatasi alcaline rimuovono il gruppo fosfato e liberano la psilocina. Questo processo, che richiede tra i venti e i sessanta minuti, è responsabile dell'insorgenza relativamente lenta degli effetti rispetto ad altre sostanze psicoattive. La biodisponibilità orale oscilla tra il 52% e il 74% secondo studi di farmacocinetica revisionati negli ultimi anni.
La funzione del gruppo fosfato non è meramente scomoda: rende la molecola più polare, più solubile in acqua e più stabile. La psilocibina è, in un certo senso, un sistema di trasporto intelligente che protegge la psilocina dalla degradazione fino a quando non raggiunge il luogo dove deve agire.
Psilocina: ciò che il cervello riceve
C₁₂H₁₆N₂O · 4-idrossi-N,N-dimetiltriptamina · 4-HO-DMT
La psilocina è il composto che occupa realmente i recettori cerebrali. Senza il gruppo fosfato che la incatena nella psilocibina, è direttamente attiva e agisce più rapidamente. L'inconveniente di questa libertà chimica è l'instabilità: in presenza di ossigeno si ossida rapidamente, assumendo tonalità marroni o nere. È questo processo a spiegare il famoso inbluimento dei funghi.

Il blu merita di essere spiegato bene, perché è probabilmente il fenomeno visivo più noto di questi funghi ed è stato interpretato in modo impreciso per decenni. Quando un fungo psilocibino viene tagliato o pressato, la psilocina liberata dal tessuto entra in contatto con l'ossigeno dell'aria e si ossida formando chinoni di colore blu indaco. Questo meccanismo è stato caratterizzato con precisione per la prima volta nel 2020 dal team di Dirk Hoffmeister all'Università di Jena: i composti risultanti sono chimicamente distinti dalla psilocina e non hanno attività psicoattiva nota. Ma la loro presenza è l'indicatore visivo più affidabile che il fungo contiene alcaloidi attivi. L'intensità dell'inbluimento non è proporzionale alla potenza, ma la sua assenza indica quasi sempre l'assenza di psilocina.
Nel cervello, la psilocina agisce principalmente come agonista dei recettori della serotonina di tipo 2A (5-HT₂A), presenti in alta densità nello strato V della corteccia prefrontale e nelle regioni limbiche. Ma la farmacologia della psilocina è più promiscua di quanto suggerisca quel titolo: mostra affinità anche per i sottotipi 5-HT₁A, 5-HT₂C, 5-HT₆ e 5-HT₇, oltre che per recettori dopaminergici (D₂, D₃) e adrenergici (α₂). Questa rete di interazioni contribuisce alla ricchezza e variabilità del profilo degli effetti: non è che il fungo prema un unico pulsante neuronale, ma che accordi uno strumento complesso.
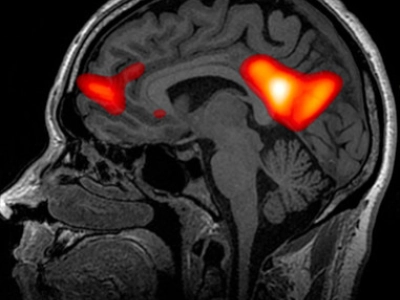
Gli studi di neuroimaging hanno documentato due fenomeni simultanei sotto psilocina che risultano particolarmente illuminanti. Da un lato, esiste una iperconnettività tra regioni cerebrali che normalmente non comunicano tra loro: la corteccia visiva parla con quella uditiva, quella sensoriale con la motoria, il lobo temporale con il frontale. Dall'altro, si produce una marcata soppressione della Rete Neurale di Default —Default Mode Network o DMN—, il circuito che gestisce la narrativa dell'io, il pensiero ruminativo e l'identità personale. Il DMN è, in senso molto concreto, la rete che mantiene la storia che ci raccontiamo su chi siamo. La sua inibizione sotto psilocina si correla direttamente con l'esperienza soggettiva di dissoluzione dell'ego, e anche — questo è ciò che è clinicamente rilevante — con l'entità dell'effetto antidepressivo osservato negli studi terapeutici. Questo fenomeno viene approfondito nell'analisi sulle applicazioni cliniche della psilocibina.
Più nuove connessioni, meno controllo dell'io abituale. Quel doppio meccanismo è la base neurobiologica sia delle esperienze mistiche sia dell'effetto antidepressivo.
Baeocistina: la terza incomoda
C₁₁H₁₅N₂O₄P · 4-fosforiloss-N-metiltriptamina
La baeocistina è strutturalmente la versione mono-metilata della psilocibina: una sola differenza chimica che la rende il terzo alcaloide più studiato della famiglia. Fu descritta per la prima volta nel 1968 da Repke et al. in Psilocybe baeocystis, la specie che le dà il nome, e da allora è rimasta in una sorta di limbo scientifico: troppo presente per essere ignorata, troppo poco studiata per essere ben caratterizzata.
In alcune specie, la baeocistina può raggiungere concentrazioni paragonabili alla psilocibina. P. baeocystis può contenerne tra lo 0,10% e lo 0,18% in peso secco; P. semilanceata, il noto «cappello elfico» dei prati europei, arriva allo 0,42% in alcune analisi. Non sono quantità trascurabili.
Ma cosa fa esattamente? Questa è la domanda alla quale la letteratura scientifica risponde con un'onestà che merita di essere trasmessa senza attenuazioni: non lo sappiamo con certezza. Gli studi sui roditori suggeriscono che produce effetti psicoattivi lievi a dosi equivalenti. Uno studio controllato del 2020 (Sherwood et al. su ACS Pharmacology & Translational Science) non ha trovato differenze statisticamente significative tra psilocibina da sola e psilocibina più baeocistina in modelli comportamentali animali. Ma un risultato negativo nei topi non esclude un effetto sinergico negli esseri umani. La farmacologia del contesto — come una molecola modifica la risposta a un'altra — è uno dei territori più difficili da studiare in psicofarmacologia, e i modelli animali hanno limiti chiari quando l'oggetto di studio coinvolge l'esperienza soggettiva.
Norbaeocistina: la più basilare e la meno nota
C₁₀H₁₃N₂O₄P · 4-fosforilossitriptamina
La norbaeocistina è la forma più basilare dello scheletro alcaloide psilocibino: senza alcun gruppo metile sull'azoto. Le sue concentrazioni nei funghi sono di solito le più basse della famiglia, raramente superiori allo 0,05% in peso secco. La sua scarsa liposolubilità — la proprietà che consente alle molecole di attraversare le membrane cellulari, inclusa la barriera emato-encefalica — suggerisce una penetrazione cerebrale diretta limitata.
Il che non esclude un ruolo di precursore metabolico: i funghi potrebbero usarla come punto di partenza per sintetizzare gli altri alcaloidi, il che significherebbe che la sua concentrazione è inversamente proporzionale all'efficienza biosintetica dell'organismo. Esiste anche la possibilità che agisca come modulatore allosterico — una molecola che non attiva direttamente un recettore ma altera il modo in cui altri composti lo fanno —, sebbene questa ipotesi non disponga ancora di prove dirette.
Aeruginascina: l'alcaloide che cambia il tono emotivo
C₁₂H₁₉N₂O₄P · N,N,N-trimetil-4-fosforilossitriptamina
L'aeruginascina merita un'attenzione particolare, perché è il composto che mette più direttamente in discussione il modello semplificato secondo cui «la psilocibina fa tutto».
Fu identificata nel 1985 in Inocybe aeruginascens, una specie dall'aspetto modesto e distribuzione principalmente europea che per lungo tempo fu classificata come non psicoattiva — o pericolosamente tossica — finché le analisi chimiche non rivelarono che contiene livelli di psilocibina paragonabili a quelli delle specie di Psilocybe. Ciò che attirò l'attenzione dei ricercatori fu la discrepanza tra il contenuto alcaloide e gli effetti riportati: chi consumava I. aeruginascens — in molti casi accidentalmente, scambiandola per funghi commestibili — descriveva invariabilmente un'esperienza marcatamente euforica, con quasi totale assenza di ansia e nausea.
Il ricercatore tedesco Jochen Gartz fu il primo a proporre, negli anni novanta, che la responsabile di quel profilo differenziale fosse l'aeruginascina: un composto che, a differenza di tutti gli altri alcaloidi psilocibini, non agisce come agonista del recettore 5-HT₂A bensì come antagonista del recettore 5-HT₃.
Il recettore 5-HT₃ è l'unico recettore serotoninergico ionotropico — agisce come un canale ionico, non come un recettore accoppiato a proteine G — ed è implicato nella mediazione della nausea, del vomito e di certi aspetti dell'elaborazione emotiva, in particolare dell'ansia anticipatoria. Gli antagonisti del 5-HT₃ sono farmaci ampiamente utilizzati in oncologia proprio per ridurre la nausea indotta dalla chemioterapia. L'ipotesi di Gartz — che l'aeruginascina modifichi il profilo del viaggio perché blocca questo recettore — ha una coerenza farmacologica reale, sebbene le prove dirette nell'uomo restino osservazionali.
L'implicazione terapeutica è immediata: se l'aeruginascina riduce la probabilità di esperienze avverse attraverso il blocco del 5-HT₃, potrebbe essere un componente di grande valore nella progettazione di protocolli terapeutici. Gli studi attuali di Compass Pathways, MAPS e altri gruppi lavorano esclusivamente con psilocibina sintetica pura. Nessuna aeruginascina. Questa esclusione è metodologicamente comprensibile — studiare un composto isolato è metodologicamente più semplice — ma significa che non sappiamo se la psilocibina pura è la formulazione ottimale per l'uso terapeutico.
Applicazioni terapeutiche della psilocibina
La psilocibina è passata dall'essere una droga proibita a uno strumento clinico promettente. Esploriamo come sta ridefinendo il trattamento di disturbi come la depressione, l'ansia e le dipendenze.
Read moreTabella comparativa degli alcaloidi dei funghi psilocibini
La famiglia completa, in sintesi:
| Alcaloide | Formula | Concentrazione tipica (% PS) | Recettore principale | Funzione proposta |
|---|---|---|---|---|
| Psilocibina | C₁₂H₁₇N₂O₄P | 0,1 – 1,0 | 5-HT₂A (profarmaco) | Alcaloide centrale. Serbatoio di psilocina. Principale azione psichedelica. |
| Psilocina | C₁₂H₁₆N₂O | 0,01 – 0,6 | 5-HT₂A (agonista diretto) | Vero metabolita attivo. Insorgenza più rapida quando libera. |
| Baeocistina | C₁₁H₁₅N₂O₄P | 0,01 – 0,5 | 5-HT₂A (lieve) | Modulatore proposto. Alta variabilità tra specie. |
| Norbaeocistina | C₁₀H₁₃N₂O₄P | Tracce < 0,05 | Parzialmente sconosciuto | Possibile precursore o modulatore allosterico. |
| Aeruginascina | C₁₂H₁₉N₂O₄P | 0 – 0,5 (variabile per specie) | 5-HT₃ (antagonista) | Blocca la nausea. Modula il tono emotivo. Associata a esperienze euforiche. |
| β-Carboline | Varie | Tracce | IMAO lieve | Possibile prolungamento dell'effetto per inibizione del metabolismo epatico. |
| Feniletilamine | Varie | Tracce | Dopaminergico / adrenergico | Energizzanti. Raramente quantificate. |
Concentrazioni espresse in percentuale sul peso secco (% PS), convenzione standard nella letteratura analitica.
Una nota sulle β-carboline
Le β-carboline — armina, armalina, tetraidroarmina — sono inibitori delle monoaminossidasi (IMAO) che si trovano in concentrazioni di tracce in alcuni funghi psilocibini, documentate nello studio di Blei et al. (2020) su Chemistry – A European Journal. La loro presenza nel fungo suscita immediati confronti con l'ayahuasca, che utilizza piante ricche di β-carboline proprio per inibire la degradazione epatica del DMT. Nei funghi, tuttavia, le concentrazioni rilevate sono generalmente troppo basse per produrre un effetto IMAO clinicamente significativo da sole. Potrebbero essere farmacologicamente irrilevanti nella maggior parte delle circostanze, oppure potrebbero avere un sottile effetto potenziante che gli studi attuali non hanno una risoluzione sufficiente per rilevare.
Potenza per specie e fattori che determinano la concentrazione alcaloide
La distribuzione degli alcaloidi non è uniforme nel genere Psilocybe. Le circa 200 specie riconosciute mostrano profili biochimici distinti, e quelle differenze hanno conseguenze reali.
| Specie | Psilocibina (% PS) | Psilocina (% PS) | Baeocistina (% PS) | Osservazioni |
|---|---|---|---|---|
| P. cubensis | 0,14 – 0,42 | 0,01 – 0,05 | 0,02 – 0,18 | La più coltivata. Alta variabilità tra ceppi. Riferimento di fatto nella ricerca clinica. |
| P. semilanceata | 0,60 – 1,28 | < 0,01 | 0,03 – 0,42 | La più potente d'Europa. Quasi tutta la potenza in psilocibina: insorgenza lenta, profilo stabile. |
| P. azurescens | 1,00 – 1,78 | 0,38 – 0,50 | 0,04 – 0,18 | Massima potenza documentata nel genere. Psilocina elevata: insorgenza rapida, intensità elevata. Associata a paralisi temporanea reversibile in alcuni consumatori (wood lovers paralysis). |
| P. cyanescens | 0,85 – 1,50 | 0,15 – 0,30 | 0,03 – 0,10 | Molto diffusa nei climi oceanici. Effetto fisico intenso per l'elevata psilocina. |
| P. tampanensis | 0,31 – 0,68 | < 0,02 | 0,02 – 0,10 | Produce sclerozi (tartufi magici). Profilo delicato e introspettivo. |
| P. mexicana | 0,17 – 0,25 | 0,01 – 0,03 | 0,01 – 0,03 | Uso rituale mesoamericano documentato da secoli. Base storica della ricerca moderna. |
| P. baeocystis | 0,60 – 0,85 | 0,10 – 0,14 | 0,10 – 0,18 | Baeocistina elevata. Profilo differenziale attribuito alla sua composizione. Specie di interesse per la ricerca sull'effetto entourage. |
| P. subtropicalis (ibrido selettivo 2025) |
fino a 5,0 (dato non replicato) |
variabile | nessun dato | Ceppo sviluppato mediante ibridazione selettiva assistita da sequenziamento genomico. Nessun dato clinico standardizzato. |
I valori sono intervalli rappresentativi basati sulla sintesi di molteplici studi analitici pubblicati tra il 2010 e il 2025, utilizzando metodologie HPLC, GC-MS e UPLC. La variabilità all'interno di ogni specie può essere tanto elevata quanto la variabilità tra le specie.
Ci sono due pattern che meritano analisi. Il primo è una correlazione inversa tra facilità di coltivazione e potenza: le specie più gestibili da coltivare in condizioni controllate, come P. cubensis, sono sistematicamente le meno potenti. Le più potenti — P. azurescens, P. cyanescens — richiedono condizioni di coltivazione all'aperto e sono più difficili da standardizzare, il che crea un paradosso per la ricerca: le specie più rilevanti terapeuticamente potrebbero essere le più difficili da produrre con la consistenza che i trial clinici richiedono.
Il secondo pattern è la differenza nel rapporto psilocibina/psilocina. P. semilanceata ha quasi tutta la sua potenza immagazzinata come psilocibina — che deve essere convertita in psilocina prima di agire —, il che produce un profilo a insorgenza lenta e plateau stabile. P. azurescens ha livelli eccezionalmente elevati di psilocina libera, che agisce direttamente: insorgenza più rapida, intensità più brusca. Due funghi di potenza totale simile possono risultare radicalmente diversi per questo motivo.
Variabili che influenzano la concentrazione alcaloide
Genetica: È il fattore dominante. All'interno della stessa specie, ceppi diversi possono variare il loro contenuto di psilocibina fino a un fattore di quattro o cinque. Il ceppo Golden Teacher di P. cubensis produce consistentemente meno alcaloidi rispetto al Penis Envy, pur essendo la stessa specie. Nel 2025, gruppi di coltivatori che combinano il sequenziamento genomico con l'ibridazione di lignaggi distanti hanno prodotto ceppi con fino al 5% di alcaloidi totali in peso secco, rispetto allo 0,5-1% tipico del P. cubensis standard. Questo rappresenta un salto di potenza che la maggior parte delle guide al dosaggio disponibili non contempla.
Substrato: Fattore secondario ma reale. I funghi coltivati su chicchi di segale o riso tendono a produrre corpi fruttiferi con concentrazioni di alcaloidi più elevate rispetto a quelli coltivati su paglia o cocco, presumibilmente perché la disponibilità di triptofano come precursore biosintetico varia con il substrato nutrizionale.
Fase di sviluppo: La concentrazione di psilocibina raggiunge il suo massimo poco prima che il velo che copre le lamelle si rompa. Dopo la rottura del velo e l'inizio della sporulazione, la concentrazione può scendere significativamente nel giro di ore. Il momento della raccolta conta più di quanto venga comunemente riconosciuto.
Conservazione: La psilocibina, in materiale essiccato conservato correttamente — buio, temperatura stabile, assenza di umidità — mantiene il 90-95% della sua attività per dodici-ventiquattro mesi. La psilocina si degrada più rapidamente per ossidazione. L'imbrunimento progressivo del materiale conservato è un segnale di perdita di alcaloidi attivi.
L'effetto entourage come ipotesi scientifica
Il concetto di effetto entourage è stato coniato nell'ambito della cannabis per descrivere la sinergia tra cannabinoidi e terpeni. Negli ultimi anni ha iniziato a essere applicato ai funghi psilocibini, non senza cautela, perché le prove disponibili sono qualitativamente diverse da quelle esistenti per la cannabis.
La domanda centrale è: il fungo intero produce effetti diversi — quantitativamente o qualitativamente — rispetto alla psilocibina isolata, a parità di dose di psilocibina?
I meccanismi proposti sono farmacologicamente plausibili. La baeocistina potrebbe agire come agonista parziale a 5-HT₂A, modulando la risposta massima alla psilocina attraverso la competizione per lo stesso recettore — un fenomeno noto in farmacologia come effetto soffitto competitivo. L'aeruginascina potrebbe attenuare la componente ansiosa bloccando il 5-HT₃, come già discusso. Le β-carboline potrebbero estendere la finestra di esposizione attiva riducendo la clearance epatica della psilocina, prolungando l'effetto senza aumentare la dose. E potrebbero esistere composti ancora non identificati che influenzano le vie dopaminergiche o glutamatergiche.
Nulla di tutto ciò è dimostrato negli esseri umani. Questo è il limite fondamentale che va enunciato chiaramente, perché la divulgazione sui funghi psilocibini tende all'eccesso in entrambe le direzioni: verso la demonizzazione o verso l'entusiasmo acritico. Le prove attuali per l'effetto entourage nei funghi sono indirette, basate su osservazioni naturalistiche, resoconti aneddotici e alcuni modelli animali. Finché non esisteranno trial clinici controllati che confrontino direttamente il fungo intero con la psilocibina isolata — con una rigorosa standardizzazione del contenuto totale di alcaloidi — qualsiasi affermazione sulla superiorità terapeutica del fungo intero deve essere trattata come un'ipotesi promettente, non come un fatto consolidato.
Ma formulare correttamente l'ipotesi è altrettanto importante. Un trial clinico che volesse valutare l'effetto entourage avrebbe bisogno di almeno quattro bracci: psilocibina pura, psilocibina più baeocistina, psilocibina più aeruginascina ed estratto standardizzato di fungo intero. Le variabili di risultato principali dovrebbero includere non solo scale di depressione o ansia, ma misure della qualità dell'esperienza, incidenza di episodi avversi e, se possibile, biomarcatori di neuroplasticità. Quel trial non esiste ancora. Progettarlo è una delle sfide metodologiche più interessanti che la psicofarmacologia abbia davanti a sé.
Se l'effetto entourage si rivelasse clinicamente rilevante, le implicazioni regolatorie sarebbero considerevoli: potrebbe giustificare percorsi di approvazione per estratti standardizzati di origine botanica, sotto modelli simili a quelli già esistenti per il Sativex (cannabis) o l'Epidiolex (cannabidiolo). Alcuni stati degli USA che stanno regolamentando l'uso terapeutico dei funghi — l'Oregon implementa il suo quadro regolatorio dal 2023, con più di mille sessioni facilitate registrate nel primo trimestre del 2025 secondo Psychedelic Alpha — lavorano di default con il fungo intero, il che rende i loro programmi fonti di dati osservazionali di enorme interesse per questa domanda.
Equivalenze di dose tra fungo essiccato e composto isolato
Qualsiasi discussione sugli alcaloidi psilocibini è incompleta senza affrontare il dosaggio, sebbene questo sia anche il terreno in cui la variabilità degli alcaloidi ha le conseguenze più dirette.
La tabella seguente utilizza il P. cubensis standard — tra lo 0,6% e lo 0,7% di alcaloidi totali in peso secco — come riferimento, che è lo standard de facto nella ricerca clinica. Le dosi di psilocibina pura corrispondono agli intervalli utilizzati nei principali trial terapeutici registrati.
| Livello | Psilocibina pura | Fungo essiccato (P. cubensis standard) | Durata | Effetti caratteristici |
|---|---|---|---|---|
| Microdose | 0,5 – 3 mg | 0,05 – 0,3 g | 4–6 h (sottile) | Nessuna percezione alterata. Miglioramenti riportati in concentrazione, umore e connessione sociale. Prove miste nei trial controllati. |
| Dose soglia | 3 – 8 mg | 0,5 – 1,0 g | 3–5 h | Lieve alterazione percettiva. Colori più saturi, sensibilità emotiva aumentata. |
| Dose bassa | 8 – 15 mg | 1,0 – 1,5 g | 4–6 h | Lievi alterazioni visive, introspezione, emozioni ampliate. |
| Dose media | 15 – 25 mg | 1,5 – 3,5 g | 4–7 h | Piena esperienza psichedelica. Distorsioni visive, pensiero non lineare, alterazione del senso del tempo. |
| Dose alta | 25 – 40 mg | 3,5 – 5,0 g | 5–8 h | Dissoluzione dell'ego. Esperienze di tipo mistico. I trial terapeutici più efficaci utilizzano questo intervallo, con accompagnamento psicologico strutturato. |
| Dose eroica* | > 40 mg | > 5,0 g | 6–10 h | Perdita di riferimento temporale e personale. L'intervallo a più alto rischio senza supporto professionale. |
*Termine coniato da Terence McKenna. Usato qui come riferimento culturale consolidato, non come raccomandazione.
L'avvertimento che merita di stare al centro di questa tabella, non a margine: se si utilizzano ceppi selezionati per la loro alta potenza — Penis Envy, Albino A+, i nuovi ibridi selettivi del 2025 — o specie selvatiche come P. azurescens o P. semilanceata, la stessa quantità in grammi può contenere tra due e cinque volte più alcaloidi. L'errore di non calibrare in base alla potenza reale è la causa più documentata di esperienze involontariamente travolgenti in contesti non terapeutici.
Biosintesi eterologa, nuove specie e psychoplastogens
La stessa via biosintetica che spiega la diversità chimica del fungo è anche quella che permette di replicarla in laboratorio.
Produrre ciò che la natura sintetizza
La conoscenza completa della via biosintetica della psilocibina ha aperto una possibilità che vent'anni fa sembrava remota: produrla in modo controllato in microrganismi. Gruppi accademici negli USA e in Germania hanno prodotto con successo psilocibina in Saccharomyces cerevisiae — il lievito della birra — e in Escherichia coli geneticamente modificati. La produzione farmaceutica su larga scala è tecnicamente fattibile.
Ancora più significativo per la ricerca sull'entourage: la biosintesi eterologa permette di produrre selettivamente alcaloidi individuali — baeocistina, aeruginascina — che oggi sono estremamente difficili da isolare in quantità sufficienti dal fungo naturale. Questo potrebbe sbloccare i trial clinici comparativi di cui l'ipotesi dell'entourage ha bisogno per essere valutata.
La diversità alcaloide che non abbiamo ancora esplorato
Delle circa 200 specie di Psilocybe riconosciute tassonomicamente, la caratterizzazione chimica completa è stata effettuata solo su una piccola frazione. Le specie delle regioni tropicali, dell'Africa subsahariana o del Sud-Est asiatico sono praticamente sconosciute dal punto di vista biochimico. La recentemente descritta Psilocybe maluti del Sudafrica potrebbe contenere alcaloidi non ancora descritti. L'analisi genomica comparativa — cercare nei genomi di funghi sequenziati i geni omologhi al cluster psi — è la strategia più promettente per mappare quella diversità senza dover coltivare e analizzare ogni specie individualmente.
Separare l'effetto terapeutico da quello psicoattivo
La frontiera più audace della psicofarmacologia psichedelica non è migliorare la psilocibina, ma sostituirla. Aziende come Delix Therapeutics stanno sviluppando composti denominati psychoplastogens: molecole che riproducono gli effetti neuroplastici della psilocina — la formazione di nuove sinapsi, la riattivazione dei periodi sensibili della plasticità neuronale — senza produrre l'esperienza soggettiva di alto livello. Se questa strategia funziona, otterrebbe qualcosa di concettualmente senza precedenti: i benefici terapeutici del viaggio senza il viaggio. Questo ridurrebbe i costi clinici — l'accompagnamento terapeutico di otto ore è la componente più costosa dei protocolli attuali — e aprirebbe la porta a trattamenti ambulatoriali.
I critici sottolineano che potrebbe anche perdere parte del meccanismo terapeutico: ci sono prove crescenti che la profondità dell'esperienza mistica durante la sessione è un predittore indipendente dei risultati terapeutici. Se si elimina l'esperienza, si elimina anche parte dell'effetto? La risposta ha importanza clinica, e al momento non ce l'abbiamo.
Una molecola dominante, una complessità irrisolta
La chimica alcaloide dei funghi psilocibini è, allo stesso tempo, più semplice e più complessa di quanto venga solitamente presentata.
Più semplice perché esiste un composto dominante — la psilocibina, o più precisamente il suo metabolita attivo la psilocina — la cui farmacologia di base è ragionevolmente ben caratterizzata. Sappiamo come raggiunge il cervello, quali recettori attiva, quali regioni modula e, in linea di massima, perché questo produce gli effetti che produce.
Più complessa perché ogni alcaloide aggiuntivo aggiunge sfumature che potrebbero essere irrilevanti o potrebbero essere decisive — e non lo sappiamo ancora. Perché lo stesso fungo produce una composizione diversa a seconda della specie, del ceppo, del substrato, del momento della raccolta e delle condizioni di conservazione. Perché due organismi senza relazione diretta sono giunti, attraverso vie biochimiche diverse, a sintetizzare la stessa molecola, il che suggerisce che in essa vi sia qualcosa che la natura considera prezioso al di là del nostro utilizzo.
E perché, in ultima analisi, la domanda più importante che questa chimica pone non è di laboratorio ma clinica: quale formulazione — psilocibina pura, alcaloidi combinati, fungo intero standardizzato — produce i migliori risultati terapeutici con i minori rischi? Quella domanda ha una risposta sperimentale. Ciò che serve è progettare i trial che possano fornirla.
Riferimenti
- Fricke J. et al. (2017). Enzymatic synthesis of psilocybin. Angewandte Chemie International Edition, 56(40). — Descrizione completa della via biosintetica del cluster psi.
- Blei F. et al. (2020). Simultaneous production of psilocybin and β-carboline MAO inhibitors in 'magic mushrooms'. Chemistry – A European Journal. — Prima documentazione rigorosa delle β-carboline nei funghi psilocibini.
- Sherwood A.M. et al. (2020). Synthesis and Biological Evaluation of Tryptamine Derivatives. ACS Pharmacology & Translational Science. — Studio comparativo di baeocistina e psilocibina in modelli animali.
- Carhart-Harris R. et al. (2021). Trial of psilocybin versus escitalopram for depression. NEJM. — Trial clinico di riferimento; psilocibina sintetica pura versus antidepressivo standard.
- Heim C. et al. (2025). Convergent evolution of psilocybin biosynthesis in mushrooms. Nature Chemical Biology. — Documentazione dell'evoluzione indipendente in Psilocybe e Conocybe.
- Polito V. & Stevenson R.J. (2019). A systematic study of microdosing psychedelics. PLOS ONE. — Revisione sistematica delle prove sul microdosaggio.
- Gartz J. (1995). Magic Mushrooms Around the World. Jes Publications. — Prima caratterizzazione del profilo di Inocybe aeruginascens e proposta del ruolo dell'aeruginascina.
- Shin Y-J. et al. (2025). Psilocybin treatment extends cellular lifespan and improves survival of aged mice. NPJ Aging, 11. — Risultati preliminari sugli effetti a livello cellulare; in attesa di replica nell'uomo.
- Psychedelic Alpha (2025). Oregon Psilocybin Services Tracker Q1 2025. Recuperato da psychedelicalpha.com — Dati di implementazione del quadro regolatorio dell'Oregon.
Articoli in relazione
-
Psilocibina: cos'è, come agisce e quali effetti provoca
Pubblicato: 24/07/2025 12:21:12 -
Guida completa ai funghi psicoattivi
Pubblicato: 14/05/2025 22:19:54 -
L'enigma evolutivo della psilocibina
Pubblicato: 29/12/2025 12:04:40