Guia dos alcaloides dos cogumelos psilocibinos
- Por que dois cogumelos idênticos produzem experiências diferentes
- Como os cogumelos fabricam a psilocibina: origem molecular e evolução
- Os alcaloides do cogumelo, molécula a molécula
- Psilocibina: o pró-fármaco que viaja
- Psilocina: o que o cérebro recebe
- Baeocistina: a terceira em discórdia
- Norbaeocistina: a mais básica e a menos conhecida
- Aeruginascina: o alcaloide que muda o tom emocional
- Tabela comparativa de alcaloides dos cogumelos psilocibinos
- Uma nota sobre as β-carbolinas
- Potência por espécie e fatores que determinam a concentração alcaloide
- Variáveis que afetam a concentração alcaloide
- O efeito entourage como hipótese científica
- Equivalências de dose entre cogumelo seco e composto isolado
- Biossíntese heteróloga, novas espécies e psychoplastogens
- Produzir o que a natureza sintetiza
- A diversidade alcaloide que ainda não explorámos
- Separar o efeito terapêutico do psicoativo
- Uma molécula dominante, uma complexidade por resolver
- Referências
Por que dois cogumelos idênticos produzem experiências diferentes
Imagine que tem à sua frente duas amostras de cogumelo seco. Analisa-as em laboratório: mesmo teor de psilocibina, mesmo peso, mesma espécie. Administra-as a dois voluntários com o mesmo set and setting, a mesma preparação, o mesmo acompanhamento terapêutico. E os resultados são diferentes: um descreve uma experiência marcadamente ansiosa, o outro fala de euforia e abertura emocional sustentada.
Como é possível?
Durante décadas, a resposta convencional foi: «variáveis psicológicas do sujeito». E sem dúvida o set —o estado mental prévio— é um fator determinante. Mas existe outra resposta que a ciência vem construindo em silêncio há anos, e que obriga a repensar como lemos o rótulo de um cogumelo: os cogumelos psilocibinos não contêm um único composto ativo. Contêm uma família de alcaloides que atuam em conjunto, e essa orquestração química pode ser tão responsável pelo perfil da experiência quanto a psicologia do consumidor.

Este guia decompõe essa família, molécula a molécula, porque o que os ensaios clínicos estão a administrar —psilocibina sintética pura— é uma versão deliberadamente simplificada do que o cogumelo contém.
Como os cogumelos fabricam a psilocibina: origem molecular e evolução
Antes de falar de efeitos, convém entender de onde vêm estes compostos e por que razão um cogumelo os produz.
Os alcaloides psicoativos dos cogumelos psilocibinos são derivados do triptofano, um dos vinte aminoácidos essenciais que os organismos vivos utilizam para construir proteínas. Estruturalmente, todos partilham um núcleo indólico —o mesmo esqueleto molecular da serotonina, o principal neurotransmissor do humor— e é esta similitude estrutural que lhes permite interagir com os recetores cerebrais concebidos para a serotonina. São, em sentido literal, moléculas que o cérebro confunde com a sua própria linguagem interna.
A maquinaria biossintética que fabrica estas moléculas foi descrita em detalhe em 2017 por Fricke et al. em Angewandte Chemie: uma cadeia de quatro enzimas codificadas pelo cluster génico denominado psi, que transforma o triptofano em psilocibina em quatro etapas sucessivas. Cada enzima tem uma função específica: PsiD descarboxila o triptofano, PsiK adiciona o grupo fosfato, PsiM introduz os grupos metilo, e PsiH realiza a hidroxilação final. É um processo modular, elegante na sua lógica, que a biotecnologia já reproduziu em leveduras e bactérias de laboratório.
Mas a descoberta mais desconcertante sobre esta via biossintética chegou em 2025, num estudo publicado na Nature Chemical Biology por Heim et al.: os cogumelos do género Psilocybe e os do género Conocybe —duas linhagens evolutivamente distantes no reino fungi— desenvolveram a capacidade de sintetizar psilocibina de forma completamente independente. Não herdaram as mesmas enzimas de um ancestral comum: inventaram enzimas diferentes que realizam as mesmas transformações químicas para chegar ao mesmo produto final.
Isto denomina-se evolução convergente, e em bioquímica é relativamente raro. Que ocorra com uma molécula tão específica e farmacologicamente ativa como a psilocibina sugere que existe uma pressão seletiva poderosa que favorece a sua síntese. A hipótese mais difundida é que serve como defesa contra predadores ou parasitas, embora continue a ser uma área de investigação ativa. O que é inegável é o dado em si: dois organismos sem relação ancestral direta «descobriram», separadamente, a mesma solução química. Em termos de complexidade bioquímica, é uma descoberta da mesma família conceptual que o olho do polvo e o olho humano. A vida, quando precisa de algo, tende a encontrá-lo por múltiplos caminhos.
O enigma evolutivo da psilocibina
A psilocibina não pertence a um único fungo. Aparece em espécies separadas por milhões de anos de evolução. Este artigo explora como a biologia encontrou (e compartilhou) a mesma solução repetidamente.
Read moreOs alcaloides do cogumelo, molécula a molécula
Psilocibina: o pró-fármaco que viaja
C₁₂H₁₇N₂O₄P · 4-fosforilox-N,N-dimetiltriptamina · 4-PO-DMT
A psilocibina é o alcaloide mais abundante e o mais estável da família. À temperatura ambiente apresenta-se como um sólido cristalino branco que, na ausência de humidade extrema e luz direta, mantém entre 90 e 95% da sua atividade durante um a dois anos.
Mas a psilocibina, por si mesma, não faz nada no cérebro.
É o que os farmacologistas chamam um pró-fármaco: uma molécula inativa concebida para ser convertida na sua forma ativa pelo metabolismo do organismo recetor. Quando ingerida por via oral, a psilocibina é absorvida no trato gastrointestinal e chega ao fígado, onde as fosfatases alcalinas eliminam o grupo fosfato e libertam psilocina. Este processo, que demora entre vinte e sessenta minutos, é responsável pelo início relativamente lento dos efeitos em comparação com outras substâncias psicoativas. A biodisponibilidade oral oscila entre 52% e 74% segundo estudos de farmacocinética revisados nos últimos anos.
A função do grupo fosfato não é meramente inconveniente: torna a molécula mais polar, mais solúvel em água e mais estável. A psilocibina é, de certo modo, um sistema de transporte inteligente que protege a psilocina da degradação até chegar ao local onde precisa de atuar.
Psilocina: o que o cérebro recebe
C₁₂H₁₆N₂O · 4-hidroxi-N,N-dimetiltriptamina · 4-HO-DMT
A psilocina é o composto que realmente ocupa os recetores cerebrais. Sem o grupo fosfato que a encadeia na psilocibina, é diretamente ativa e atua mais rapidamente. O inconveniente desta liberdade química é a instabilidade: na presença de oxigénio oxida-se rapidamente, adquirindo tons castanhos ou negros. É este processo que explica o famoso azulamento dos cogumelos.

O azul merece ser bem explicado porque é provavelmente o fenómeno visual mais conhecido destes cogumelos e durante décadas foi interpretado de forma imprecisa. Quando se corta ou pressiona um cogumelo psilocibino, a psilocina libertada do tecido entra em contacto com o oxigénio do ar e oxida-se formando quinonas de cor azul índigo. Este mecanismo foi caracterizado com precisão pela primeira vez em 2020 pela equipa de Dirk Hoffmeister na Universidade de Jena: os compostos resultantes são quimicamente distintos da psilocina e não têm atividade psicoativa conhecida. Mas a sua presença é o indicador visual mais fiável de que o cogumelo contém alcaloides ativos. A intensidade do azulamento não é proporcional à potência, mas a sua ausência quase sempre indica ausência de psilocina.
No cérebro, a psilocina atua principalmente como agonista dos recetores de serotonina tipo 2A (5-HT₂A), que se encontram em alta densidade na camada V do córtex pré-frontal e em regiões límbicas. Mas a farmacologia da psilocina é mais promíscua do que esse título sugere: apresenta afinidade também pelos subtipos 5-HT₁A, 5-HT₂C, 5-HT₆ e 5-HT₇, assim como por recetores dopaminérgicos (D₂, D₃) e adrenérgicos (α₂). Esta rede de interações contribui para a riqueza e variabilidade do perfil de efeitos: não é que o cogumelo prima um único botão neuronal, mas que afina um instrumento complexo.
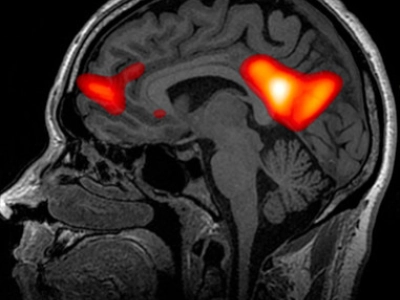
Os estudos de neuroimagem documentaram dois fenómenos simultâneos sob psilocina que se revelam especialmente esclarecedores. Por um lado, existe uma hiperconectividade entre regiões cerebrais que normalmente não comunicam entre si: o córtex visual fala com o auditivo, o sensorial com o motor, o lobo temporal com o frontal. Por outro, produz-se uma supressão marcada da Rede Neuronal por Defeito —Default Mode Network ou DMN—, o circuito que gere a narrativa do eu, o pensamento ruminativo e a identidade pessoal. A DMN é, num sentido muito concreto, a rede que mantém a história que contamos a nós mesmos sobre quem somos. A sua inibição sob psilocina correlaciona-se diretamente com a experiência subjetiva de dissolução do ego, e também —isto é o que é clinicamente relevante— com a magnitude do efeito antidepressivo observado nos ensaios terapêuticos. Este fenómeno é aprofundado na análise sobre as aplicações clínicas da psilocibina.
Mais novas conexões, menos controlo do eu habitual. Esse duplo mecanismo é a base neurobiológica tanto das experiências místicas como do efeito antidepressivo.
Baeocistina: a terceira em discórdia
C₁₁H₁₅N₂O₄P · 4-fosforilox-N-metiltriptamina
A baeocistina é estruturalmente a versão mono-metilada da psilocibina: uma única diferença química que a torna o terceiro alcaloide mais estudado da família. Foi descrita pela primeira vez em 1968 por Repke et al. em Psilocybe baeocystis, a espécie que lhe dá o nome, e desde então permaneceu numa espécie de limbo científico: demasiado presente para ser ignorada, demasiado pouco estudada para ser bem caracterizada.
Em algumas espécies, a baeocistina pode atingir concentrações comparáveis às da psilocibina. P. baeocystis pode ter entre 0,10% e 0,18% em peso seco; P. semilanceata, a conhecida «cabeça de gnomo» dos prados europeus, chega a 0,42% em algumas análises. Não são quantidades vestigiais.
Mas o que faz, exatamente? Esta é a pergunta à qual a literatura científica responde com uma honestidade que merece ser transmitida sem suavizar: não sabemos com certeza. Os estudos em roedores sugerem que produz efeitos psicoativos leves em doses equivalentes. Um estudo controlado de 2020 (Sherwood et al. em ACS Pharmacology & Translational Science) não encontrou diferenças estatisticamente significativas entre psilocibina isolada e psilocibina mais baeocistina em modelos de comportamento animal. Mas um resultado negativo em ratos não descarta um efeito sinérgico em humanos. A farmacologia do contexto —como uma molécula modifica a resposta a outra— é um dos territórios mais difíceis de estudar em psicofarmacologia, e os modelos animais têm limites claros quando o objeto de estudo envolve experiência subjetiva.
Norbaeocistina: a mais básica e a menos conhecida
C₁₀H₁₃N₂O₄P · 4-fosforiloxitriptamina
A norbaeocistina é a forma mais básica do esqueleto alcaloide psilocibino: sem qualquer grupo metilo sobre o azoto. As suas concentrações nos cogumelos são habitualmente as mais baixas da família, raramente acima de 0,05% em peso seco. A sua escassa lipossolubilidade —a propriedade que permite às moléculas atravessar membranas celulares, incluindo a barreira hematoencefálica— sugere uma penetração cerebral direta limitada.
O que não exclui um papel como precursor metabólico: os cogumelos poderiam utilizá-la como ponto de partida para sintetizar os outros alcaloides, o que significaria que a sua concentração é inversamente proporcional à eficiência biossintética do organismo. Existe também a possibilidade de atuar como modulador alostérico —uma molécula que não ativa diretamente um recetor mas altera a forma como outros compostos o fazem—, embora esta hipótese não disponha ainda de evidência direta.
Aeruginascina: o alcaloide que muda o tom emocional
C₁₂H₁₉N₂O₄P · N,N,N-trimetil-4-fosforiloxitriptamina
A aeruginascina merece atenção especial, porque é o composto que mais diretamente questiona o modelo simplificado de «a psilocibina faz tudo».
Foi identificada em 1985 em Inocybe aeruginascens, uma espécie de aspeto modesto e distribuição principalmente europeia que durante muito tempo foi classificada como não psicoativa —ou perigosamente tóxica— até que as análises químicas revelaram que contém níveis de psilocibina comparáveis aos de espécies de Psilocybe. O que chamou a atenção dos investigadores foi a discrepância entre o conteúdo alcaloide e os efeitos relatados: quem consumia I. aeruginascens —em muitos casos acidentalmente, confundindo-a com cogumelos comestíveis— descrevia invariavelmente uma experiência marcadamente eufórica, com ausência quase total de ansiedade e náuseas.
O investigador alemão Jochen Gartz foi o primeiro a propor, nos anos noventa, que a responsável por esse perfil diferencial era a aeruginascina: um composto que, ao contrário de todos os outros alcaloides psilocibinos, não atua como agonista do recetor 5-HT₂A mas como antagonista do recetor 5-HT₃.
O recetor 5-HT₃ é o único recetor serotoninérgico ionotrópico —atua como um canal iónico, não como um recetor acoplado a proteínas G— e está implicado na mediação das náuseas, dos vómitos e de certos aspetos do processamento emocional, especialmente a ansiedade antecipatória. Os antagonistas do 5-HT₃ são fármacos amplamente utilizados em oncologia precisamente para reduzir as náuseas induzidas pela quimioterapia. A hipótese de Gartz —que a aeruginascina modifica o perfil da viagem porque bloqueia este recetor— tem uma coerência farmacológica real, embora a evidência direta em humanos continue a ser observacional.
A implicação terapêutica é imediata: se a aeruginascina reduz a probabilidade de experiências adversas através do bloqueio do 5-HT₃, poderia ser um componente de grande valor no desenho de protocolos terapêuticos. Os ensaios atuais da Compass Pathways, MAPS e outros grupos trabalham exclusivamente com psilocibina sintética pura. Não há aeruginascina. Esta exclusão é metodologicamente compreensível —estudar um composto isolado é metodologicamente mais simples— mas significa que não sabemos se a psilocibina pura é a formulação ótima para uso terapêutico.
Aplicações terapêuticas da psilocibina
A psilocibina passou de uma droga proibida a uma ferramenta clínica promissora. Exploramos como ela redefine o tratamento de distúrbios como depressão, ansiedade e vícios.
Read moreTabela comparativa de alcaloides dos cogumelos psilocibinos
A família completa, de relance:
| Alcaloide | Fórmula | Concentração típica (% PS) | Recetor principal | Função proposta |
|---|---|---|---|---|
| Psilocibina | C₁₂H₁₇N₂O₄P | 0,1 – 1,0 | 5-HT₂A (pró-fármaco) | Alcaloide central. Reservatório de psilocina. Ação psicodélica principal. |
| Psilocina | C₁₂H₁₆N₂O | 0,01 – 0,6 | 5-HT₂A (agonista direto) | Metabolito ativo real. Início mais rápido quando está livre. |
| Baeocistina | C₁₁H₁₅N₂O₄P | 0,01 – 0,5 | 5-HT₂A (leve) | Modulador proposto. Alta variabilidade entre espécies. |
| Norbaeocistina | C₁₀H₁₃N₂O₄P | Vestígios < 0,05 | Parcialmente desconhecido | Possível precursor ou modulador alostérico. |
| Aeruginascina | C₁₂H₁₉N₂O₄P | 0 – 0,5 (variável por espécie) | 5-HT₃ (antagonista) | Bloqueia náuseas. Modula o tom emocional. Associada a experiências eufóricas. |
| β-Carbolinas | Diversas | Vestígios | IMAO leve | Possível extensão do efeito por inibição do metabolismo hepático. |
| Fenetilaminas | Diversas | Vestígios | Dopaminérgico / adrenérgico | Energizantes. Raramente quantificadas. |
Concentrações expressas em percentagem em peso seco (% PS), convenção padrão na literatura analítica.
Uma nota sobre as β-carbolinas
As β-carbolinas —harmina, harmalina, tetrahidroharmina— são inibidores da monoaminoxidase (IMAO) que se encontram em concentrações vestigiais em alguns cogumelos psilocibinos, documentadas no estudo de Blei et al. (2020) em Chemistry – A European Journal. A sua presença no cogumelo suscita comparações imediatas com a ayahuasca, que utiliza plantas ricas em β-carbolinas precisamente para inibir a degradação hepática do DMT. Nos cogumelos, porém, as concentrações detetadas são geralmente demasiado baixas para produzir um efeito IMAO clinicamente significativo por si só. Poderiam ser farmacologicamente irrelevantes na maioria das circunstâncias, ou poderiam ter um efeito potenciador subtil que os estudos atuais não têm resolução suficiente para detetar.
Potência por espécie e fatores que determinam a concentração alcaloide
A distribuição de alcaloides não é uniforme no género Psilocybe. As aproximadamente 200 espécies reconhecidas exibem perfis bioquímicos distintos, e essas diferenças têm consequências reais.
| Espécie | Psilocibina (% PS) | Psilocina (% PS) | Baeocistina (% PS) | Observações |
|---|---|---|---|---|
| P. cubensis | 0,14 – 0,42 | 0,01 – 0,05 | 0,02 – 0,18 | A mais cultivada. Alta variabilidade entre estirpes. Referência de facto em investigação clínica. |
| P. semilanceata | 0,60 – 1,28 | < 0,01 | 0,03 – 0,42 | A mais potente da Europa. Quase toda a potência em psilocibina: início lento, perfil estável. |
| P. azurescens | 1,00 – 1,78 | 0,38 – 0,50 | 0,04 – 0,18 | Potência máxima documentada no género. Psilocina elevada: início rápido, intensidade elevada. Associada a paralisia temporária reversível em alguns consumidores (wood lovers paralysis). |
| P. cyanescens | 0,85 – 1,50 | 0,15 – 0,30 | 0,03 – 0,10 | Muito disseminada em climas oceânicos. Efeito físico intenso devido à psilocina elevada. |
| P. tampanensis | 0,31 – 0,68 | < 0,02 | 0,02 – 0,10 | Produz esclerócios (trufas mágicas). Perfil suave e introspetivo. |
| P. mexicana | 0,17 – 0,25 | 0,01 – 0,03 | 0,01 – 0,03 | Uso ritual mesoamericano documentado durante séculos. Base histórica da investigação moderna. |
| P. baeocystis | 0,60 – 0,85 | 0,10 – 0,14 | 0,10 – 0,18 | Baeocistina elevada. Perfil diferencial atribuído à sua composição. Espécie de interesse para a investigação do efeito entourage. |
| P. subtropicalis (híbrido seletivo 2025) |
até 5,0 (dado não replicado) |
variável | sem dados | Estirpe desenvolvida mediante hibridação seletiva assistida por sequenciação genómica. Sem dados clínicos estandardizados. |
Os valores são intervalos representativos baseados na síntese de múltiplos estudos analíticos publicados entre 2010 e 2025, utilizando metodologias HPLC, GC-MS e UPLC. A variabilidade dentro de cada espécie pode ser tão elevada quanto a variabilidade entre espécies.
Existem dois padrões que merecem análise. O primeiro é uma correlação inversa entre facilidade de cultivo e potência: as espécies mais manejáveis para cultivar em condições controladas, como P. cubensis, são sistematicamente as menos potentes. As mais potentes —P. azurescens, P. cyanescens— requerem condições de cultivo ao ar livre e são mais difíceis de estandardizar, o que cria um paradoxo para a investigação: as espécies mais relevantes terapeuticamente poderiam ser as mais difíceis de produzir com a consistência que os ensaios clínicos exigem.
O segundo padrão é a diferença no rácio psilocibina/psilocina. P. semilanceata tem quase toda a sua potência armazenada em psilocibina —que deve ser convertida em psilocina antes de atuar—, o que produz um perfil de início lento e planalto estável. P. azurescens tem níveis excecionalmente elevados de psilocina livre, que atua diretamente: início mais rápido, intensidade mais abrupta. Dois cogumelos com potência total semelhante podem sentir-se radicalmente diferentes por este motivo.
Variáveis que afetam a concentração alcaloide
Genética: É o fator dominante. Dentro da mesma espécie, estirpes diferentes podem variar o seu conteúdo em psilocibina até um fator de quatro ou cinco. A estirpe Golden Teacher de P. cubensis produz consistentemente menos alcaloides do que a Penis Envy, apesar de serem a mesma espécie. Em 2025, grupos de cultivadores que combinam sequenciação genómica com hibridação de linhagens distantes produziram estirpes com até 5% de alcaloides totais em peso seco, face ao 0,5-1% típico do P. cubensis padrão. Isto representa um salto de potência que a maioria dos guias de dosagem disponíveis não contempla.
Substrato: Fator secundário mas real. Os cogumelos cultivados em grãos de centeio ou arroz tendem a produzir corpos frutíferos com maior concentração de alcaloides do que os cultivados em palha ou coco, presumivelmente porque a disponibilidade de triptofano como precursor biossintético varia com o substrato nutricional.
Fase de desenvolvimento: A concentração de psilocibina atinge o seu máximo pouco antes de o véu que cobre as lamelas se romper. Após a rotura do véu e o início da esporulação, a concentração pode descer de forma significativa em questão de horas. O momento da colheita importa mais do que habitualmente se reconhece.
Conservação: A psilocibina, em material seco armazenado corretamente —escuridão, temperatura estável, ausência de humidade—, mantém 90-95% da sua atividade durante doze a vinte e quatro meses. A psilocina degrada-se com maior rapidez por oxidação. O escurecimento progressivo do material armazenado é um sinal de perda de alcaloides ativos.
O efeito entourage como hipótese científica
O conceito de efeito entourage foi cunhado no âmbito da cannabis para descrever a sinergia entre canabinoides e terpenos. Nos últimos anos começou a aplicar-se aos cogumelos psilocibinos, não sem cautela, porque a evidência disponível é qualitativamente diferente da que existe para a cannabis.
A pergunta central é: o cogumelo completo produz efeitos diferentes —quantitativa ou qualitativamente— da psilocibina isolada, a doses iguais de psilocibina?
Os mecanismos propostos são farmacologicamente plausíveis. A baeocistina poderia atuar como agonista parcial no 5-HT₂A, modulando a resposta máxima à psilocina mediante competição pelo mesmo recetor —um fenómeno conhecido em farmacologia como efeito teto competitivo. A aeruginascina poderia suavizar o componente ansioso bloqueando o 5-HT₃, como já se discutiu. As β-carbolinas poderiam estender a janela de exposição ativa ao reduzir o clearance hepático da psilocina, prolongando o efeito sem aumentar a dose. E poderiam existir compostos ainda não identificados que influenciem as vias dopaminérgicas ou glutamatérgicas.
Nada disto está demonstrado em humanos. Esta é a limitação fundamental que é necessário enunciar com clareza, porque a divulgação sobre cogumelos psilocibinos tende ao excesso em ambas as direções: para a demonização ou para o entusiasmo acrítico. A evidência atual para o efeito entourage em cogumelos é indireta, baseada em observações naturalistas, relatos anedóticos e alguns modelos animais. Até que existam ensaios clínicos controlados que comparem diretamente o cogumelo completo com a psilocibina isolada —com estandardização rigorosa do conteúdo alcaloide total— qualquer afirmação sobre superioridade terapêutica do cogumelo completo deve ser tratada como hipótese promissora, não como facto estabelecido.
Mas formular corretamente a hipótese também importa. Um ensaio clínico que pretendesse avaliar o efeito entourage necessitaria de pelo menos quatro braços: psilocibina pura, psilocibina mais baeocistina, psilocibina mais aeruginascina, e extrato estandardizado de cogumelo completo. As variáveis de resultados principais deveriam incluir não apenas escalas de depressão ou ansiedade, mas medidas da qualidade da experiência, incidência de episódios adversos e, se possível, biomarcadores de neuroplasticidade. Esse ensaio ainda não existe. Desenhá-lo é um dos desafios metodológicos mais interessantes que a psicofarmacologia tem pela frente.
Se o efeito entourage se revelar clinicamente relevante, as implicações regulatórias são consideráveis: poderia justificar vias de aprovação para extratos estandardizados de origem botânica, sob modelos semelhantes aos que já existem para o Sativex (cannabis) ou o Epidiolex (cannabidiol). Alguns estados dos EUA que estão a regular o uso terapêutico de cogumelos —o Oregon implementa o seu quadro regulatório desde 2023, com mais de mil sessões facilitadas registadas no primeiro trimestre de 2025 segundo a Psychedelic Alpha— trabalham com o cogumelo completo por defeito, o que torna os seus programas em fontes de dados observacionais de enorme interesse para esta questão.
Equivalências de dose entre cogumelo seco e composto isolado
Qualquer discussão sobre alcaloides psilocibinos fica incompleta sem abordar a dosagem, embora este seja também o terreno onde a variabilidade alcaloide tem as consequências mais diretas.
A tabela seguinte usa P. cubensis padrão —entre 0,6% e 0,7% de alcaloides totais em peso seco— como referência, que é o padrão de facto em investigação clínica. As doses de psilocibina pura correspondem aos intervalos utilizados nos principais ensaios terapêuticos registados.
| Nível | Psilocibina pura | Cogumelo seco (P. cubensis padrão) | Duração | Efeitos característicos |
|---|---|---|---|---|
| Microdose | 0,5 – 3 mg | 0,05 – 0,3 g | 4–6 h (subtil) | Sem perceção alterada. Melhorias relatadas no foco, estado de humor e conexão social. Evidência mista em ensaios controlados. |
| Dose limiar | 3 – 8 mg | 0,5 – 1,0 g | 3–5 h | Ligeira alteração percetual. Cores mais saturadas, sensibilidade emocional aumentada. |
| Dose baixa | 8 – 15 mg | 1,0 – 1,5 g | 4–6 h | Alterações visuais suaves, introspeção, emoções amplificadas. |
| Dose média | 15 – 25 mg | 1,5 – 3,5 g | 4–7 h | Experiência psicodélica plena. Distorções visuais, pensamento não linear, alteração do sentido do tempo. |
| Dose elevada | 25 – 40 mg | 3,5 – 5,0 g | 5–8 h | Dissolução do ego. Experiências de tipo místico. Os ensaios terapêuticos mais bem-sucedidos utilizam este intervalo, com acompanhamento psicológico estruturado. |
| Dose heróica* | > 40 mg | > 5,0 g | 6–10 h | Perda de referência temporal e pessoal. O intervalo de maior risco sem apoio profissional. |
*Termo cunhado por Terence McKenna. Utilizado aqui como referência cultural estabelecida, não como recomendação.
O aviso que merece estar no centro desta tabela, e não à margem: se forem utilizadas estirpes selecionadas pela sua elevada potência —Penis Envy, Albino A+, os novos híbridos seletivos de 2025— ou espécies silvestres como P. azurescens ou P. semilanceata, a mesma quantidade em gramas pode conter entre duas e cinco vezes mais alcaloides. O erro de não calibrar pela potência real é a causa mais documentada de experiências involuntariamente avassaladoras em contextos não terapêuticos.
Biossíntese heteróloga, novas espécies e psychoplastogens
A mesma via biossintética que explica a diversidade química do cogumelo é também a que permite replicá-la em laboratório.
Produzir o que a natureza sintetiza
O conhecimento completo da via biossintética da psilocibina abriu uma possibilidade que há vinte anos parecia remota: produzi-la de forma controlada em micro-organismos. Grupos académicos nos EUA e na Alemanha conseguiram produzir psilocibina em Saccharomyces cerevisiae —a levedura da cerveja— e em Escherichia coli geneticamente modificadas. A produção farmacêutica em grande escala é tecnicamente viável.
Mais significativo para a investigação do entourage: a biossíntese heteróloga permite produzir seletivamente alcaloides individuais —baeocistina, aeruginascina— que hoje são extremamente difíceis de isolar em quantidades suficientes do cogumelo natural. Isto poderia desbloquear os ensaios clínicos comparativos de que a hipótese do entourage necessita para ser avaliada.
A diversidade alcaloide que ainda não explorámos
Das aproximadamente 200 espécies de Psilocybe reconhecidas taxonomicamente, a caracterização química completa foi realizada apenas numa pequena fração. As espécies de regiões tropicais, de África subsaariana ou do Sudeste Asiático são praticamente desconhecidas do ponto de vista bioquímico. A recentemente descrita Psilocybe maluti da África do Sul poderia conter alcaloides ainda não descritos. A análise genómica comparativa —procurar nos genomas de fungos sequenciados os genes homólogos ao cluster psi— é a estratégia mais promissora para cartografar essa diversidade sem ter de cultivar e analisar cada espécie individualmente.
Separar o efeito terapêutico do psicoativo
A fronteira mais audaciosa da psicofarmacologia psicodélica não é melhorar a psilocibina, mas substituí-la. Empresas como a Delix Therapeutics estão a desenvolver compostos denominados psychoplastogens: moléculas que reproduzem os efeitos neuroplásticos da psilocina —a formação de novas sinapses, a reativação de períodos sensíveis da plasticidade neuronal— sem produzir a experiência subjetiva de alto nível. Se esta estratégia funcionar, conseguiria algo conceptualmente sem precedentes: os benefícios terapêuticos da viagem sem a viagem. Isto reduziria os custos clínicos —o acompanhamento terapêutico durante oito horas é o componente mais caro dos protocolos atuais— e abriria a porta a tratamentos em ambulatório.
Os críticos assinalam que poderia também perder parte do mecanismo terapêutico: há evidência crescente de que a profundidade da experiência mística durante a sessão é um preditor independente dos resultados terapêuticos. Se se elimina a experiência, elimina-se também parte do efeito? A resposta tem importância clínica, e atualmente não a temos.
Uma molécula dominante, uma complexidade por resolver
A química alcaloide dos cogumelos psilocibinos é, ao mesmo tempo, mais simples e mais complexa do que habitualmente se apresenta.
Mais simples porque existe um composto dominante —a psilocibina, ou mais precisamente o seu metabolito ativo a psilocina— cuja farmacologia básica está razoavelmente bem caracterizada. Sabemos como chega ao cérebro, que recetores ativa, que regiões modula e, em traços gerais, por que razão isso produz os efeitos que produz.
Mais complexa porque cada alcaloide adicional acrescenta nuances que poderiam ser irrelevantes ou poderiam ser decisivas —e ainda não sabemos qual. Porque o mesmo cogumelo produz uma composição diferente consoante a espécie, a estirpe, o substrato, o momento da colheita e as condições de conservação. Porque dois organismos sem relação direta chegaram, por vias bioquímicas distintas, a sintetizar a mesma molécula, o que sugere que há nela algo que a natureza considera valioso para além do uso que fazemos dela.
E porque, em última análise, a pergunta mais importante que esta química coloca não é de laboratório mas clínica: que formulação —psilocibina pura, alcaloides combinados, cogumelo completo estandardizado— produz os melhores resultados terapêuticos com os menores riscos? Essa pergunta tem resposta experimental. O que é necessário é desenhar os ensaios que a possam responder.
Referências
- Fricke J. et al. (2017). Enzymatic synthesis of psilocybin. Angewandte Chemie International Edition, 56(40). — Descrição completa da via biossintética do cluster psi.
- Blei F. et al. (2020). Simultaneous production of psilocybin and β-carboline MAO inhibitors in 'magic mushrooms'. Chemistry – A European Journal. — Primeira documentação rigorosa de β-carbolinas em cogumelos psilocibinos.
- Sherwood A.M. et al. (2020). Synthesis and Biological Evaluation of Tryptamine Derivatives. ACS Pharmacology & Translational Science. — Estudo comparativo de baeocistina e psilocibina em modelos animais.
- Carhart-Harris R. et al. (2021). Trial of psilocybin versus escitalopram for depression. NEJM. — Ensaio clínico de referência; psilocibina sintética pura versus antidepressivo padrão.
- Heim C. et al. (2025). Convergent evolution of psilocybin biosynthesis in mushrooms. Nature Chemical Biology. — Documentação da evolução independente em Psilocybe e Conocybe.
- Polito V. & Stevenson R.J. (2019). A systematic study of microdosing psychedelics. PLOS ONE. — Revisão sistemática de evidência em microdosagem.
- Gartz J. (1995). Magic Mushrooms Around the World. Jes Publications. — Primeira caracterização do perfil de Inocybe aeruginascens e proposta do papel da aeruginascina.
- Shin Y-J. et al. (2025). Psilocybin treatment extends cellular lifespan and improves survival of aged mice. NPJ Aging, 11. — Resultados preliminares sobre efeitos a nível celular; pendentes de replicação em humanos.
- Psychedelic Alpha (2025). Oregon Psilocybin Services Tracker Q1 2025. Obtido de psychedelicalpha.com — Dados de implementação do quadro regulatório do Oregon.
Artigos relacionados
-
Psilocibina: o que é, como atua e quais efeitos provoca
Publicado em: 2025-07-24 12:21:12 -
Guia completo dos cogumelos psicoactivos
Publicado em: 2025-05-14 22:19:54 -
O enigma evolutivo da psilocibina
Publicado em: 2025-12-29 12:04:40