Guía de alcaloides de los hongos psilocibios
- Por qué dos hongos idénticos producen experiencias distintas
- Cómo fabrican los hongos la psilocibina: origen molecular y evolución
- Los alcaloides del hongo, molécula a molécula
- Psilocibina: el profármaco que viaja
- Psilocina: lo que el cerebro recibe
- Baeocistina: el tercero en discordia
- Norbaeocistina: el más básico y el menos conocido
- Aeruginascina: el alcaloide que cambia el tono emocional
- Tabla comparativa de alcaloides de los hongos psilocibios
- Un apunte sobre las β-carbolinas
- Potencia por especie y factores que determinan la concentración alcaloide
- Variables que afectan a la concentración alcaloide
- El efecto entourage como hipótesis científica
- Equivalencias de dosis entre hongo seco y compuesto aislado
- Biosíntesis heteróloga, nuevas especies y psychoplastogens
- Producir lo que la naturaleza sintetiza
- La diversidad alcaloide que no hemos explorado
- Separar el efecto terapéutico del psicoactivo
- Una molécula dominante, una complejidad sin resolver
- Referencias
Por qué dos hongos idénticos producen experiencias distintas
Imagina que tienes delante dos muestras de hongo seco. Las analizas en laboratorio: mismo contenido de psilocibina, mismo peso, misma especie. Las administras a dos voluntarios con el mismo set and setting, la misma preparación, el mismo acompañamiento terapéutico. Y los resultados son distintos: uno describe una experiencia marcadamente ansiosa, el otro habla de euforia y apertura emocional sostenida.
¿Cómo es posible?
Durante décadas, la respuesta convencional fue: «variables psicológicas del sujeto». Y sin duda el set —el estado mental previo— es un factor determinante. Pero hay otra respuesta que la ciencia lleva años construyendo en silencio, y que obliga a repensar cómo leemos la etiqueta de un hongo: los hongos psilocibios no contienen un compuesto activo. Contienen una familia de alcaloides que actúan en concierto, y esa orquestación química puede ser tan responsable del perfil de la experiencia como la psicología del consumidor.

Esta guía descompone esa familia, molécula a molécula, porque lo que los ensayos clínicos están administrando —psilocibina sintética pura— es una versión deliberadamente simplificada de lo que el hongo contiene.
Cómo fabrican los hongos la psilocibina: origen molecular y evolución
Antes de hablar de efectos, conviene entender de dónde vienen estos compuestos y por qué un hongo los fabrica.
Los alcaloides psicoactivos de los hongos psilocibios son derivados del triptófano, uno de los veinte aminoácidos esenciales que los organismos vivos usan para construir proteínas. Estructuralmente, todos comparten un núcleo indólico —el mismo esqueleto molecular de la serotonina, el principal neurotransmisor del estado de ánimo— y es esta similitud estructural la que les permite interactuar con los receptores cerebrales diseñados para la serotonina. Son, en sentido literal, moléculas que el cerebro confunde con su propio lenguaje interno.
La maquinaria biosintética que fabrica estas moléculas fue descrita en detalle en 2017 por Fricke et al. en Angewandte Chemie: una cadena de cuatro enzimas codificadas por el clúster génico denominado psi, que transforma el triptófano en psilocibina mediante cuatro pasos sucesivos. Cada enzima tiene una función específica: PsiD descarboxila el triptófano, PsiK añade el grupo fosfato, PsiM introduce los grupos metilo, y PsiH realiza la hidroxilación final. Es un proceso modular, elegante en su lógica, que la biotecnología ya ha reproducido en levaduras y bacterias de laboratorio.
Pero el hallazgo más desconcertante sobre esta vía biosintética llegó en 2025, en un estudio publicado en Nature Chemical Biology por Heim et al.: los hongos del género Psilocybe y los del género Conocybe —dos linajes evolutivamente distantes dentro del reino fungi— desarrollaron la capacidad de sintetizar psilocibina de forma completamente independiente. No heredaron las mismas enzimas de un ancestro común: inventaron enzimas diferentes que realizan las mismas transformaciones químicas para llegar al mismo producto final.
Esto se denomina evolución convergente, y en bioquímica es relativamente raro. Que ocurra con una molécula tan específica y farmacológicamente activa como la psilocibina sugiere que hay una presión selectiva poderosa que favorece su síntesis. La hipótesis más extendida es que sirve como defensa contra depredadores o parásitos, aunque sigue siendo un área de investigación activa. Lo que es innegable es el dato en sí: dos organismos sin relación ancestral directa «descubrieron», por separado, la misma solución química. En términos de complejidad bioquímica, es un hallazgo de la misma familia conceptual que el ojo del pulpo y el ojo humano. La vida, cuando necesita algo, tiende a encontrarlo por múltiples caminos.
El enigma evolutivo de la psilocibina
La psilocibina no pertenece a un solo hongo. Aparece en especies separadas por millones de años de evolución. Este artículo explora cómo la biología encontró (y compartió) la misma solución una y otra vez.
Leer másLos alcaloides del hongo, molécula a molécula
Psilocibina: el profármaco que viaja
C₁₂H₁₇N₂O₄P · 4-fosforilox-N,N-dimetiltriptamina · 4-PO-DMT
La psilocibina es el alcaloide más abundante y el más estable de la familia. A temperatura ambiente se presenta como un sólido cristalino blanco que, en ausencia de humedad extrema y luz directa, mantiene entre el 90 y el 95% de su actividad durante uno o dos años.
Pero la psilocibina, por sí misma, no hace nada en el cerebro.
Es lo que los farmacólogos llaman un profármaco: una molécula inactiva diseñada para ser convertida en su forma activa por el metabolismo del organismo receptor. Cuando se ingiere por vía oral, la psilocibina es absorbida en el tracto gastrointestinal y llega al hígado, donde las fosfatasas alcalinas eliminan el grupo fosfato y liberan psilocina. Este proceso, que tarda entre veinte y sesenta minutos, es el responsable del inicio relativamente lento de los efectos comparado con otras sustancias psicoactivas. La biodisponibilidad oral oscila entre el 52% y el 74% según estudios de farmacocinética revisados en los últimos años.
La función del grupo fosfato no es meramente incómoda: hace la molécula más polar, más soluble en agua y más estable. La psilocibina es, en cierto modo, un sistema de transporte inteligente que protege a la psilocina de la degradación hasta que llega al lugar donde necesita actuar.
Psilocina: lo que el cerebro recibe
C₁₂H₁₆N₂O · 4-hidroxi-N,N-dimetiltriptamina · 4-HO-DMT
La psilocina es el compuesto que realmente ocupa los receptores cerebrales. Sin el grupo fosfato que la encadena en la psilocibina, es directamente activa y actúa más rápido. El inconveniente de esta libertad química es la inestabilidad: en presencia de oxígeno se oxida con rapidez, adquiriendo tonos pardos o negros. Es este proceso el que explica el famoso azulado de los hongos.

El azul, vale la pena explicarlo bien porque es probablemente el fenómeno visual más conocido de estos hongos y durante décadas se interpretó de forma imprecisa. Cuando se corta o presiona un hongo psilocibio, la psilocina liberada del tejido entra en contacto con el oxígeno del aire y se oxida formando quinonas de color azul índigo. Este mecanismo fue caracterizado con precisión por primera vez en 2020 por el equipo de Dirk Hoffmeister en la Universidad de Jena: los compuestos resultantes son químicamente distintos de la psilocina y no tienen actividad psicoactiva conocida. Pero su presencia es el indicador visual más fiable de que el hongo contiene alcaloides activos. La intensidad del azulado no es proporcional a la potencia, pero su ausencia casi siempre indica ausencia de psilocina.
En el cerebro, la psilocina actúa principalmente como agonista de los receptores de serotonina tipo 2A (5-HT₂A), que se encuentran en alta densidad en la capa V de la corteza prefrontal y en regiones límbicas. Pero la farmacología de la psilocina es más promiscua de lo que sugiere ese titular: muestra afinidad también por los subtipos 5-HT₁A, 5-HT₂C, 5-HT₆ y 5-HT₇, así como por receptores dopaminérgicos (D₂, D₃) y adrenérgicos (α₂). Esta red de interacciones contribuye a la riqueza y variabilidad del perfil de efectos: no es que el hongo pulse un único botón neuronal, sino que afina un instrumento complejo.
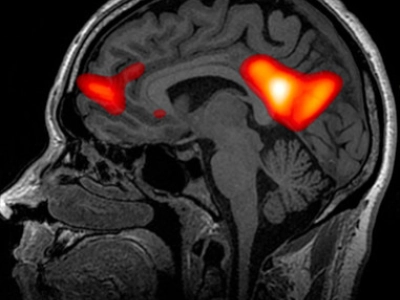
Los estudios de neuroimagen han documentado dos fenómenos simultáneos bajo psilocina que resultan especialmente iluminadores. Por un lado, hay una hiperconectividad entre regiones cerebrales que normalmente no se comunican entre sí: la corteza visual habla con la auditiva, la sensorial con la motora, el lóbulo temporal con el frontal. Por otro, se produce una supresión marcada de la Red Neuronal por Defecto —Default Mode Network o DMN—, el circuito que gestiona la narrativa del yo, el pensamiento rumiativo y la identidad personal. La DMN es, en un sentido muy concreto, la red que mantiene la historia que nos contamos sobre quiénes somos. Su inhibición bajo psilocina se correlaciona directamente con la experiencia subjetiva de disolución del ego, y también —esto es lo clínicamente relevante— con la magnitud del efecto antidepresivo observado en los ensayos terapéuticos. Este fenómeno se desarrolla en profundidad en el análisis sobre las aplicaciones clínicas de la psilocibina.
Más conexiones nuevas, menos control del yo habitual. Ese doble mecanismo es la base neurobiológica tanto de las experiencias místicas como del efecto antidepresivo.
Baeocistina: el tercero en discordia
C₁₁H₁₅N₂O₄P · 4-fosforilox-N-metiltriptamina
La baeocistina es estructuralmente la versión mono-metilada de la psilocibina: una sola diferencia química que la convierte en el tercer alcaloide más estudiado de la familia. Fue descrita por primera vez en 1968 por Repke et al. en Psilocybe baeocystis, la especie que le da nombre, y desde entonces ha permanecido en una especie de limbo científico: demasiado presente para ignorarla, demasiado poco estudiada para caracterizarla bien.
En algunas especies, la baeocistina puede alcanzar concentraciones comparables a la psilocibina. P. baeocystis puede tener entre un 0,10% y un 0,18% en peso seco; P. semilanceata, la conocida «cabeza de duende» de los prados europeos, llega a un 0,42% en algunos análisis. No son cantidades trazas.
¿Pero qué hace, exactamente? Esta es la pregunta que la literatura científica responde con una honestidad que merece ser transmitida sin suavizar: no lo sabemos con certeza. Los estudios en roedores sugieren que produce efectos psicoactivos leves a dosis equivalentes. Un estudio controlado de 2020 (Sherwood et al. en ACS Pharmacology & Translational Science) no encontró diferencias estadísticamente significativas entre psilocibina sola y psilocibina más baeocistina en modelos de comportamiento animal. Pero un resultado negativo en ratones no descarta un efecto sinérgico en humanos. La farmacología del contexto —cómo una molécula modifica la respuesta a otra— es uno de los territorios más difíciles de estudiar en psicofarmacología, y los modelos animales tienen límites claros cuando el objeto de estudio involucra experiencia subjetiva.
Norbaeocistina: el más básico y el menos conocido
C₁₀H₁₃N₂O₄P · 4-fosforiloxitriptamina
La norbaeocistina es la forma más básica del esqueleto alcaloide psilocibio: sin ningún grupo metilo sobre el nitrógeno. Sus concentraciones en los hongos son habitualmente las más bajas de la familia, raramente por encima del 0,05% en peso seco. Su escasa liposolubilidad —la propiedad que permite a las moléculas atravesar membranas celulares, incluyendo la barrera hematoencefálica— sugiere una penetración cerebral directa limitada.
Lo que no excluye un papel como precursor metabólico: los hongos podrían usarla como punto de partida para sintetizar los otros alcaloides, lo que significaría que su concentración es inversamente proporcional a la eficiencia biosintética del organismo. También existe la posibilidad de que actúe como modulador alostérico —una molécula que no activa directamente un receptor pero altera cómo otros compuestos lo hacen—, aunque esta hipótesis no cuenta aún con evidencia directa.
Aeruginascina: el alcaloide que cambia el tono emocional
C₁₂H₁₉N₂O₄P · N,N,N-trimetil-4-fosforiloxitriptamina
La aeruginascina merece atención especial, porque es el compuesto que más directamente cuestiona el modelo simplificado de «la psilocibina lo hace todo».
Fue identificada en 1985 en Inocybe aeruginascens, una especie de aspecto modesto y distribución principalmente europea que durante mucho tiempo estuvo clasificada como no psicoactiva —o peligrosamente tóxica— hasta que los análisis químicos revelaron que contiene niveles de psilocibina comparables a especies de Psilocybe. Lo que llamó la atención de los investigadores fue la discrepancia entre el contenido alcaloide y los efectos reportados: quienes consumían I. aeruginascens —en muchos casos de forma accidental, confundiéndola con setas comestibles— describían invariablemente una experiencia marcadamente eufórica, con ausencia casi total de ansiedad y náusea.
El investigador alemán Jochen Gartz fue el primero en proponer, en los años noventa, que la responsable de ese perfil diferencial era la aeruginascina: un compuesto que, a diferencia de todos los otros alcaloides psilocibios, no actúa como agonista del receptor 5-HT₂A sino como antagonista del receptor 5-HT₃.
El receptor 5-HT₃ es el único receptor serotoninérgico ionotrópico —actúa como un canal iónico, no como un receptor acoplado a proteínas G— y está implicado en la mediación de la náusea, el vómito y ciertos aspectos del procesamiento emocional, especialmente la ansiedad anticipatoria. Los antagonistas de 5-HT₃ son fármacos ampliamente utilizados en oncología precisamente para reducir las náuseas inducidas por quimioterapia. La hipótesis de Gartz —que la aeruginascina modifica el perfil del viaje porque bloquea este receptor— tiene una coherencia farmacológica real, aunque la evidencia directa en humanos sigue siendo observacional.
La implicación terapéutica es inmediata: si la aeruginascina reduce la probabilidad de experiencias adversas mediante el bloqueo de 5-HT₃, podría ser un componente de gran valor para el diseño de protocolos terapéuticos. Los ensayos actuales de Compass Pathways, MAPS y otros grupos trabajan exclusivamente con psilocibina sintética pura. No hay aeruginascina. Esta exclusión es metodológicamente comprensible —estudiar un compuesto aislado es metodológicamente más sencillo— pero significa que no sabemos si la psilocibina pura es la formulación óptima para uso terapéutico.
Aplicaciones terapéuticas de la psilocibina
La psilocibina ha pasado de ser una droga prohibida a una herramienta clínica prometedora. Exploramos cómo redefine el tratamiento de trastornos como la depresión, ansiedad y las adicciones.
Leer másTabla comparativa de alcaloides de los hongos psilocibios
La familia completa, de un vistazo:
| Alcaloide | Fórmula | Concentración típica (% PS) | Receptor principal | Función propuesta |
|---|---|---|---|---|
| Psilocibina | C₁₂H₁₇N₂O₄P | 0,1 – 1,0 | 5-HT₂A (profármaco) | Alcaloide central. Reservorio de psilocina. Acción psicodélica principal. |
| Psilocina | C₁₂H₁₆N₂O | 0,01 – 0,6 | 5-HT₂A (agonista directo) | Metabolito activo real. Inicio más rápido cuando está libre. |
| Baeocistina | C₁₁H₁₅N₂O₄P | 0,01 – 0,5 | 5-HT₂A (leve) | Modulador propuesto. Alta variabilidad entre especies. |
| Norbaeocistina | C₁₀H₁₃N₂O₄P | Trazas < 0,05 | Parcialmente desconocido | Posible precursor o modulador alostérico. |
| Aeruginascina | C₁₂H₁₉N₂O₄P | 0 – 0,5 (variable por especie) | 5-HT₃ (antagonista) | Bloquea náusea. Modula tono emocional. Vinculada a experiencias eufóricas. |
| β-Carbolinas | Diversas | Trazas | IMAO leve | Posible extensión del efecto por inhibición del metabolismo hepático. |
| Feniletilaminas | Diversas | Trazas | Dopaminérgico / adrenérgico | Energizantes. Raramente cuantificadas. |
Concentraciones expresadas en porcentaje en peso seco (% PS), convención estándar en la literatura analítica.
Un apunte sobre las β-carbolinas
Las β-carbolinas —harmina, harmalina, tetrahidroharmina— son inhibidores de la monoaminooxidasa (IMAO) que se encuentran en concentraciones trazas en algunos hongos psilocibios, documentadas en el estudio de Blei et al. (2020) en Chemistry – A European Journal. Su presencia en el hongo suscita comparaciones inmediatas con la ayahuasca, que utiliza plantas ricas en β-carbolinas precisamente para inhibir la degradación hepática del DMT. En los hongos, sin embargo, las concentraciones detectadas son generalmente demasiado bajas para producir un efecto IMAO clínicamente significativo por sí solas. Podrían ser farmacológicamente irrelevantes en la mayoría de las circunstancias, o podrían tener un efecto potenciador sutil que los estudios actuales no tienen resolución suficiente para detectar.
Potencia por especie y factores que determinan la concentración alcaloide
La distribución de alcaloides no es uniforme en el género Psilocybe. Las aproximadamente 200 especies reconocidas exhiben perfiles bioquímicos distintos, y esas diferencias tienen consecuencias reales.
| Especie | Psilocibina (% PS) | Psilocina (% PS) | Baeocistina (% PS) | Observaciones |
|---|---|---|---|---|
| P. cubensis | 0,14 – 0,42 | 0,01 – 0,05 | 0,02 – 0,18 | La más cultivada. Alta variabilidad entre cepas. Referencia de facto en investigación clínica. |
| P. semilanceata | 0,60 – 1,28 | < 0,01 | 0,03 – 0,42 | La más potente de Europa. Casi toda la potencia en psilocibina: inicio lento, perfil estable. |
| P. azurescens | 1,00 – 1,78 | 0,38 – 0,50 | 0,04 – 0,18 | Potencia máxima documentada en el género. Alta psilocina: inicio rápido, intensidad elevada. Asociada a parálisis temporal reversible en algunos consumidores (wood lovers paralysis). |
| P. cyanescens | 0,85 – 1,50 | 0,15 – 0,30 | 0,03 – 0,10 | Muy extendida en climas oceánicos. Efecto físico intenso por alta psilocina. |
| P. tampanensis | 0,31 – 0,68 | < 0,02 | 0,02 – 0,10 | Produce esclerocios (trufas mágicas). Perfil suave e introspectivo. |
| P. mexicana | 0,17 – 0,25 | 0,01 – 0,03 | 0,01 – 0,03 | Uso ritual mesoamericano documentado durante siglos. Base histórica de la investigación moderna. |
| P. baeocystis | 0,60 – 0,85 | 0,10 – 0,14 | 0,10 – 0,18 | Alta baeocistina. Perfil diferencial atribuido a su composición. Especie de interés para investigación del efecto entourage. |
| P. subtropicalis (híbrido selectivo 2025) |
hasta 5,0 (dato no replicado) |
variable | sin datos | Cepa desarrollada mediante hibridación selectiva asistida por secuenciación genómica. Sin datos clínicos estandarizados. |
Los valores son rangos representativos basados en la síntesis de múltiples estudios analíticos publicados entre 2010 y 2025, utilizando metodologías HPLC, GC-MS y UPLC. La variabilidad dentro de cada especie puede ser tan alta como la variabilidad entre especies.
Hay dos patrones que merecen análisis. El primero es una correlación inversa entre facilidad de cultivo y potencia: las especies más manejables para cultivar en condiciones controladas, como P. cubensis, son sistemáticamente las menos potentes. Las más potentes —P. azurescens, P. cyanescens— requieren condiciones de cultivo exteriores y son más difíciles de estandarizar, lo que crea una paradoja para la investigación: las especies más relevantes terapéuticamente podrían ser las más difíciles de producir con la consistencia que los ensayos clínicos requieren.
El segundo patrón es la diferencia en el ratio psilocibina/psilocina. P. semilanceata tiene casi toda su potencia almacenada en psilocibina —que debe convertirse en psilocina antes de actuar—, lo que produce un perfil de inicio lento y meseta estable. P. azurescens tiene niveles excepcionalmente altos de psilocina libre, que actúa directamente: inicio más rápido, intensidad más abrupta. Dos hongos con potencia total similar pueden sentirse radicalmente distintos por este motivo.
Variables que afectan a la concentración alcaloide
Genética: Es el factor dominante. Dentro de la misma especie, cepas diferentes pueden variar su contenido en psilocibina hasta en un factor de cuatro o cinco. La cepa Golden Teacher de P. cubensis produce consistentemente menos alcaloides que la Penis Envy, a pesar de ser la misma especie. En 2025, grupos de cultivadores que combinan secuenciación genómica con hibridación de linajes distantes han producido cepas con hasta un 5% de alcaloides totales en peso seco, frente al 0,5-1% típico del P. cubensis estándar. Esto representa un salto de potencia que la mayoría de las guías de dosificación disponibles no contemplan.
Sustrato: Factor secundario pero real. Los hongos cultivados sobre granos de centeno o arroz tienden a producir frutos con mayor concentración de alcaloides que los cultivados sobre paja o coco, presumiblemente porque la disponibilidad de triptófano como precursor biosintético varía con el sustrato nutricional.
Etapa de desarrollo: La concentración de psilocibina alcanza su máximo justo antes de que el velo que cubre las láminas se rompa. Tras la rotura del velo y el inicio de la esporulación, la concentración puede descender de forma significativa en cuestión de horas. El momento de la cosecha importa más de lo que habitualmente se reconoce.
Conservación: La psilocibina, en material seco almacenado correctamente —oscuridad, temperatura estable, ausencia de humedad—, mantiene el 90-95% de su actividad durante doce a veinticuatro meses. La psilocina se degrada con mayor rapidez por oxidación. El oscurecimiento progresivo del material almacenado es una señal de pérdida de alcaloides activos.
El efecto entourage como hipótesis científica
El concepto de efecto entourage se acuñó en el ámbito del cannabis para describir la sinergia entre cannabinoides y terpenos. En los últimos años se ha comenzado a aplicar a los hongos psilocibios, no sin cautela, porque la evidencia disponible es cualitativamente diferente a la que existe para el cannabis.
La pregunta central es: ¿produce el hongo completo efectos distintos —cuantitativamente o cualitativamente— a la psilocibina aislada, a igualdad de dosis de psilocibina?
Los mecanismos propuestos son farmacológicamente plausibles. La baeocistina podría actuar como agonista parcial en 5-HT₂A, modulando la respuesta máxima a la psilocina mediante competencia por el mismo receptor —un fenómeno conocido en farmacología como efecto techo competitivo. La aeruginascina podría suavizar el componente ansioso bloqueando 5-HT₃, como ya se discutió. Las β-carbolinas podrían extender la ventana de exposición activa al reducir el aclaramiento hepático de la psilocina, alargando el efecto sin aumentar la dosis. Y podrían existir compuestos aún no identificados que influyan sobre vías dopaminérgicas o glutamatérgicas.
Nada de esto está demostrado en humanos. Esta es la limitación fundamental que hay que enunciar con claridad, porque la divulgación sobre hongos psilocibios tiende al exceso en ambas direcciones: hacia la demonización o hacia el entusiasmo acrítico. La evidencia actual para el efecto entourage en hongos es indirecta, basada en observaciones naturalistas, reportes anecdóticos y algunos modelos animales. Hasta que existan ensayos clínicos controlados que comparen directamente el hongo completo frente a psilocibina aislada —con estandarización rigurosa del contenido alcaloide total— cualquier afirmación sobre superioridad terapéutica del hongo completo debe tratarse como hipótesis promisoria, no como hecho establecido.
Pero formular la hipótesis correctamente también importa. Un ensayo clínico que quisiera evaluar el efecto entourage necesitaría al menos cuatro brazos: psilocibina pura, psilocibina más baeocistina, psilocibina más aeruginascina, y extracto estandarizado de hongo completo. Las variables de resultados principales deberían incluir no solo escalas de depresión o ansiedad, sino medidas de la calidad de la experiencia, incidencia de episodios adversos y, si es posible, biomarcadores de neuroplasticidad. Ese ensayo no existe todavía. Diseñarlo es uno de los retos metodológicos más interesantes que la psicofarmacología tiene por delante.
Si el efecto entourage resulta ser clínicamente relevante, las implicaciones regulatorias son considerables: podría justificar vías de aprobación para extractos estandarizados de origen botánico, bajo modelos similares a los que ya existen para el Sativex (cannabis) o el Epidiolex (cannabidiol). Algunos estados de EE.UU. que están regulando el uso terapéutico de hongos —Oregon lleva desde 2023 implementando su marco regulatorio, con más de mil sesiones facilitadas registradas en el primer trimestre de 2025 según Psychedelic Alpha— trabajan con el hongo completo por defecto, lo que convierte a sus programas en fuentes de datos observacionales de enorme interés para esta pregunta.
Equivalencias de dosis entre hongo seco y compuesto aislado
Cualquier discusión sobre alcaloides psilocibios queda incompleta sin abordar la dosificación, aunque este es también el terreno donde la variabilidad alcaloide tiene consecuencias más directas.
La tabla siguiente usa P. cubensis estándar —entre 0,6% y 0,7% de alcaloides totales en peso seco— como referencia, que es el estándar de facto en investigación clínica. Las dosis de psilocibina pura corresponden a los rangos utilizados en los principales ensayos terapéuticos registrados.
| Nivel | Psilocibina pura | Hongo seco (P. cubensis estándar) | Duración | Efectos característicos |
|---|---|---|---|---|
| Microdosis | 0,5 – 3 mg | 0,05 – 0,3 g | 4–6 h (sutil) | Sin percepción alterada. Mejoras reportadas en foco, estado de ánimo y conexión social. Evidencia mixta en ensayos controlados. |
| Dosis umbral | 3 – 8 mg | 0,5 – 1,0 g | 3–5 h | Ligera alteración perceptual. Colores más saturados, sensibilidad emocional aumentada. |
| Dosis baja | 8 – 15 mg | 1,0 – 1,5 g | 4–6 h | Alteraciones visuales suaves, introspección, emociones amplificadas. |
| Dosis media | 15 – 25 mg | 1,5 – 3,5 g | 4–7 h | Experiencia psicodélica plena. Distorsiones visuales, pensamiento no-lineal, alteración del sentido del tiempo. |
| Dosis alta | 25 – 40 mg | 3,5 – 5,0 g | 5–8 h | Disolución del ego. Experiencias de tipo místico. Los ensayos terapéuticos más exitosos utilizan este rango, con acompañamiento psicológico estructurado. |
| Dosis heroica* | > 40 mg | > 5,0 g | 6–10 h | Pérdida de referencia temporal y personal. El rango de mayor riesgo sin apoyo profesional. |
*Término acuñado por Terence McKenna. Usado aquí como referencia cultural establecida, no como recomendación.
La advertencia que merece estar en el centro de esta tabla, no al margen: si se utilizan cepas seleccionadas por su alta potencia —Penis Envy, Albino A+, los nuevos híbridos selectivos de 2025— o especies silvestres como P. azurescens o P. semilanceata, la misma cantidad en gramos puede contener entre dos y cinco veces más alcaloides. El error de no calibrar por potencia real es la causa más documentada de experiencias involuntariamente abrumadoras en contextos no terapéuticos.
Biosíntesis heteróloga, nuevas especies y psychoplastogens
La misma ruta biosintética que explica la diversidad química del hongo es también la que permite replicarla en el laboratorio.
Producir lo que la naturaleza sintetiza
El conocimiento completo de la ruta biosintética de la psilocibina ha abierto una posibilidad que hace veinte años parecía remota: producirla de forma controlada en microorganismos. Grupos académicos en EE.UU. y Alemania han conseguido producir psilocibina en Saccharomyces cerevisiae —la levadura de la cerveza— y en Escherichia coli modificadas genéticamente. La producción farmacéutica a gran escala es técnicamente factible.
Más significativo para la investigación del entourage: la biosíntesis heteróloga permite producir de forma selectiva alcaloides individuales —baeocistina, aeruginascina— que hoy son extremadamente difíciles de aislar en cantidades suficientes del hongo natural. Esto podría desbloquear los ensayos clínicos comparativos que la hipótesis del entourage necesita para ser evaluada.
La diversidad alcaloide que no hemos explorado
De las aproximadamente 200 especies de Psilocybe reconocidas taxonómicamente, la caracterización química completa se ha realizado solo en una fracción pequeña. Las especies de regiones tropicales, de África subsahariana o de Asia sudoriental son prácticamente desconocidas desde el punto de vista bioquímico. La recientemente descrita Psilocybe maluti de Sudáfrica podría contener alcaloides no descritos. El análisis genómico comparativo —buscar en los genomas de hongos secuenciados los genes homólogos al clúster psi— es la estrategia más prometedora para cartografiar esa diversidad sin tener que cultivar y analizar cada especie individualmente.
Separar el efecto terapéutico del psicoactivo
La frontera más audaz de la psicofarmacología psicodélica no es mejorar la psilocibina, sino reemplazarla. Empresas como Delix Therapeutics están desarrollando compuestos denominados psychoplastogens: moléculas que reproducen los efectos neuroplásticos de la psilocina —la formación de nuevas sinapsis, la reactivación de períodos sensibles de la plasticidad neuronal— sin producir la experiencia subjetiva de alto nivel. Si esta estrategia funciona, lograría algo conceptualmente sin precedentes: los beneficios terapéuticos del viaje sin el viaje. Esto reduciría los costes clínicos —el acompañamiento terapéutico durante ocho horas es el componente más caro de los protocolos actuales— y abriría la puerta a tratamientos ambulatorios.
Los críticos señalan que podría también perder parte del mecanismo terapéutico: hay evidencia creciente de que la profundidad de la experiencia mística durante la sesión es un predictor independiente de los resultados terapéuticos. Si se elimina la experiencia, ¿se elimina también parte del efecto? La respuesta importa clínicamente, y actualmente no la tenemos.
Una molécula dominante, una complejidad sin resolver
La química alcaloide de los hongos psilocibios es, a la vez, más sencilla y más compleja de lo que habitualmente se presenta.
Más sencilla porque hay un compuesto dominante —la psilocibina, o más exactamente su metabolito activo la psilocina— cuya farmacología básica está razonablemente bien caracterizada. Sabemos cómo llega al cerebro, qué receptores activa, qué regiones modula y, a grandes rasgos, por qué eso produce los efectos que produce.
Más compleja porque cada alcaloide adicional añade matices que podrían ser irrelevantes o podrían ser decisivos —y no lo sabemos todavía. Porque el mismo hongo produce una composición diferente según la especie, la cepa, el sustrato, el momento de la cosecha y las condiciones de conservación. Porque dos organismos sin relación directa llegaron, por caminos bioquímicos distintos, a sintetizar la misma molécula, lo que sugiere que hay algo en ella que la naturaleza considera valioso más allá de nuestro uso de ella.
Y porque, en última instancia, la pregunta más importante que esta química plantea no es de laboratorio sino clínica: ¿qué formulación —psilocibina pura, alcaloides combinados, hongo completo estandarizado— produce los mejores resultados terapéuticos con los menores riesgos? Esa pregunta tiene respuesta experimental. Lo que hace falta es diseñar los ensayos que puedan responderla.
Referencias
- Fricke J. et al. (2017). Enzymatic synthesis of psilocybin. Angewandte Chemie International Edition, 56(40). — Descripción completa de la ruta biosintética del clúster psi.
- Blei F. et al. (2020). Simultaneous production of psilocybin and β-carboline MAO inhibitors in 'magic mushrooms'. Chemistry – A European Journal. — Primera documentación rigurosa de β-carbolinas en hongos psilocibios.
- Sherwood A.M. et al. (2020). Synthesis and Biological Evaluation of Tryptamine Derivatives. ACS Pharmacology & Translational Science. — Estudio comparativo de baeocistina y psilocibina en modelos animales.
- Carhart-Harris R. et al. (2021). Trial of psilocybin versus escitalopram for depression. NEJM. — Ensayo clínico de referencia; psilocibina sintética pura frente a antidepresivo estándar.
- Heim C. et al. (2025). Convergent evolution of psilocybin biosynthesis in mushrooms. Nature Chemical Biology. — Documentación de la evolución independiente en Psilocybe y Conocybe.
- Polito V. & Stevenson R.J. (2019). A systematic study of microdosing psychedelics. PLOS ONE. — Revisión sistemática de evidencia en microdosificación.
- Gartz J. (1995). Magic Mushrooms Around the World. Jes Publications. — Primera caracterización del perfil de Inocybe aeruginascens y propuesta del papel de la aeruginascina.
- Shin Y-J. et al. (2025). Psilocybin treatment extends cellular lifespan and improves survival of aged mice. NPJ Aging, 11. — Hallazgos preliminares sobre efectos a nivel celular; pendientes de replicación en humanos.
- Psychedelic Alpha (2025). Oregon Psilocybin Services Tracker Q1 2025. Recuperado de psychedelicalpha.com — Datos de implementación del marco regulatorio de Oregón.
Artículos relacionados
-
Psilocibina: qué es, cómo actúa y qué efectos provoca
Publicado : 24/07/2025 12:21:12 -
Guía completa de setas psicoactivas
Publicado : 14/05/2025 22:19:54 -
El enigma evolutivo de la psilocibina
Publicado : 29/12/2025 12:04:40