Guide til alkaloider i psilocybinsvampe
- Hvorfor to identiske svampe giver forskellige oplevelser
- Hvordan svampe fremstiller psilocybin: molekylær oprindelse og evolution
- Svampens alkaloider, molekyle for molekyle
- Psilocybin: det rejsende prodrug
- Psilocin: det hjernen modtager
- Baeocystin: den tredje i rækken
- Norbaeocystin: det mest basale og mindst kendte
- Aeruginascin: det alkaloid der ændrer den følelsesmæssige tone
- Sammenligningstabel over alkaloider i psilocybinsvampe
- En note om β-carbolin
- Styrke efter art og faktorer der bestemmer alkaloidkoncentrationen
- Variabler der påvirker alkaloidkoncentrationen
- Entourage-effekten som videnskabelig hypotese
- Dosis-ækvivalenser mellem tørret svamp og isoleret forbindelse
- Heterolog biosyntese, nye arter og psychoplastogens
- At producere det naturen syntetiserer
- Den alkaloidmangfoldighed vi endnu ikke har udforsket
- At adskille den terapeutiske effekt fra den psykoaktive
- Et dominerende molekyle, en uløst kompleksitet
- Referencer
Hvorfor to identiske svampe giver forskellige oplevelser
Forestil dig, at du har to prøver af tørret svamp foran dig. Du analyserer dem i laboratoriet: samme psilocybinindhold, samme vægt, samme art. Du giver dem til to frivillige med det samme set and setting, den samme forberedelse, den samme terapeutiske støtte. Og resultaterne er forskellige: den ene beskriver en markant angstpræget oplevelse, den anden taler om eufori og vedvarende følelsesmæssig åbenhed.
Hvordan er det muligt?
I årtier har det konventionelle svar lydt: »psykologiske variabler hos subjektet.« Og settet —den mentale tilstand forud for oplevelsen— er uden tvivl en afgørende faktor. Men der findes et andet svar, som videnskaben stille og roligt har bygget op i årevis, og som tvinger os til at gentænke, hvordan vi læser etiketten på en svamp: psilocybinsvampe indeholder ikke én enkelt aktiv forbindelse. De indeholder en familie af alkaloider, der virker i samspil, og denne kemiske orkestrering kan være lige så ansvarlig for oplevelsens profil som forbrugerens psykologi.

Denne guide nedbryder den familie, molekyle for molekyle, fordi det, kliniske forsøg administrerer —ren syntetisk psilocybin— er en bevidst forenklet udgave af det, svampen indeholder.
Hvordan svampe fremstiller psilocybin: molekylær oprindelse og evolution
Før vi taler om virkninger, er det værd at forstå, hvor disse forbindelser stammer fra, og hvorfor en svamp producerer dem.
De psykoaktive alkaloider i psilocybinsvampe er derivater af tryptofan, en af de tyve essentielle aminosyrer, som levende organismer bruger til at opbygge proteiner. Strukturelt deler de alle en indolkerne — det samme molekylære grundgerüst som serotonin, hjernens vigtigste stemningsneurotransmitter — og det er denne strukturelle lighed, der giver dem mulighed for at interagere med de hjernereceptorer, der er designet til serotonin. De er, i bogstaveligste forstand, molekyler, som hjernen forveksler med sit eget indre sprog.
Den biosyntetiske maskine, der fremstiller disse molekyler, blev beskrevet i detaljer i 2017 af Fricke et al. i Angewandte Chemie: en kæde af fire enzymer kodet af genklusteren psi, der omdanner tryptofan til psilocybin i fire successive trin. Hvert enzym har en specifik funktion: PsiD decarboxylerer tryptofanet, PsiK tilføjer fosfatgruppen, PsiM introducerer methylgrupperne, og PsiH udfører den afsluttende hydroxylering. Det er en modulær proces, elegant i sin logik, som bioteknologien allerede har reproduceret i laboratoriegær og -bakterier.
Men den mest foruroligende opdagelse om denne biosyntetiske vej kom i 2025 i et studie publiceret i Nature Chemical Biology af Heim et al.: svampe af slægten Psilocybe og slægten Conocybe —to evolutionært fjerne afstamningslinjer inden for svampenes rige— udviklede evnen til at syntetisere psilocybin på en fuldstændig uafhængig måde. De arvede ikke de samme enzymer fra en fælles forfader: de opfandt forskellige enzymer, der udfører de samme kemiske transformationer for at nå frem til det samme slutprodukt.
Dette kaldes konvergent evolution, og det er relativt sjældent i biokemien. At det sker med et så specifikt og farmakologisk aktivt molekyle som psilocybin tyder på, at der er et kraftigt selektivt pres, der fremmer dets syntese. Den mest udbredte hypotese er, at det fungerer som et forsvar mod prædatorer eller parasitter, selvom det stadig er et aktivt forskningsområde. Det, der er uomtvisteligt, er selve kendsgerningen: to organismer uden direkte ancestral forbindelse »opdagede« uafhængigt af hinanden den samme kemiske løsning. I biokemisk kompleksitetstermer er det en opdagelse af samme konceptuelle familie som blækspruttens øje og det menneskelige øje. Når livet har brug for noget, finder det en tendens til at finde det ad mange veje.
Psilocybinens evolutionære gåde
Psilocybin tilhører ikke kun én svamp. Det forekommer i arter adskilt af millioner af års evolution. Denne artikel udforsker, hvordan biologien fandt (og delte) den samme løsning igen og igen.
Read moreSvampens alkaloider, molekyle for molekyle
Psilocybin: det rejsende prodrug
C₁₂H₁₇N₂O₄P · 4-phosphoryloxy-N,N-dimethyltryptamin · 4-PO-DMT
Psilocybin er familiens mest forekommende og mest stabile alkaloid. Ved stuetemperatur fremstår det som et hvidt krystallinskt fast stof, der i fravær af ekstrem fugtighed og direkte lys bevarer mellem 90 og 95 % af sin aktivitet i et til to år.
Men psilocybin gør i sig selv ingenting i hjernen.
Det er, hvad farmakologer kalder et prodrug: et inaktivt molekyle designet til at blive omdannet til sin aktive form af den modtagende organismes stofskifte. Når det indtages oralt, optages psilocybin i mave-tarmkanalen og når leveren, hvor alkaliske fosfataser fjerner fosfatgruppen og frigiver psilocin. Denne proces, der tager mellem tyve og tres minutter, er ansvarlig for den relativt langsomme virkningstid sammenlignet med andre psykoaktive stoffer. Den orale biotilgængelighed ligger mellem 52 % og 74 % ifølge farmakokinetiske studier, der er gennemgået i de seneste år.
Fosfatgruppens funktion er ikke blot besværlig: den gør molekylet mere polært, mere vandopløseligt og mere stabilt. Psilocybin er på en måde et intelligent transportsystem, der beskytter psilocin mod nedbrydning, indtil det når det sted, hvor det skal virke.
Psilocin: det hjernen modtager
C₁₂H₁₆N₂O · 4-hydroxy-N,N-dimethyltryptamin · 4-HO-DMT
Psilocin er den forbindelse, der faktisk besætter hjernereceptorerne. Uden den fosfatgruppe, der binder den i psilocybin, er den direkte aktiv og virker hurtigere. Ulempen ved denne kemiske frihed er instabiliteten: i nærvær af ilt oxideres den hurtigt og antager brune eller sorte toner. Det er denne proces, der forklarer svampenes berømte blå misfarvning.

Det blå fortjener en grundig forklaring, for det er sandsynligvis det mest kendte visuelle fænomen ved disse svampe og blev misfortolket i årtier. Når en psilocybinsvamp skæres eller presses, kommer det psilocin, der frigives fra vævet, i kontakt med luftens ilt og oxideres under dannelse af quinoner af indigoblå farve. Denne mekanisme blev præcist karakteriseret for første gang i 2020 af Dirk Hoffmeisters hold ved Universitetet i Jena: de resulterende forbindelser er kemisk forskellige fra psilocin og har ingen kendt psykoaktiv aktivitet. Men deres tilstedeværelse er den mest pålidelige visuelle indikator for, at svampen indeholder aktive alkaloider. Intensiteten af blåfarvningen er ikke proportional med styrken, men dens fravær indikerer næsten altid fravær af psilocin.
I hjernen virker psilocin primært som agonist på serotonin type 2A-receptorer (5-HT₂A), der findes i høj tæthed i lag V af den præfrontale cortex og i limbiske regioner. Men psilocins farmakologi er mere promiskuøs end denne overskrift antyder: det viser også affinitet for subtyperne 5-HT₁A, 5-HT₂C, 5-HT₆ og 5-HT₇ samt for dopaminerge (D₂, D₃) og adrenerge receptorer (α₂). Dette netværk af interaktioner bidrager til rigdommen og variabiliteten i virkningsprofilen: det er ikke sådan, at svampen trykker på én enkelt neuronal knap, men at den stemmer et komplekst instrument.
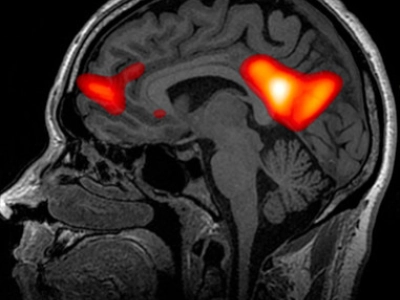
Neuroimaging-studier har dokumenteret to samtidige fænomener under psilocin, der er særligt oplysende. På den ene side er der en hyperkonnektivitet mellem hjerneregioner, der normalt ikke kommunikerer med hinanden: den visuelle cortex taler med den auditive, den sensoriske med den motoriske, temporallappen med frontallappen. På den anden side sker der en markant undertrykkelse af Default Mode Network (DMN) — det kredsløb, der håndterer jeg-fortællingen, den ruminerende tænkning og den personlige identitet. DMN er, i meget konkret forstand, det netværk, der opretholder den historie, vi fortæller os selv om, hvem vi er. Dets hæmning under psilocin korrelerer direkte med den subjektive oplevelse af ego-opløsning, og også — det er det klinisk relevante — med størrelsen af den antidepressive effekt observeret i terapeutiske forsøg. Dette fænomen uddybes i analysen af psilocybins kliniske anvendelser.
Flere nye forbindelser, mindre kontrol fra det vante jeg. Denne dobbelte mekanisme er det neurobiologiske grundlag for både mystiske oplevelser og den antidepressive effekt.
Baeocystin: den tredje i rækken
C₁₁H₁₅N₂O₄P · 4-phosphoryloxy-N-methyltryptamin
Baeocystin er strukturelt den monomethylerede udgave af psilocybin: én enkelt kemisk forskel, der gør det til familiens tredje mest undersøgte alkaloid. Det blev første gang beskrevet i 1968 af Repke et al. i Psilocybe baeocystis, den art der giver det sit navn, og har siden befundet sig i en slags videnskabeligt ingenmandsland: for til stede til at ignorere, for lidt undersøgt til at karakterisere ordentligt.
I visse arter kan baeocystin nå koncentrationer, der er sammenlignelige med psilocybin. P. baeocystis kan indeholde mellem 0,10 % og 0,18 % af tørvægt; P. semilanceata, den kendte spidset tåresvamp fra europæiske enge, når op på 0,42 % i nogle analyser. Det er ikke sporkoncentrationer.
Men hvad gør det præcist? Det er det spørgsmål, den videnskabelige litteratur besvarer med en ærlighed, der fortjener at blive formidlet uden forbehold: det ved vi ikke med sikkerhed. Studier på gnavere tyder på, at det fremkalder milde psykoaktive virkninger ved ækvivalente doser. Et kontrolleret studie fra 2020 (Sherwood et al. i ACS Pharmacology & Translational Science) fandt ingen statistisk signifikante forskelle mellem psilocybin alene og psilocybin plus baeocystin i adfærdsmodeller på dyr. Men et negativt resultat hos mus udelukker ikke en synergistisk effekt hos mennesker. Kontekstens farmakologi — hvordan ét molekyle modificerer reaktionen på et andet — er et af de sværeste områder at studere i psykofarmakologi, og dyremodeller har klare begrænsninger, når det, der undersøges, involverer subjektiv oplevelse.
Norbaeocystin: det mest basale og mindst kendte
C₁₀H₁₃N₂O₄P · 4-phosphoryloxytryptamin
Norbaeocystin er den mest basale form af det psilocybine alkaloidskelet: uden nogen methylgruppe på kvælstoffet. Dets koncentrationer i svampe er sædvanligvis de laveste i familien, sjældent over 0,05 % af tørvægt. Dets lave lipidopløselighed — den egenskab, der giver molekyler mulighed for at krydse cellemembraner, herunder blod-hjerne-barrieren — tyder på en begrænset direkte cerebral penetration.
Hvilket ikke udelukker en rolle som metabolisk forløber: svampe kunne bruge det som udgangspunkt for at syntetisere de andre alkaloider, hvilket ville betyde, at dets koncentration er omvendt proportional med organismens biosyntetiske effektivitet. Der er også mulighed for, at det virker som en allosterisk modulator — et molekyle, der ikke direkte aktiverer en receptor, men ændrer den måde, andre forbindelser gør det på — selvom denne hypotese endnu ikke har direkte belæg.
Aeruginascin: det alkaloid der ændrer den følelsesmæssige tone
C₁₂H₁₉N₂O₄P · N,N,N-trimethyl-4-phosphoryloxytryptamin
Aeruginascin fortjener særlig opmærksomhed, for det er den forbindelse, der mest direkte udfordrer den forsimplede model om, at »psilocybin gør det hele«.
Det blev identificeret i 1985 i Inocybe aeruginascens, en art af beskedent udseende med en primært europæisk udbredelse, der i lang tid blev klassificeret som ikke-psykoaktiv — eller farligt giftig — indtil kemiske analyser afslørede, at den indeholder psilocybinniveauer, der er sammenlignelige med Psilocybe-arter. Det, der fangede forskernes opmærksomhed, var diskrepansen mellem alkaloidindholdet og de rapporterede virkninger: dem, der indtog I. aeruginascens — i mange tilfælde utilsigtet, da de forvekslede den med spiselige svampe — beskrev invariabelt en markant euforisk oplevelse med næsten total fravær af angst og kvalme.
Den tyske forsker Jochen Gartz var den første til at foreslå i 1990'erne, at aeruginascin var ansvarlig for denne differentielle profil: en forbindelse, der i modsætning til alle andre psilocybine alkaloider ikke virker som agonist på 5-HT₂A-receptoren, men som antagonist på 5-HT₃-receptoren.
5-HT₃-receptoren er den eneste ionotrope serotoninreceptor — den virker som en ionkanal, ikke som en G-proteinkoblet receptor — og er involveret i formidlingen af kvalme, opkastning og visse aspekter af følelsesmæssig bearbejdning, særligt anticipatorisk angst. 5-HT₃-antagonister er lægemidler, der anvendes bredt i onkologien netop for at reducere kemoterapi-induceret kvalme. Gartz' hypotese — at aeruginascin modificerer oplevelsens profil, fordi den blokerer denne receptor — har en reel farmakologisk sammenhæng, selvom de direkte beviser hos mennesker stadig er observationelle.
Den terapeutiske implikation er umiddelbar: hvis aeruginascin reducerer sandsynligheden for negative oplevelser ved at blokere 5-HT₃, kunne det være et ekstremt værdifuldt element i udformningen af terapeutiske protokoller. De aktuelle forsøg fra Compass Pathways, MAPS og andre grupper arbejder udelukkende med ren syntetisk psilocybin. Ingen aeruginascin. Denne udelukkelse er metodologisk forståelig — at studere en isoleret forbindelse er metodologisk enklere — men det betyder, at vi ikke ved, om ren psilocybin er den optimale formulering til terapeutisk brug.
Terapeutiske anvendelser af psilocybin
Psilocybin er gået fra at være et forbudt stof til at være et lovende klinisk redskab. Vi undersøger, hvordan det omdefinerer behandlingen af lidelser som depression, angst og afhængighed
Read moreSammenligningstabel over alkaloider i psilocybinsvampe
Den komplette familie, på et øjeblik:
| Alkaloid | Formel | Typisk koncentration (% TV) | Primær receptor | Foreslået funktion |
|---|---|---|---|---|
| Psilocybin | C₁₂H₁₇N₂O₄P | 0,1 – 1,0 | 5-HT₂A (prodrug) | Centralt alkaloid. Psilocin-reservoir. Primær psykedelisk virkning. |
| Psilocin | C₁₂H₁₆N₂O | 0,01 – 0,6 | 5-HT₂A (direkte agonist) | Faktisk aktiv metabolit. Hurtigere indsætning når fri. |
| Baeocystin | C₁₁H₁₅N₂O₄P | 0,01 – 0,5 | 5-HT₂A (svag) | Foreslået modulator. Høj variabilitet mellem arter. |
| Norbaeocystin | C₁₀H₁₃N₂O₄P | Spor < 0,05 | Delvist ukendt | Mulig forløber eller allosterisk modulator. |
| Aeruginascin | C₁₂H₁₉N₂O₄P | 0 – 0,5 (artsvariabelt) | 5-HT₃ (antagonist) | Blokerer kvalme. Modulerer følelsesmæssig tone. Forbundet med euforiske oplevelser. |
| β-Carbolin | Diverse | Spor | Svag MAO-hæmmer | Mulig forlængelse af effekt ved hæmning af levermetabolismen. |
| Phenethylaminer | Diverse | Spor | Dopaminerg / adrenerg | Energigivende. Sjældent kvantificerede. |
Koncentrationer udtrykt som procent af tørvægt (% TV), standardkonvention i den analytiske litteratur.
En note om β-carbolin
β-Carbolin — harmin, harmalin, tetrahydroharmin — er monoaminooxidasehæmmere (MAO-hæmmere), der forekommer i sporkoncentrationer i visse psilocybinsvampe, dokumenteret i studiet af Blei et al. (2020) i Chemistry – A European Journal. Deres tilstedeværelse i svampen fremkalder umiddelbare sammenligninger med ayahuasca, der anvender planter rige på β-carbolin netop for at hæmme den hepatiske nedbrydning af DMT. I svampe er de detekterede koncentrationer imidlertid generelt for lave til at producere en klinisk signifikant MAO-hæmmende effekt alene. De kan være farmakologisk irrelevante under de fleste omstændigheder, eller de kan have en subtil potentierende effekt, som de aktuelle studier ikke har tilstrækkelig opløsning til at detektere.
Styrke efter art og faktorer der bestemmer alkaloidkoncentrationen
Alkaloidfordelingen er ikke ensartet inden for slægten Psilocybe. De ca. 200 anerkendte arter udviser forskellige biokemiske profiler, og disse forskelle har reelle konsekvenser.
| Art | Psilocybin (% TV) | Psilocin (% TV) | Baeocystin (% TV) | Observationer |
|---|---|---|---|---|
| P. cubensis | 0,14 – 0,42 | 0,01 – 0,05 | 0,02 – 0,18 | Den mest dyrkede. Høj variabilitet mellem stammer. De facto-reference i klinisk forskning. |
| P. semilanceata | 0,60 – 1,28 | < 0,01 | 0,03 – 0,42 | Den stærkeste i Europa. Næsten al styrke i psilocybin: langsom indsætning, stabilt profil. |
| P. azurescens | 1,00 – 1,78 | 0,38 – 0,50 | 0,04 – 0,18 | Højest dokumenterede styrke i slægten. Høj psilocin: hurtig indsætning, høj intensitet. Forbundet med reversibel midlertidig lammelse hos visse brugere (wood lovers paralysis). |
| P. cyanescens | 0,85 – 1,50 | 0,15 – 0,30 | 0,03 – 0,10 | Meget udbredt i oceaniske klimaer. Intens fysisk effekt pga. høj psilocin. |
| P. tampanensis | 0,31 – 0,68 | < 0,02 | 0,02 – 0,10 | Producerer sklerotier (magiske trøfler). Mildt og introspektivt profil. |
| P. mexicana | 0,17 – 0,25 | 0,01 – 0,03 | 0,01 – 0,03 | Mesoamerikansk rituel brug dokumenteret i århundreder. Historisk grundlag for moderne forskning. |
| P. baeocystis | 0,60 – 0,85 | 0,10 – 0,14 | 0,10 – 0,18 | Højt baeocystinindhold. Differentieret profil tilskrevet dens sammensætning. Art af interesse for forskning i entourage-effekten. |
| P. subtropicalis (selektiv hybrid 2025) |
op til 5,0 (ikke-replikeret tal) |
variabelt | ingen data | Stamme udviklet gennem selektiv hybridisering assisteret af genomsekventering. Ingen standardiserede kliniske data. |
Værdierne er repræsentative intervaller baseret på syntesen af adskillige analytiske studier publiceret mellem 2010 og 2025, ved brug af HPLC-, GC-MS- og UPLC-metoder. Variabiliteten inden for hver art kan være lige så høj som variabiliteten mellem arterne.
To mønstre fortjener analyse. Det første er en omvendt korrelation mellem dyrkningsbarhed og styrke: de arter, der er lettest at dyrke i kontrollerede omgivelser, som P. cubensis, er systematisk de mindst potente. De stærkeste — P. azurescens, P. cyanescens — kræver udendørsdyrkningsforhold og er sværere at standardisere, hvilket skaber et paradoks for forskningen: de terapeutisk mest relevante arter kan vise sig at være de sværeste at producere med den konsistens, som kliniske forsøg kræver.
Det andet mønster er forskellen i psilocybin/psilocin-forholdet. P. semilanceata har næsten al sin styrke lagret som psilocybin — som skal omdannes til psilocin, før det virker — hvilket giver et profil med langsom indsætning og stabilt plateau. P. azurescens har exceptionelt høje niveauer af frit psilocin, der virker direkte: hurtigere indsætning, mere brat intensitet. To svampe med lignende samlet styrke kan føles radikalt forskellige af denne grund alene.
Variabler der påvirker alkaloidkoncentrationen
Genetik: Det dominerende faktor. Inden for samme art kan forskellige stammer variere deres psilocybinindhold med en faktor på fire til fem. Golden Teacher-stammen af P. cubensis producerer konsekvent færre alkaloider end Penis Envy, på trods af at de tilhører samme art. I 2025 har grupper af dyrkere, der kombinerer genomsekventering med hybridisering af fjerne afstamningslinjer, produceret stammer med op til 5 % samlede alkaloider i tørvægt, mod de typiske 0,5-1 % for standard-P. cubensis. Dette repræsenterer et styrkespring, som de fleste tilgængelige doseringsvejledninger ikke tager højde for.
Substrat: En sekundær men reel faktor. Svampe dyrket på rug- eller riskorn har en tendens til at producere frugtlegemer med højere alkaloidkoncentrationer end dem, der dyrkes på halm eller kokos, formentlig fordi tilgængeligheden af tryptofan som biosyntetisk forløber varierer med næringssubstratet.
Udviklingsfase: Psilocybinkoncentrationen når sit maksimum lige inden det slør, der dækker lamellerne, bristrer. Efter slørets brist og begyndelsen af sporedannelse kan koncentrationen falde betydeligt på blot få timer. Tidspunktet for høst betyder mere, end det almindeligvis anerkendes.
Opbevaring: Psilocybin i korrekt opbevaret tørt materiale — mørke, stabil temperatur, fravær af fugt — bevarer 90-95 % af sin aktivitet i tolv til fireogtyve måneder. Psilocin nedbrydes hurtigere ved oxidation. En progressiv mørkfarvning af det opbevarede materiale er et tegn på tab af aktive alkaloider.
Entourage-effekten som videnskabelig hypotese
Begrebet entourage-effekten blev skabt inden for cannabisfeltet for at beskrive synergi mellem cannabinoider og terpener. I de senere år er det begyndt at blive anvendt på psilocybinsvampe, ikke uden forsigtighed, fordi de tilgængelige beviser er kvalitativt anderledes end dem, der eksisterer for cannabis.
Det centrale spørgsmål er: producerer den hele svamp virkninger — kvantitativt eller kvalitativt — der adskiller sig fra isoleret psilocybin ved samme dosis psilocybin?
De foreslåede mekanismer er farmakologisk plausible. Baeocystin kunne virke som en partiel agonist ved 5-HT₂A og modulere den maksimale respons på psilocin gennem konkurrence om den samme receptor — et fænomen kendt i farmakologien som den kompetitive lofteffekt. Aeruginascin kunne dæmpe angstkomponenten ved at blokere 5-HT₃, som allerede diskuteret. β-Carbolin kunne forlænge det aktive eksponeringsvindue ved at reducere den hepatiske clearance af psilocin og dermed forlænge effekten uden at øge dosen. Og der kan eksistere endnu uidentificerede forbindelser, der påvirker dopaminerge eller glutamaterge veje.
Intet af dette er påvist hos mennesker. Det er den grundlæggende begrænsning, der skal formuleres klart, fordi formidlingen om psilocybinsvampe har tendens til at gå til yderligheder i begge retninger: mod dæmonisering eller mod ukritisk begejstring. De nuværende beviser for entourage-effekten hos svampe er indirekte, baseret på naturalistiske observationer, anekdotiske beretninger og visse dyremodeller. Indtil der eksisterer kontrollerede kliniske forsøg, der direkte sammenligner hele svampen med isoleret psilocybin — med stringent standardisering af det samlede alkaloidindhold — skal enhver påstand om hel svamps terapeutiske overlegenhed behandles som en lovende hypotese, ikke som et etableret faktum.
Men at formulere hypotesen korrekt er også vigtigt. Et klinisk forsøg, der ønskede at evaluere entourage-effekten, ville kræve mindst fire arme: rent psilocybin, psilocybin plus baeocystin, psilocybin plus aeruginascin og standardiseret helsvampekstrakt. De primære resultatvariabler bør ikke kun inkludere depressions- eller angstskalaer, men også mål for oplevelsens kvalitet, forekomst af uønskede hændelser og, om muligt, neuroplasticitetsmarkører. Det forsøg eksisterer endnu ikke. At designe det er en af de mest interessante metodologiske udfordringer, psykofarmakologien har foran sig.
Hvis entourage-effekten viser sig at være klinisk relevant, er de regulatoriske implikationer betydelige: det kunne retfærdiggøre godkendelsesveje for standardiserede botaniske ekstrakter under modeller svarende til dem, der allerede eksisterer for Sativex (cannabis) eller Epidiolex (cannabidiol). Visse amerikanske stater, der regulerer terapeutisk brug af svampe — Oregon har implementeret sin reguleringsramme siden 2023 med over tusind faciliterede sessioner registreret i første kvartal af 2025 ifølge Psychedelic Alpha — arbejder som standard med hele svampen, hvilket gør deres programmer til kilder til observationelle data af enorm interesse for dette spørgsmål.
Dosis-ækvivalenser mellem tørret svamp og isoleret forbindelse
Enhver diskussion om psilocybinalkaloider er ufuldstændig uden at adressere dosering, selvom dette også er det terræn, hvor alkaloidvariabiliteten har de mest direkte konsekvenser.
Den følgende tabel bruger standard P. cubensis — mellem 0,6 % og 0,7 % samlede alkaloider i tørvægt — som reference, hvilket er de facto-standarden i klinisk forskning. Doser af rent psilocybin svarer til de intervaller, der bruges i de vigtigste registrerede terapeutiske forsøg.
| Niveau | Rent psilocybin | Tørret svamp (standard P. cubensis) | Varighed | Karakteristiske virkninger |
|---|---|---|---|---|
| Mikrodosis | 0,5 – 3 mg | 0,05 – 0,3 g | 4–6 t (subtil) | Ingen ændret perception. Rapporterede forbedringer i fokus, humør og social forbundenhed. Blandede beviser i kontrollerede forsøg. |
| Tærskeldosis | 3 – 8 mg | 0,5 – 1,0 g | 3–5 t | Let perceptionsændring. Mere mættede farver, øget følelsesmæssig sensitivitet. |
| Lav dosis | 8 – 15 mg | 1,0 – 1,5 g | 4–6 t | Blide visuelle ændringer, introspektion, forstærkede følelser. |
| Middel dosis | 15 – 25 mg | 1,5 – 3,5 g | 4–7 t | Fuld psykedelisk oplevelse. Visuelle forvrængninger, ikke-lineær tænkning, ændret tidsfornemmelse. |
| Høj dosis | 25 – 40 mg | 3,5 – 5,0 g | 5–8 t | Ego-opløsning. Mystiske oplevelser. De mest succesfulde terapeutiske forsøg anvender dette interval med struktureret psykologisk støtte. |
| Heroisk dosis* | > 40 mg | > 5,0 g | 6–10 t | Tab af tidslig og personlig orientering. Det interval med højest risiko uden professionel støtte. |
*Udtryk skabt af Terence McKenna. Anvendt her som en etableret kulturel reference, ikke som anbefaling.
Den advarsel, der fortjener at stå i centrum af denne tabel og ikke i marginen: hvis der bruges stammer selekteret for høj styrke — Penis Envy, Albino A+, de nye selektive hybrider fra 2025 — eller vilde arter som P. azurescens eller P. semilanceata, kan den samme mængde i gram indeholde mellem to og fem gange så mange alkaloider. Fejlen ved ikke at kalibrere efter den faktiske styrke er den mest dokumenterede årsag til utilsigtet overvældende oplevelser i ikke-terapeutiske sammenhænge.
Heterolog biosyntese, nye arter og psychoplastogens
Den samme biosyntetiske vej, der forklarer svampens kemiske mangfoldighed, er også den, der gør det muligt at replikere den i laboratoriet.
At producere det naturen syntetiserer
Den fulde viden om psilocybins biosyntetiske vej har åbnet en mulighed, der for tyve år siden virkede fjern: at producere det kontrolleret i mikroorganismer. Akademiske grupper i USA og Tyskland har med succes produceret psilocybin i Saccharomyces cerevisiae — ølgær — og i genetisk modificerede Escherichia coli. Farmaseutisk storskalaproduktion er teknisk mulig.
Endnu mere betydningsfuldt for entourage-forskningen: heterolog biosyntese gør det muligt selektivt at producere individuelle alkaloider — baeocystin, aeruginascin — som i dag er ekstremt svære at isolere i tilstrækkelige mængder fra den naturlige svamp. Dette kunne låse op for de komparative kliniske forsøg, som entourage-hypotesen har brug for for at blive evalueret.
Den alkaloidmangfoldighed vi endnu ikke har udforsket
Af de ca. 200 taksonomisk anerkendte Psilocybe-arter er den komplette kemiske karakterisering kun udført på en lille brøkdel. Arter fra tropiske regioner, det subsahariske Afrika eller Sydøstasien er praktisk talt ukendte fra et biokemisk synspunkt. Den nyligt beskrevne Psilocybe maluti fra Sydafrika kunne indeholde hidtil ubeskrevne alkaloider. Den komparative genomanalyse — at søge i sekvenserede svampegenom efter gener homologe til psi-klusteret — er den mest lovende strategi til at kortlægge denne mangfoldighed uden at skulle dyrke og analysere hver art individuelt.
At adskille den terapeutiske effekt fra den psykoaktive
Den dristigste grænse i psykedelisk psykofarmakologi er ikke at forbedre psilocybin, men at erstatte det. Virksomheder som Delix Therapeutics udvikler forbindelser kaldet psychoplastogens: molekyler, der reproducerer psilocins neuroplastiske virkninger — dannelsen af nye synapser, genaktiveringen af sensitive perioder for neural plasticitet — uden at producere den høj-niveau subjektive oplevelse. Hvis denne strategi virker, ville den opnå noget konceptuelt uden fortilfælde: rejsens terapeutiske fordele uden rejsen. Dette ville reducere de kliniske omkostninger — den ottetime terapeutiske ledsagelse er den dyreste komponent i de nuværende protokoller — og åbne døren for ambulant behandling.
Kritikere påpeger, at det også kunne miste en del af den terapeutiske mekanisme: der er voksende beviser for, at dybden af den mystiske oplevelse under sessionen er en uafhængig prædiktor for terapeutiske resultater. Hvis oplevelsen elimineres, elimineres en del af effekten også? Det svar har klinisk betydning, og vi har det ikke i øjeblikket.
Et dominerende molekyle, en uløst kompleksitet
Alkaloidkemien i psilocybinsvampe er på én gang enklere og mere kompleks end normalt fremstillet.
Enklere fordi der er en dominerende forbindelse — psilocybin, eller mere præcist dens aktive metabolit psilocin — hvis grundlæggende farmakologi er rimeligt godt karakteriseret. Vi ved, hvordan den når hjernen, hvilke receptorer den aktiverer, hvilke regioner den modulerer og, i grove træk, hvorfor det producerer de virkninger, det producerer.
Mere kompleks fordi hvert ekstra alkaloid tilføjer nuancer, der kunne være irrelevante eller afgørende — og vi ved det endnu ikke. Fordi den samme svamp producerer en forskellig sammensætning afhængigt af art, stamme, substrat, høsttidspunkt og opbevaringsforhold. Fordi to organismer uden direkte slægtskab nåede frem til, ad biokemisk forskellige veje, at syntetisere det samme molekyle, hvilket antyder, at der er noget i det, som naturen finder værdifuldt ud over vores brug af det.
Og fordi det vigtigste spørgsmål, denne kemi rejser, i sidste ende ikke er et laboratoriumspørgsmål men et klinisk: hvilken formulering — rent psilocybin, kombinerede alkaloider, standardiseret hel svamp — producerer de bedste terapeutiske resultater med de mindste risici? Det spørgsmål har et eksperimentelt svar. Det, der er nødvendigt, er at designe de forsøg, der kan give det.
Referencer
- Fricke J. et al. (2017). Enzymatic synthesis of psilocybin. Angewandte Chemie International Edition, 56(40). — Fuldstændig beskrivelse af den biosyntetiske vej for psi-klusteret.
- Blei F. et al. (2020). Simultaneous production of psilocybin and β-carboline MAO inhibitors in 'magic mushrooms'. Chemistry – A European Journal. — Første stringente dokumentation af β-carbolin i psilocybinsvampe.
- Sherwood A.M. et al. (2020). Synthesis and Biological Evaluation of Tryptamine Derivatives. ACS Pharmacology & Translational Science. — Komparativt studie af baeocystin og psilocybin i dyremodeller.
- Carhart-Harris R. et al. (2021). Trial of psilocybin versus escitalopram for depression. NEJM. — Referenceklinisk forsøg; rent syntetisk psilocybin versus standard antidepressivum.
- Heim C. et al. (2025). Convergent evolution of psilocybin biosynthesis in mushrooms. Nature Chemical Biology. — Dokumentation af uafhængig evolution i Psilocybe og Conocybe.
- Polito V. & Stevenson R.J. (2019). A systematic study of microdosing psychedelics. PLOS ONE. — Systematisk gennemgang af evidens for mikrodosering.
- Gartz J. (1995). Magic Mushrooms Around the World. Jes Publications. — Første karakterisering af Inocybe aeruginascens-profilen og forslag til aeruginascins rolle.
- Shin Y-J. et al. (2025). Psilocybin treatment extends cellular lifespan and improves survival of aged mice. NPJ Aging, 11. — Foreløbige fund om cellulære virkninger; afventer replikation hos mennesker.
- Psychedelic Alpha (2025). Oregon Psilocybin Services Tracker Q1 2025. Hentet fra psychedelicalpha.com — Implementeringsdata for Oregons reguleringsramme.
Relaterede indlæg
-
Psilocybin: hvad det er, hvordan det virker og hvilke effekter det har
Udgivet : 2025-07-24 12:21:12 -
Komplet guide til psykoaktive svampe
Udgivet : 2025-05-14 22:19:54 -
Psilocybinens evolutionære gåde
Udgivet : 2025-12-29 12:04:40