Guide des alcaloïdes des champignons psilocybines
- Pourquoi deux champignons identiques produisent des expériences différentes
- Comment les champignons fabriquent la psilocybine : origine moléculaire et évolution
- Les alcaloïdes du champignon, molécule par molécule
- Psilocybine : le promédicament qui voyage
- Psilocine : ce que le cerveau reçoit
- Baeocystine : le troisième larron
- Norbaeocystine : la plus basique et la moins connue
- Aéruginascine : l'alcaloïde qui change le ton émotionnel
- Tableau comparatif des alcaloïdes des champignons psilocybines
- Une note sur les β-carbolines
- Puissance par espèce et facteurs déterminant la concentration en alcaloïdes
- Variables influençant la concentration en alcaloïdes
- L'effet entourage comme hypothèse scientifique
- Équivalences de doses entre champignon séché et composé isolé
- Biosynthèse hétérologue, nouvelles espèces et psychoplastogens
- Produire ce que la nature synthétise
- La diversité en alcaloïdes que nous n'avons pas encore explorée
- Séparer l'effet thérapeutique du psychoactif
- Une molécule dominante, une complexité irrésolue
- Références
Pourquoi deux champignons identiques produisent des expériences différentes
Imaginez que vous avez devant vous deux échantillons de champignon séché. Vous les analysez en laboratoire : même teneur en psilocybine, même poids, même espèce. Vous les administrez à deux volontaires avec le même set and setting, la même préparation, le même accompagnement thérapeutique. Et les résultats sont différents : l'un décrit une expérience marquée par l'anxiété, l'autre parle d'euphorie et d'ouverture émotionnelle soutenue.
Comment est-ce possible ?
Pendant des décennies, la réponse conventionnelle a été : « variables psychologiques du sujet ». Et le set —l'état mental préalable— est sans aucun doute un facteur déterminant. Mais il existe une autre réponse que la science construit en silence depuis des années, et qui oblige à repenser la façon dont nous lisons l'étiquette d'un champignon : les champignons psilocybines ne contiennent pas un seul composé actif. Ils contiennent une famille d'alcaloïdes qui agissent de concert, et cette orchestration chimique peut être aussi responsable du profil de l'expérience que la psychologie du consommateur.

Ce guide décompose cette famille, molécule par molécule, parce que ce que les essais cliniques administrent — de la psilocybine synthétique pure — est une version délibérément simplifiée de ce que le champignon contient.
Comment les champignons fabriquent la psilocybine : origine moléculaire et évolution
Avant de parler des effets, il convient de comprendre d'où viennent ces composés et pourquoi un champignon les fabrique.
Les alcaloïdes psychoactifs des champignons psilocybines sont des dérivés du tryptophane, l'un des vingt acides aminés essentiels que les organismes vivants utilisent pour construire des protéines. Structurellement, ils partagent tous un noyau indolique — le même squelette moléculaire que la sérotonine, le principal neurotransmetteur de l'humeur — et c'est cette similitude structurelle qui leur permet d'interagir avec les récepteurs cérébraux conçus pour la sérotonine. Ce sont, au sens littéral, des molécules que le cerveau confond avec son propre langage interne.
La machinerie biosynthétique qui fabrique ces molécules a été décrite en détail en 2017 par Fricke et al. dans Angewandte Chemie : une chaîne de quatre enzymes codées par le cluster génique dénommé psi, qui transforme le tryptophane en psilocybine en quatre étapes successives. Chaque enzyme a une fonction spécifique : PsiD décarboxyle le tryptophane, PsiK ajoute le groupe phosphate, PsiM introduit les groupes méthyle, et PsiH réalise l'hydroxylation finale. C'est un processus modulaire, élégant dans sa logique, que la biotechnologie a déjà reproduit dans des levures et des bactéries de laboratoire.
Mais la découverte la plus déconcertante sur cette voie biosynthétique est arrivée en 2025, dans une étude publiée dans Nature Chemical Biology par Heim et al. : les champignons du genre Psilocybe et ceux du genre Conocybe — deux lignées évolutivement éloignées au sein du règne fungi — ont développé la capacité de synthétiser la psilocybine de façon complètement indépendante. Ils n'ont pas hérité des mêmes enzymes d'un ancêtre commun : ils ont inventé des enzymes différentes qui réalisent les mêmes transformations chimiques pour aboutir au même produit final.
On appelle cela l'évolution convergente, et c'est relativement rare en biochimie. Qu'elle se produise avec une molécule aussi spécifique et pharmacologiquement active que la psilocybine suggère qu'il existe une pression sélective puissante qui favorise sa synthèse. L'hypothèse la plus répandue est qu'elle sert de défense contre les prédateurs ou les parasites, bien que ce soit toujours un domaine de recherche actif. Ce qui est indéniable, c'est la donnée elle-même : deux organismes sans relation ancestrale directe ont « découvert », séparément, la même solution chimique. En termes de complexité biochimique, c'est une découverte de la même famille conceptuelle que l'œil du poulpe et l'œil humain. La vie, quand elle a besoin de quelque chose, tend à le trouver par de multiples chemins.
L'énigme évolutive de la psilocybine
La psilocybine n'appartient pas à un seul champignon. Elle apparaît chez des espèces séparées par des millions d'années d'évolution. Cet article explore comment la biologie a trouvé (et partagé) la même solution encore et encore.
Read moreLes alcaloïdes du champignon, molécule par molécule
Psilocybine : le promédicament qui voyage
C₁₂H₁₇N₂O₄P · 4-phosphoryloxy-N,N-diméthyltryptamine · 4-PO-DMT
La psilocybine est l'alcaloïde le plus abondant et le plus stable de la famille. À température ambiante, elle se présente comme un solide cristallin blanc qui, en l'absence d'humidité extrême et de lumière directe, conserve entre 90 et 95 % de son activité pendant un à deux ans.
Mais la psilocybine, en elle-même, ne fait rien dans le cerveau.
C'est ce que les pharmacologues appellent un promédicament : une molécule inactive conçue pour être convertie en sa forme active par le métabolisme de l'organisme récepteur. Lorsqu'elle est ingérée par voie orale, la psilocybine est absorbée dans le tractus gastro-intestinal et arrive au foie, où les phosphatases alcalines éliminent le groupe phosphate et libèrent la psilocine. Ce processus, qui prend entre vingt et soixante minutes, est responsable du début relativement lent des effets par rapport à d'autres substances psychoactives. La biodisponibilité orale oscille entre 52 % et 74 % selon des études de pharmacocinétique révisées ces dernières années.
La fonction du groupe phosphate n'est pas simplement encombrante : elle rend la molécule plus polaire, plus soluble dans l'eau et plus stable. La psilocybine est, en quelque sorte, un système de transport intelligent qui protège la psilocine de la dégradation jusqu'à ce qu'elle atteigne l'endroit où elle doit agir.
Psilocine : ce que le cerveau reçoit
C₁₂H₁₆N₂O · 4-hydroxy-N,N-diméthyltryptamine · 4-HO-DMT
La psilocine est le composé qui occupe réellement les récepteurs cérébraux. Sans le groupe phosphate qui l'enchaîne dans la psilocybine, elle est directement active et agit plus vite. L'inconvénient de cette liberté chimique est l'instabilité : en présence d'oxygène, elle s'oxyde rapidement, prenant des teintes brunes ou noires. C'est ce processus qui explique le fameux bleuissement des champignons.

Le bleu mérite d'être bien expliqué, car c'est probablement le phénomène visuel le plus connu de ces champignons et il a été interprété de façon imprécise pendant des décennies. Quand on coupe ou presse un champignon psilocybine, la psilocine libérée du tissu entre en contact avec l'oxygène de l'air et s'oxyde en formant des quinones de couleur bleu indigo. Ce mécanisme a été caractérisé avec précision pour la première fois en 2020 par l'équipe de Dirk Hoffmeister à l'Université de Iéna : les composés résultants sont chimiquement distincts de la psilocine et n'ont pas d'activité psychoactive connue. Mais leur présence est l'indicateur visuel le plus fiable que le champignon contient des alcaloïdes actifs. L'intensité du bleuissement n'est pas proportionnelle à la puissance, mais son absence indique presque toujours l'absence de psilocine.
Dans le cerveau, la psilocine agit principalement comme agoniste des récepteurs de sérotonine de type 2A (5-HT₂A), que l'on trouve en haute densité dans la couche V du cortex préfrontal et dans les régions limbiques. Mais la pharmacologie de la psilocine est plus promiscue que ne le suggère ce titre : elle montre une affinité également pour les sous-types 5-HT₁A, 5-HT₂C, 5-HT₆ et 5-HT₇, ainsi que pour les récepteurs dopaminergiques (D₂, D₃) et adrénergiques (α₂). Ce réseau d'interactions contribue à la richesse et à la variabilité du profil des effets : ce n'est pas que le champignon appuie sur un seul bouton neuronal, mais qu'il accorde un instrument complexe.
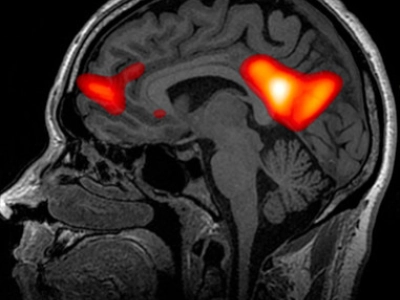
Les études de neuroimagerie ont documenté deux phénomènes simultanés sous psilocine qui sont particulièrement éclairants. D'un côté, il existe une hyperconnectivité entre les régions cérébrales qui ne communiquent normalement pas entre elles : le cortex visuel parle à l'auditif, le sensoriel au moteur, le lobe temporal au frontal. De l'autre, on observe une suppression marquée du Réseau en Mode par Défaut —Default Mode Network ou DMN—, le circuit qui gère le récit du moi, la pensée rumination et l'identité personnelle. Le DMN est, en un sens très concret, le réseau qui maintient l'histoire que nous nous racontons sur qui nous sommes. Son inhibition sous psilocine se corrèle directement avec l'expérience subjective de dissolution de l'ego, et aussi — c'est ce qui est cliniquement pertinent — avec l'ampleur de l'effet antidépresseur observé dans les essais thérapeutiques. Ce phénomène est approfondi dans l'analyse sur les applications cliniques de la psilocybine.
Plus de nouvelles connexions, moins de contrôle du moi habituel. Ce double mécanisme est la base neurobiologique aussi bien des expériences mystiques que de l'effet antidépresseur.
Baeocystine : le troisième larron
C₁₁H₁₅N₂O₄P · 4-phosphoryloxy-N-méthyltryptamine
La baeocystine est structurellement la version mono-méthylée de la psilocybine : une seule différence chimique qui en fait le troisième alcaloïde le plus étudié de la famille. Elle a été décrite pour la première fois en 1968 par Repke et al. dans Psilocybe baeocystis, l'espèce qui lui donne son nom, et depuis lors elle est restée dans une sorte de limbe scientifique : trop présente pour l'ignorer, trop peu étudiée pour bien la caractériser.
Dans certaines espèces, la baeocystine peut atteindre des concentrations comparables à la psilocybine. P. baeocystis peut en contenir entre 0,10 % et 0,18 % en poids sec ; P. semilanceata, la bien connue « coiffe de liberté » des prairies européennes, atteint 0,42 % dans certaines analyses. Ce ne sont pas des quantités traces.
Mais que fait-elle exactement ? C'est la question à laquelle la littérature scientifique répond avec une honnêteté qui mérite d'être transmise sans édulcorer : nous ne le savons pas avec certitude. Les études sur les rongeurs suggèrent qu'elle produit des effets psychoactifs légers à doses équivalentes. Une étude contrôlée de 2020 (Sherwood et al. dans ACS Pharmacology & Translational Science) n'a pas trouvé de différences statistiquement significatives entre la psilocybine seule et la psilocybine plus baeocystine dans des modèles comportementaux animaux. Mais un résultat négatif chez les souris n'exclut pas un effet synergique chez l'humain. La pharmacologie du contexte — comment une molécule modifie la réponse à une autre — est l'un des territoires les plus difficiles à étudier en psychopharmacologie, et les modèles animaux ont des limites claires quand l'objet d'étude implique l'expérience subjective.
Norbaeocystine : la plus basique et la moins connue
C₁₀H₁₃N₂O₄P · 4-phosphoryloxytryptamine
La norbaeocystine est la forme la plus basique du squelette alcaloïde psilocybine : sans aucun groupe méthyle sur l'azote. Ses concentrations dans les champignons sont habituellement les plus basses de la famille, rarement au-dessus de 0,05 % en poids sec. Sa faible liposolubilité — la propriété qui permet aux molécules de traverser les membranes cellulaires, y compris la barrière hémato-encéphalique — suggère une pénétration cérébrale directe limitée.
Ce qui n'exclut pas un rôle de précurseur métabolique : les champignons pourraient l'utiliser comme point de départ pour synthétiser les autres alcaloïdes, ce qui signifierait que sa concentration est inversement proportionnelle à l'efficacité biosynthétique de l'organisme. Il existe aussi la possibilité qu'elle agisse comme modulateur allostérique — une molécule qui n'active pas directement un récepteur mais modifie la façon dont d'autres composés le font —, bien que cette hypothèse ne dispose pas encore de preuves directes.
Aéruginascine : l'alcaloïde qui change le ton émotionnel
C₁₂H₁₉N₂O₄P · N,N,N-triméthyl-4-phosphoryloxytryptamine
L'aéruginascine mérite une attention particulière, car c'est le composé qui remet le plus directement en question le modèle simplifié selon lequel « la psilocybine fait tout ».
Elle a été identifiée en 1985 dans Inocybe aeruginascens, une espèce d'aspect modeste à distribution principalement européenne qui a longtemps été classée comme non psychoactive — ou dangereusement toxique — jusqu'à ce que les analyses chimiques révèlent qu'elle contient des niveaux de psilocybine comparables à des espèces de Psilocybe. Ce qui a attiré l'attention des chercheurs était la discordance entre la teneur en alcaloïdes et les effets rapportés : ceux qui consommaient I. aeruginascens — dans de nombreux cas accidentellement, en la confondant avec des champignons comestibles — décrivaient invariablement une expérience marquée par l'euphorie, avec une quasi-absence d'anxiété et de nausées.
Le chercheur allemand Jochen Gartz fut le premier à proposer, dans les années quatre-vingt-dix, que la responsable de ce profil différentiel était l'aéruginascine : un composé qui, contrairement à tous les autres alcaloïdes psilocybines, n'agit pas comme agoniste du récepteur 5-HT₂A mais comme antagoniste du récepteur 5-HT₃.
Le récepteur 5-HT₃ est le seul récepteur sérotoninergique ionotropique — il agit comme un canal ionique, non comme un récepteur couplé aux protéines G — et il est impliqué dans la médiation des nausées, des vomissements et de certains aspects du traitement émotionnel, notamment l'anxiété anticipatoire. Les antagonistes du 5-HT₃ sont des médicaments largement utilisés en oncologie précisément pour réduire les nausées induites par la chimiothérapie. L'hypothèse de Gartz — que l'aéruginascine modifie le profil du voyage parce qu'elle bloque ce récepteur — a une cohérence pharmacologique réelle, bien que les preuves directes chez l'humain restent observationnelles.
L'implication thérapeutique est immédiate : si l'aéruginascine réduit la probabilité d'expériences adverses en bloquant le 5-HT₃, elle pourrait être un composant de grande valeur pour la conception de protocoles thérapeutiques. Les essais actuels de Compass Pathways, MAPS et d'autres groupes travaillent exclusivement avec de la psilocybine synthétique pure. Pas d'aéruginascine. Cette exclusion est méthodologiquement compréhensible — étudier un composé isolé est méthodologiquement plus simple — mais elle signifie que nous ne savons pas si la psilocybine pure est la formulation optimale pour un usage thérapeutique.
Applications thérapeutiques de la psilocybine
La psilocybine est passée du statut de drogue interdite à celui d'outil clinique prometteur. Nous explorons comment elle redéfinit le traitement de troubles tels que la dépression, l'anxiété et les ad
Read moreTableau comparatif des alcaloïdes des champignons psilocybines
La famille complète, en un coup d'œil :
| Alcaloïde | Formule | Concentration typique (% PS) | Récepteur principal | Fonction proposée |
|---|---|---|---|---|
| Psilocybine | C₁₂H₁₇N₂O₄P | 0,1 – 1,0 | 5-HT₂A (promédicament) | Alcaloïde central. Réservoir de psilocine. Action psychédélique principale. |
| Psilocine | C₁₂H₁₆N₂O | 0,01 – 0,6 | 5-HT₂A (agoniste direct) | Métabolite actif réel. Début d'action plus rapide quand elle est libre. |
| Baeocystine | C₁₁H₁₅N₂O₄P | 0,01 – 0,5 | 5-HT₂A (léger) | Modulateur proposé. Grande variabilité entre espèces. |
| Norbaeocystine | C₁₀H₁₃N₂O₄P | Traces < 0,05 | Partiellement inconnu | Possible précurseur ou modulateur allostérique. |
| Aéruginascine | C₁₂H₁₉N₂O₄P | 0 – 0,5 (variable selon l'espèce) | 5-HT₃ (antagoniste) | Bloque les nausées. Module le ton émotionnel. Associée à des expériences euphoriques. |
| β-Carbolines | Diverses | Traces | IMAO léger | Possible prolongation de l'effet par inhibition du métabolisme hépatique. |
| Phényléthylamines | Diverses | Traces | Dopaminergique / adrénergique | Énergisantes. Rarement quantifiées. |
Concentrations exprimées en pourcentage en poids sec (% PS), convention standard dans la littérature analytique.
Une note sur les β-carbolines
Les β-carbolines — harmine, harmaline, tétrahydroharmine — sont des inhibiteurs de la monoamine oxydase (IMAO) que l'on trouve à l'état de traces dans certains champignons psilocybines, documentés dans l'étude de Blei et al. (2020) dans Chemistry – A European Journal. Leur présence dans le champignon suscite des comparaisons immédiates avec l'ayahuasca, qui utilise des plantes riches en β-carbolines précisément pour inhiber la dégradation hépatique du DMT. Dans les champignons, cependant, les concentrations détectées sont généralement trop faibles pour produire un effet IMAO cliniquement significatif par elles-mêmes. Elles pourraient être pharmacologiquement non pertinentes dans la plupart des circonstances, ou pourraient avoir un effet potentialisateur subtil que les études actuelles n'ont pas la résolution suffisante pour détecter.
Puissance par espèce et facteurs déterminant la concentration en alcaloïdes
La distribution des alcaloïdes n'est pas uniforme dans le genre Psilocybe. Les quelque 200 espèces reconnues présentent des profils biochimiques distincts, et ces différences ont des conséquences réelles.
| Espèce | Psilocybine (% PS) | Psilocine (% PS) | Baeocystine (% PS) | Observations |
|---|---|---|---|---|
| P. cubensis | 0,14 – 0,42 | 0,01 – 0,05 | 0,02 – 0,18 | La plus cultivée. Grande variabilité entre souches. Référence de facto en recherche clinique. |
| P. semilanceata | 0,60 – 1,28 | < 0,01 | 0,03 – 0,42 | La plus puissante d'Europe. Presque toute la puissance en psilocybine : début lent, profil stable. |
| P. azurescens | 1,00 – 1,78 | 0,38 – 0,50 | 0,04 – 0,18 | Puissance maximale documentée dans le genre. Psilocine élevée : début rapide, intensité élevée. Associée à une paralysie temporaire réversible chez certains consommateurs (wood lovers paralysis). |
| P. cyanescens | 0,85 – 1,50 | 0,15 – 0,30 | 0,03 – 0,10 | Très répandue dans les climats océaniques. Effet physique intense dû à la psilocine élevée. |
| P. tampanensis | 0,31 – 0,68 | < 0,02 | 0,02 – 0,10 | Produit des sclérotes (truffes magiques). Profil doux et introspectif. |
| P. mexicana | 0,17 – 0,25 | 0,01 – 0,03 | 0,01 – 0,03 | Usage rituel mésoaméricain documenté depuis des siècles. Base historique de la recherche moderne. |
| P. baeocystis | 0,60 – 0,85 | 0,10 – 0,14 | 0,10 – 0,18 | Baeocystine élevée. Profil différentiel attribué à sa composition. Espèce d'intérêt pour la recherche sur l'effet entourage. |
| P. subtropicalis (hybride sélectif 2025) |
jusqu'à 5,0 (donnée non répliquée) |
variable | sans données | Souche développée par hybridation sélective assistée par séquençage génomique. Sans données cliniques standardisées. |
Les valeurs sont des plages représentatives basées sur la synthèse de multiples études analytiques publiées entre 2010 et 2025, utilisant des méthodologies HPLC, GC-MS et UPLC. La variabilité au sein de chaque espèce peut être aussi élevée que la variabilité entre espèces.
Deux schémas méritent analyse. Le premier est une corrélation inverse entre facilité de culture et puissance : les espèces les plus faciles à cultiver en conditions contrôlées, comme P. cubensis, sont systématiquement les moins puissantes. Les plus puissantes — P. azurescens, P. cyanescens — nécessitent des conditions de culture en extérieur et sont plus difficiles à standardiser, ce qui crée un paradoxe pour la recherche : les espèces les plus pertinentes sur le plan thérapeutique pourraient être les plus difficiles à produire avec la constance que les essais cliniques exigent.
Le second schéma est la différence dans le rapport psilocybine/psilocine. P. semilanceata stocke presque toute sa puissance en psilocybine — qui doit être convertie en psilocine avant d'agir —, ce qui produit un profil à début lent et plateau stable. P. azurescens présente des niveaux exceptionnellement élevés de psilocine libre, qui agit directement : début plus rapide, intensité plus abrupte. Deux champignons de puissance totale similaire peuvent se ressentir de façon radicalement différente pour cette raison.
Variables influençant la concentration en alcaloïdes
Génétique : C'est le facteur dominant. Au sein d'une même espèce, des souches différentes peuvent faire varier leur teneur en psilocybine d'un facteur quatre à cinq. La souche Golden Teacher de P. cubensis produit systématiquement moins d'alcaloïdes que la Penis Envy, malgré leur appartenance à la même espèce. En 2025, des groupes de cultivateurs combinant séquençage génomique et hybridation de lignées éloignées ont produit des souches contenant jusqu'à 5 % d'alcaloïdes totaux en poids sec, contre les 0,5-1 % typiques du P. cubensis standard. Cela représente un saut de puissance que la plupart des guides de dosage disponibles ne prennent pas en compte.
Substrat : Facteur secondaire mais réel. Les champignons cultivés sur du seigle ou du riz tendent à produire des fructifications avec une concentration plus élevée en alcaloïdes que ceux cultivés sur de la paille ou de la noix de coco, vraisemblablement parce que la disponibilité du tryptophane comme précurseur biosynthétique varie selon le substrat nutritionnel.
Stade de développement : La concentration en psilocybine atteint son maximum juste avant que le voile couvrant les lamelles ne se rompe. Après la rupture du voile et le début de la sporulation, la concentration peut diminuer de façon significative en quelques heures. Le moment de la récolte a plus d'importance qu'on ne le reconnaît habituellement.
Conservation : La psilocybine, dans un matériau sec correctement conservé — obscurité, température stable, absence d'humidité —, conserve 90-95 % de son activité pendant douze à vingt-quatre mois. La psilocine se dégrade plus rapidement par oxydation. L'assombrissement progressif du matériau stocké est un signe de perte d'alcaloïdes actifs.
L'effet entourage comme hypothèse scientifique
Le concept d'effet entourage a été forgé dans le domaine du cannabis pour décrire la synergie entre cannabinoïdes et terpènes. Ces dernières années, il a commencé à s'appliquer aux champignons psilocybines, non sans prudence, car les preuves disponibles sont qualitativement différentes de celles qui existent pour le cannabis.
La question centrale est : le champignon entier produit-il des effets différents — quantitativement ou qualitativement — par rapport à la psilocybine isolée, à dose de psilocybine égale ?
Les mécanismes proposés sont pharmacologiquement plausibles. La baeocystine pourrait agir comme agoniste partiel au niveau du 5-HT₂A, modulant la réponse maximale à la psilocine par compétition pour le même récepteur — un phénomène connu en pharmacologie sous le nom d'effet plafond compétitif. L'aéruginascine pourrait atténuer la composante anxieuse en bloquant le 5-HT₃, comme nous l'avons déjà mentionné. Les β-carbolines pourraient prolonger la fenêtre d'exposition active en réduisant la clairance hépatique de la psilocine, allongeant l'effet sans augmenter la dose. Et il pourrait exister des composés encore non identifiés qui influencent les voies dopaminergiques ou glutamatergiques.
Rien de tout cela n'est démontré chez l'humain. C'est la limitation fondamentale qu'il faut énoncer clairement, car la vulgarisation sur les champignons psilocybines tend à l'excès dans les deux directions : vers la diabolisation ou vers l'enthousiasme acritique. Les preuves actuelles de l'effet entourage chez les champignons sont indirectes, basées sur des observations naturalistes, des rapports anecdotiques et quelques modèles animaux. Jusqu'à ce qu'il existe des essais cliniques contrôlés comparant directement le champignon entier à la psilocybine isolée — avec une standardisation rigoureuse de la teneur totale en alcaloïdes — toute affirmation sur la supériorité thérapeutique du champignon entier doit être traitée comme une hypothèse prometteuse, non comme un fait établi.
Mais formuler correctement l'hypothèse est également important. Un essai clinique voulant évaluer l'effet entourage nécessiterait au moins quatre bras : psilocybine pure, psilocybine plus baeocystine, psilocybine plus aéruginascine, et extrait standardisé de champignon entier. Les variables de résultats principales devraient inclure non seulement des échelles de dépression ou d'anxiété, mais aussi des mesures de la qualité de l'expérience, l'incidence d'épisodes indésirables et, si possible, des biomarqueurs de neuroplasticité. Cet essai n'existe pas encore. Le concevoir est l'un des défis méthodologiques les plus intéressants que la psychopharmacologie ait devant elle.
Si l'effet entourage s'avère cliniquement pertinent, les implications réglementaires sont considérables : il pourrait justifier des voies d'approbation pour des extraits standardisés d'origine botanique, sous des modèles similaires à ceux qui existent déjà pour le Sativex (cannabis) ou l'Epidiolex (cannabidiol). Certains États américains qui régulent l'usage thérapeutique des champignons — l'Oregon met en œuvre son cadre réglementaire depuis 2023, avec plus de mille séances facilitées enregistrées au premier trimestre 2025 selon Psychedelic Alpha — travaillent par défaut avec le champignon entier, ce qui fait de leurs programmes des sources de données observationnelles d'un intérêt immense pour cette question.
Équivalences de doses entre champignon séché et composé isolé
Toute discussion sur les alcaloïdes psilocybines reste incomplète sans aborder le dosage, bien que ce soit aussi le terrain où la variabilité des alcaloïdes a les conséquences les plus directes.
Le tableau suivant utilise le P. cubensis standard — entre 0,6 % et 0,7 % d'alcaloïdes totaux en poids sec — comme référence, qui est le standard de facto en recherche clinique. Les doses de psilocybine pure correspondent aux plages utilisées dans les principaux essais thérapeutiques enregistrés.
| Niveau | Psilocybine pure | Champignon séché (P. cubensis standard) | Durée | Effets caractéristiques |
|---|---|---|---|---|
| Microdose | 0,5 – 3 mg | 0,05 – 0,3 g | 4–6 h (subtil) | Sans perception altérée. Améliorations rapportées de la concentration, de l'humeur et de la connexion sociale. Preuves mitigées dans les essais contrôlés. |
| Dose seuil | 3 – 8 mg | 0,5 – 1,0 g | 3–5 h | Légère altération perceptuelle. Couleurs plus saturées, sensibilité émotionnelle accrue. |
| Dose faible | 8 – 15 mg | 1,0 – 1,5 g | 4–6 h | Altérations visuelles douces, introspection, émotions amplifiées. |
| Dose moyenne | 15 – 25 mg | 1,5 – 3,5 g | 4–7 h | Expérience psychédélique pleine. Distorsions visuelles, pensée non linéaire, altération du sens du temps. |
| Dose élevée | 25 – 40 mg | 3,5 – 5,0 g | 5–8 h | Dissolution de l'ego. Expériences de type mystique. Les essais thérapeutiques les plus réussis utilisent cette plage, avec un accompagnement psychologique structuré. |
| Dose héroïque* | > 40 mg | > 5,0 g | 6–10 h | Perte de repères temporels et personnels. La plage présentant le risque le plus élevé sans soutien professionnel. |
*Terme forgé par Terence McKenna. Utilisé ici comme référence culturelle établie, non comme recommandation.
L'avertissement qui mérite d'être au centre de ce tableau, et non en marge : si l'on utilise des souches sélectionnées pour leur haute puissance — Penis Envy, Albino A+, les nouveaux hybrides sélectifs de 2025 — ou des espèces sauvages comme P. azurescens ou P. semilanceata, la même quantité en grammes peut contenir entre deux et cinq fois plus d'alcaloïdes. L'erreur de ne pas calibrer en fonction de la puissance réelle est la cause la plus documentée d'expériences involontairement accablantes dans des contextes non thérapeutiques.
Biosynthèse hétérologue, nouvelles espèces et psychoplastogens
La même voie biosynthétique qui explique la diversité chimique du champignon est aussi celle qui permet de la reproduire en laboratoire.
Produire ce que la nature synthétise
La connaissance complète de la voie biosynthétique de la psilocybine a ouvert une possibilité qui semblait lointaine il y a vingt ans : la produire de façon contrôlée dans des micro-organismes. Des groupes académiques aux États-Unis et en Allemagne ont réussi à produire de la psilocybine dans Saccharomyces cerevisiae — la levure de bière — et dans des Escherichia coli génétiquement modifiées. La production pharmaceutique à grande échelle est techniquement faisable.
Plus significatif encore pour la recherche sur l'entourage : la biosynthèse hétérologue permet de produire sélectivement des alcaloïdes individuels — baeocystine, aéruginascine — qui sont aujourd'hui extrêmement difficiles à isoler en quantités suffisantes à partir du champignon naturel. Cela pourrait débloquer les essais cliniques comparatifs dont l'hypothèse de l'entourage a besoin pour être évaluée.
La diversité en alcaloïdes que nous n'avons pas encore explorée
Sur les quelque 200 espèces de Psilocybe reconnues taxonomiquement, la caractérisation chimique complète n'a été réalisée que pour une petite fraction. Les espèces des régions tropicales, d'Afrique subsaharienne ou d'Asie du Sud-Est sont pratiquement inconnues du point de vue biochimique. La récemment décrite Psilocybe maluti d'Afrique du Sud pourrait contenir des alcaloïdes non décrits. L'analyse génomique comparative — rechercher dans les génomes de champignons séquencés les gènes homologues au cluster psi — est la stratégie la plus prometteuse pour cartographier cette diversité sans avoir à cultiver et analyser chaque espèce individuellement.
Séparer l'effet thérapeutique du psychoactif
La frontière la plus audacieuse de la psychopharmacologie psychédélique n'est pas d'améliorer la psilocybine, mais de la remplacer. Des entreprises comme Delix Therapeutics développent des composés appelés psychoplastogens : des molécules qui reproduisent les effets neuroplastiques de la psilocine — la formation de nouvelles synapses, la réactivation des périodes sensibles de la plasticité neuronale — sans produire l'expérience subjective de haut niveau. Si cette stratégie fonctionne, elle parviendrait à quelque chose de conceptuellement sans précédent : les bénéfices thérapeutiques du voyage sans le voyage. Cela réduirait les coûts cliniques — l'accompagnement thérapeutique pendant huit heures est la composante la plus coûteuse des protocoles actuels — et ouvrirait la porte à des traitements ambulatoires.
Les critiques soulignent que cela pourrait aussi faire perdre une partie du mécanisme thérapeutique : il existe des preuves croissantes que la profondeur de l'expérience mystique pendant la séance est un prédicteur indépendant des résultats thérapeutiques. Si l'on supprime l'expérience, supprime-t-on aussi une partie de l'effet ? La réponse a une importance clinique, et nous ne l'avons pas encore.
Une molécule dominante, une complexité irrésolue
La chimie des alcaloïdes des champignons psilocybines est à la fois plus simple et plus complexe que ce qui est habituellement présenté.
Plus simple parce qu'il existe un composé dominant — la psilocybine, ou plus exactement son métabolite actif la psilocine — dont la pharmacologie de base est raisonnablement bien caractérisée. Nous savons comment elle atteint le cerveau, quels récepteurs elle active, quelles régions elle module et, dans les grandes lignes, pourquoi cela produit les effets qu'elle produit.
Plus complexe parce que chaque alcaloïde supplémentaire ajoute des nuances qui pourraient être non pertinentes ou pourraient être décisives — et nous ne le savons pas encore. Parce que le même champignon produit une composition différente selon l'espèce, la souche, le substrat, le moment de la récolte et les conditions de conservation. Parce que deux organismes sans relation directe sont parvenus, par des voies biochimiques distinctes, à synthétiser la même molécule, ce qui suggère qu'il y a en elle quelque chose que la nature juge précieux au-delà de l'usage que nous en faisons.
Et parce que, en dernière instance, la question la plus importante que cette chimie pose n'est pas de laboratoire mais clinique : quelle formulation — psilocybine pure, alcaloïdes combinés, champignon entier standardisé — produit les meilleurs résultats thérapeutiques avec les moindres risques ? Cette question a une réponse expérimentale. Ce qu'il faut, c'est concevoir les essais qui pourront y répondre.
Références
- Fricke J. et al. (2017). Enzymatic synthesis of psilocybin. Angewandte Chemie International Edition, 56(40). — Description complète de la voie biosynthétique du cluster psi.
- Blei F. et al. (2020). Simultaneous production of psilocybin and β-carboline MAO inhibitors in 'magic mushrooms'. Chemistry – A European Journal. — Première documentation rigoureuse des β-carbolines dans les champignons psilocybines.
- Sherwood A.M. et al. (2020). Synthesis and Biological Evaluation of Tryptamine Derivatives. ACS Pharmacology & Translational Science. — Étude comparative de la baeocystine et de la psilocybine dans des modèles animaux.
- Carhart-Harris R. et al. (2021). Trial of psilocybin versus escitalopram for depression. NEJM. — Essai clinique de référence ; psilocybine synthétique pure versus antidépresseur standard.
- Heim C. et al. (2025). Convergent evolution of psilocybin biosynthesis in mushrooms. Nature Chemical Biology. — Documentation de l'évolution indépendante chez Psilocybe et Conocybe.
- Polito V. & Stevenson R.J. (2019). A systematic study of microdosing psychedelics. PLOS ONE. — Revue systématique des données probantes sur le microdosage.
- Gartz J. (1995). Magic Mushrooms Around the World. Jes Publications. — Première caractérisation du profil d'Inocybe aeruginascens et proposition du rôle de l'aéruginascine.
- Shin Y-J. et al. (2025). Psilocybin treatment extends cellular lifespan and improves survival of aged mice. NPJ Aging, 11. — Résultats préliminaires sur les effets cellulaires ; en attente de réplication chez l'humain.
- Psychedelic Alpha (2025). Oregon Psilocybin Services Tracker Q1 2025. Récupéré de psychedelicalpha.com — Données de mise en œuvre du cadre réglementaire de l'Oregon.
Articles en relation
-
Psilocybine : qu'est-ce que c'est, comment agit-elle et quels sont ses effets ?
Publié : 24/07/2025 12:21:12 -
Guide complet des champignons psychoactifs
Publié : 14/05/2025 22:19:54 -
L'énigme évolutive de la psilocybine
Publié : 29/12/2025 12:04:40