Fusarium venenatum, el fong que desafia l'eficiència de la indústria càrnia
La indústria global de la proteïna travessa una fase d'esgotament silenciós. Durant l'última dècada, la resposta dominant a la crisi ambiental i ètica de la ramaderia ha estat la proliferació de productes vegetals que imiten la carn: hamburgueses de pèsol, salsitxes de soja, matrius de midó i aromes reconstruïdes al laboratori. Han aconseguit reduir emissions i obrir el debat, però no han convençut tothom. Ni al paladar, ni als sistemes agrícoles, ni als balanços energètics.
En aquest context, la ciència ha començat a mirar amb major atenció un territori que no és ni animal ni vegetal: el regne fungi. No com una moda culinària, sinó com una plataforma biotecnològica madura, capaç de produir proteïna d'alta qualitat amb una eficiència metabòlica que l'agricultura tradicional no pot igualar.

El punt d'inflexió va arribar el novembre de 2025. Un equip d'investigadors de la Universitat de Jiangnan (Xina), liderat per el doctor Xiao Liu, va publicar a Trends in Biotechnology un avenç que canvia les regles del joc. Utilitzant edició genètica de precisió, van aconseguir optimitzar el fong Fusarium venenatum per convertir-lo en una font de proteïna significativament més productiva i barata. No es va tractar d'una promesa futurista, sinó d'un desbloqueig molecular concret amb resultats immediats.
Redissenyar el metabolisme fúngic
La micoproteïna no és un descobriment recent ni una resposta improvisada a l'ansietat climàtica. Fusarium venenatum és un vell conegut identificat com a candidat alimentari ja als anys setanta, en un context marcat per crisis energètiques i temor al desproveïment. Quan va arribar al mercat als anys vuitanta (sota marques com Quorn), la seva proposta era radical: produir proteïna en tancs de fermentació, sense camp, sense pastures i sense animals.
No obstant això, aquella primera generació va arribar amb limitacions. La seva producció industrial sempre ha xocat amb un límit biològic: la velocitat a la qual el fong pot assimilar nutrients, específicament el nitrogen. Durant dècades, Fusarium va sobreviure com una solució de nínxol, amb costos elevats i una eficiència que no acabava d'enlairar-se.
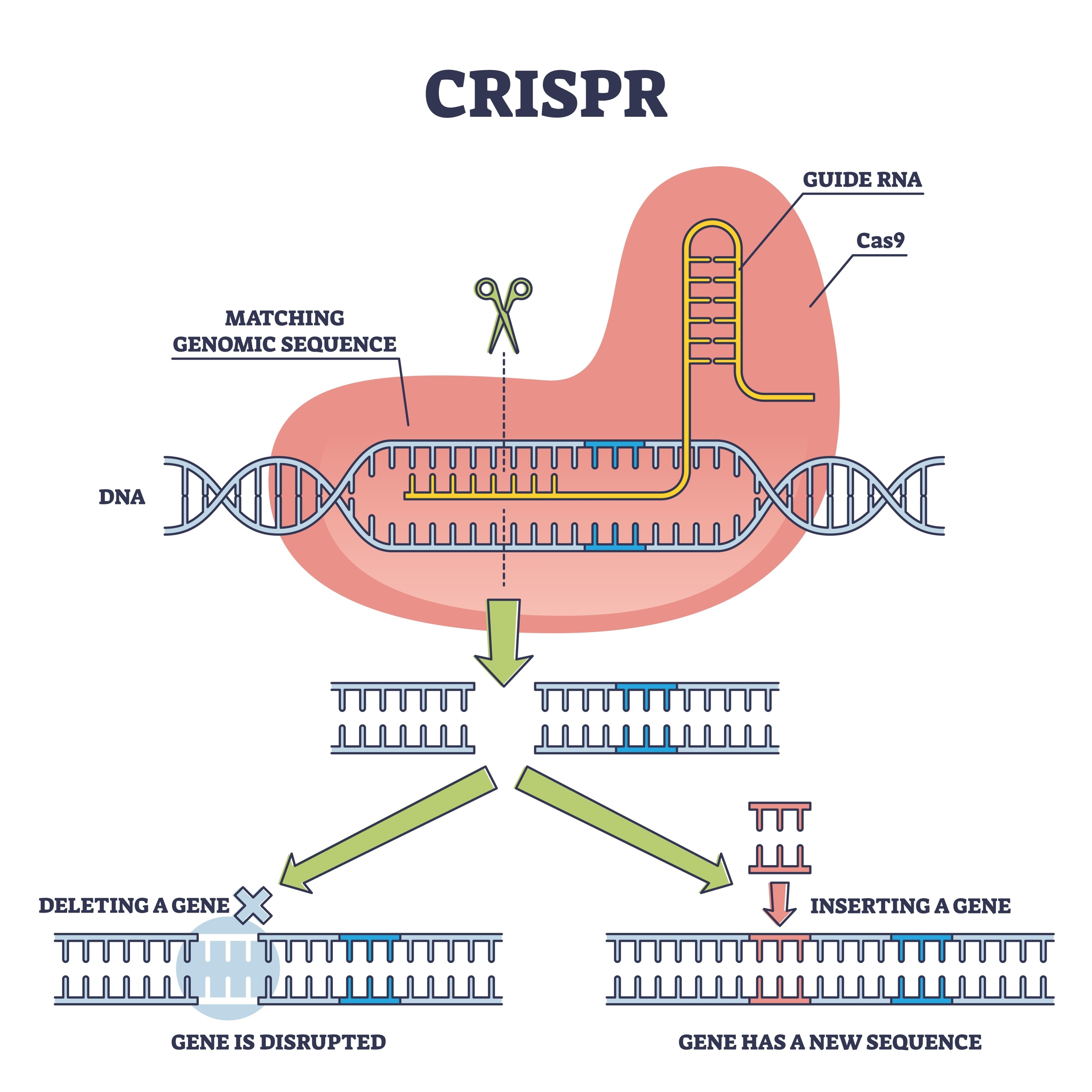
Aquí és on entra l'equip de Xiao Liu, rescatant aquesta tecnologia per col·locar-la en condicions de competir. Van optar per una estratègia de "cisgènesi". A diferència dels transgènics clàssics, on s'introdueix ADN d'altres espècies, aquí es va utilitzar l'eina CRISPR-Cas9 per editar gens que ja existien al fong. L'objectiu va ser una família gènica concreta: glnA, responsable de la producció de la glutamina sintetasa. Aquest enzim actua com a "porter" metabòlic; a la soca silvestre, limita la quantitat de nitrogen que el fong absorbeix per construir proteïnes.
En modificar els promotors d'aquests gens, els investigadors van aconseguir treure-li el "fre de mà" a l'organisme. El resultat és un fong que optimitza el seu metabolisme intern per deixar de regular el seu creixement a la baixa, convertint els nutrients en biomassa amb una voracitat inèdita.
Increment de biomassa i reducció de costos
A la indústria alimentària, la sostenibilitat és una equació matemàtica. Si el producte final és car o lent de produir, no substituirà la carn. Els resultats presentats per la Universitat de Jiangnan ataquen precisament aquesta equació amb xifres contundents:
- Explosió de creixement (+88 %): En condicions de cultiu idèntiques, la soca editada gairebé duplica la seva biomassa respecte a la variant natural. Això permet a les plantes de fermentació duplicar la seva producció sense necessitat de construir nous bioreactors, reduint dràsticament la inversió de capital necessària.
- Estalvi de recursos (-44 %): El fong modificat va necessitar gairebé la meitat de sucre per créixer. Atès que el medi de cultiu (l'"aliment" del fong) representa un dels majors costos operatius, aquesta eficiència és la clau per assolir la paritat de preus amb la carn industrial barata.
Si contextualitzem aquestes dades, l'abisme amb la ramaderia s'eixampla. La producció d'aquesta micoproteïna emet entre un 60 i un 70 % menys de gasos d'efecte hivernacle que el boví i elimina de l'equació la desforestació i el consum massiu d'aigua. És proteïna industrialitzada, sí, però sense el llast ecològic del model carni tradicional.

Així i tot, l'eficiència no és una promesa automàtica. En biotecnologia, els resultats de laboratori no sempre sobreviuen al salt a escala industrial. Un organisme que creix amb voracitat en condicions controlades pot comportar-se de forma imprevisible en fermentadors de centenars de milers de litres, sotmesos a variacions de temperatura, oxigenació i estrès metabòlic perllongat.
Els mateixos autors de l'estudi assenyalen que el següent desafiament serà avaluar l'estabilitat genètica de la soca editada a llarg termini, així com el seu comportament en cicles continus de producció. La història de la biotecnologia alimentària és plena d'avenços brillants que van fracassar no per falta de ciència, sinó per límits pràctics. Aquest Fusarium ha guanyat velocitat; ara ha de demostrar resistència.
Però produir més proteïna no serveix de res si el cos humà no la pot aprofitar. I aquí és on la biologia del fong plantejava, fins ara, un dels seus majors límits.
Més nutritiu i digerible: com l'edició genètica redissenya la fibra fúngica
El consumidor no compra proteïnes; compra experiència. Fibra, mossegada, sucositat. Aquí és on la biologia del fong ofereix un avantatge estructural: creix formant hifes, filaments microscòpics que imiten de forma natural la disposició de les fibres musculars animals.
No obstant això, aquesta arquitectura tenia un preu ocult: la biodisponibilitat. Les cèl·lules dels fongs estan protegides per parets rígides de quitina —el mateix material de l'exoesquelet dels insectes—. Fins ara, per al sistema digestiu humà, trencar aquesta "armadura" resultava complex, la qual cosa impedia accedir a gran part de la proteïna que el fong emmagatzema al seu interior. Teníem un aliment ric en teoria, però no sempre aprofitat amb l'eficiència que la seva composició prometia.
L'equip de Jiangnan va abordar aquest obstacle amb una segona ronda d'edició genètica, paral·lela a la del creixement. Van eliminar els gens associats a la quitina sintasa, reduint significativament el gruix de la paret cel·lular.
El resultat és un equilibri biotecnològic delicat: les hifes mantenen la seva estructura entrellaçada (preservant la textura càrnia), però els seus murs defensius són ara més fins. En "aprimar" aquesta barrera, els investigadors van alliberar la proteïna intracel·lular perquè el nostre cos la pugui absorbir realment. Ja no és només un aliment que "omple" per la seva fibra, sinó un que nodreix amb l'eficiència promesa.
Encara que l'estudi de Liu es va centrar en creixement i digestibilitat, el camp avança cap al sabor. Altres investigacions recents utilitzen tècniques similars per induir la producció d'hemoproteïnes —responsables del gust metàl·lic de la carn—, prometent tancar la bretxa sensorial definitiva entre el fermentador i l'escorxador.
Escalat industrial i marc regulatori
No és casual que aquest avenç provingui de la Xina. En l'última dècada, el país ha identificat la fermentació de precisió com una tecnologia estratègica, capaç de reduir la seva dependència d'importacions agrícoles i esmorteir la volatilitat dels mercats globals de proteïna.
La proteïna fúngica no només competeix amb la carn: competeix amb el model agrícola extensiu, amb la logística global i amb la geopolítica de l'aliment. En aquest tauler, els bioreactors es converteixen en infraestructures tan crítiques com les sitges de gra o els ports comercials.

L'avenç científic és innegable, però el camí al supermercat passa per la burocràcia. No obstant això, la tècnica triada per l'equip de Xiao Liu podria facilitar el procés. En no incorporar ADN exogen, aquests fongs se situen en una zona regulatòria favorable en regions com els Estats Units i, cada vegada més, a la Unió Europea, on es comença a distingir entre organismes modificats genèticament (OMG) clàssics i organismes editats (NGT). La lògica és que, en no introduir material genètic d'espècies estranyes, el resultat final es considera biològicament equivalent a una mutació que podria haver ocorregut a la natura. Això permet esquivar els estrictes i costosos protocols de seguretat exigits als transgènics clàssics.
En una planta de fermentació, no hi ha prats ni corrals. Només tancs d'acer, canonades i una remor constant de líquids en moviment. El fong creix sense veure la llum del sol, transformant sucres i nitrogen en fibres comestibles amb una eficiència que cap animal pot replicar. No hi ha sacrifici ni èpica rural: només metabolisme optimitzat.
Potser aquesta sigui la raó per la qual aquesta revolució avança en silenci. No apel·la a la nostàlgia ni a l'emoció, sinó a una pregunta incòmoda: què estem disposats a deixar enrere per seguir alimentant-nos sense esgotar el planeta.
En un món que s'aproxima als deu mil milions d'habitants, la pregunta potser no sigui si acceptarem menjar fongs, sinó quines altres idees sobre el menjar haurem d'abandonar per seguir alimentant-nos sense esgotar el planeta. La proposta de Liu ofereix una solució sòbria: proteïna abundant, eficient i barata, cultivada en la foscor per deixar que el planeta recuperi la llum.
Fonts i referències
- Liu, X., et al. (2025). Dual enhancement of mycoprotein nutrition and sustainability via CRISPR-mediated metabolic engineering of Fusarium venenatum. Trends in Biotechnology.
- Finnigan, T., et al. (2019). Mycoprotein: The Future of Nutritious Nonmeat Protein, a Review. Current Developments in Nutrition.
- Regulació i Mercat:
- Sobre l'aprovació regulatòria a la Xina (2025): La Xina aprova el seu primer ingredient de micoproteïna
- Sobre seguretat alimentària: How gene-edited crops are regulated around the world (Nature).
- Wiebe, M. G. (2002). Myco-protein from Fusarium venenatum: a well-established product for human consumption. Applied Microbiology and Biotechnology.
Posts relacionats
-
Fongs radiotròfics: organismes que transformen radiació en vida
Publicat : 2025-06-09 13:25:44 -
Micologia forense: fongs al servei de la investigació
Publicat : 2025-05-17 19:36:29 -
La biosonificació fúngica: Fent música amb bolets
Publicat : 2025-11-05 18:37:50























